- Диализному врачу
- 1. Ведение пациентов с ХБП 4-5-й стадии.
- 2. Подготовка к трансплантации, диализу или к консервативной терапии
- 3. Физиологические принципы и моделирование кинетики мочевины
- 4. Оборудование для гемодиализа и расходные материалы
- 5. Вода для диализа и диализирующий раствор
- 6. Артериовенозные фистулы и протезы. Основные положения
- 7. Центральный венозный катетер в качестве доступа: основы
- 8. Мониторинг артериовенозного доступа и осложнений
- 9. Инфекции и другие осложнения центральных венозных катетеров
- 10. Назначение острого гемодиализа
- 11. Назначение хронического гемодиализа
- 12. Осложнения в ходе процедуры гемодиализа
- 13. Повторное использование диализаторов
- 14. Антикоагуляция
- 15. Продленная заместительная почечная терапия
- 16. Гемодиафильтрация
- 17. Терапевтический аферез
- 18. Актуальность сорбционных технологий сегодня
- 19. Руководство по диализу
Ведение пациентов с ХБП 4-5-й стадии. Подготовка к трансплантации, диализу или к консервативной терапии
Хроническую болезнь почек (Х Б П ) можно определить по-разному. Служба предупреждения болезней в СШ А (U S Preventive Health Service) определяет ее как снижение функции почек со скорректированной на размер тела расчетной скоростью клубочковой фильтрации (рСКФ/1,73 м 2) <60 мл/мин), или как почечное повреждение, персистирующ ее более трех месяцев.
Ведение пациентов с ХБП вклю чает в себя: скрининг, этиологический диагноз, установление стадии ХБП , идентификацию пациентов с вы соким риском прогрессирования и мероприятия по коррекции этих рисков; коррекцию осложнений ХБП; подготовку пациентов к трансплантации или заместительной почечной терапии.
I. СКРИНИНГ, ДИАГНОЗ И СТАДИЯ ХБП. Скрининг должен вклю чать в себя мониторинг наличия протеинурии и измерение почечной функции. Скрининг должен быть ориентирован на пациентов с факторами риска ХБП . Они вклю чаю т в себя диабет, гипертензию, сердечно-сосудистую патологию, курение, ожирение, возраст старш е 60 лет, определенную этническую и расовую принадлежность, семейный анамнез ХБП.
A. Измерение протеинурии. US Preventive Health Service рекомендует проводить оценку протеинурии в качестве скрининга у всех пациентов вы сокого риска. А мериканская диабетическая ассоциация (ADA) рекомендует проводить оценку микроальбуминурии у всех пациентов с диабетом II типа при его вы явлении и у всех пациентов с диабетом I типа через 5 лет после начала заболевания. Скрининг можно проводить по мочевым полоскам, но наиболее надежным методом является измерение отношения альбумина к креатинину в разовой утренней порции мочи. Полоски должны вы являть как альбумин, так и наличие эритроцитов и лейкоцитов в моче. Если полоски вы явили наличие клеток, следует провести микроскопический анализ осадка мочи. Табл. 1.1 представляет некоторые ограничения по использованию м очевы х полосок. Одной из проблем является то, что они измеряют только концентрацию и могут дать лож н о-отрицательные результаты в разведенной моче. Расчет отношения альбумина к креатинину (АКО) обходит эту проблему, поскольку как альбумин, так и креатинин одинаково подвергаю тся разведению , и эффект разведения мочи не проявляется. Н ормальная альбуминурия определяется как уровень меньш е 30 мг/г (меньш е 3 мг/ммоль); микроальбуминурией обозначается уровень 3 0 -3 0 0 мг/г (3 -3 0 мг/ммоль); макроальбуминурия - уровень выш е 300 мг/г (30 мг/ммоль). Эти границы в целом соотносятся с альбуминурией, оцениваемой в мг/день (то есть 30 и 300 мг/день) - в предположении, что за сутки экскретируется 1 г креатинина.
Ложноотрицательные результатыНизкая плотность мочи (<1,010)
Высокая концентрация солей в моче
Кислая моча
Неальбуминовая протеинурия
Ложноположительные результаты
Присутствие крови или семенной жидкости
Щелочная моча
Детергенты/дезинфектанты
Радиоконтрастные вещества
Высокая плотность мочи (>1,030)
В действительности суточная экскреция креатинина выш е; кроме того, она выш е у мужчин, чем у женщин, и у молодых выш е, чем у пожилых. Однако точное определение границ АКО фактически не имеет очень большого клинического значения, поскольку риск, связанны й с нарастанием экскреции альбумина, является непрерывной величиной и увеличивается с ростом альбуминурии даже в диапазоне меньш е 30 мг/день. Анализ АКО можно вы полнять в лю бое время суток, но утренний тест увеличивает чувствительность и с большей вероятностью исключает относительно благоприятные условия ортостатической протеинурии, когда протеинурия наблюдается в течение дня, но отсутствует, пока пациент спит лежа. Выявленный положительный тест АКО следует повторить как минимум дваж ды за три месяца для подтверждения п оложительного теста и исключения острого почечного повреждения.
B. Измерение почечной функции
1. Скорость клубочковой фильтрации (СкФ). СКФ, обычно вы раж аемая в мл/мин, это объем сы воротки крови, очищаемой почками в единицу времени. СКФ зави сит от размера тела и возраста, поэтом у однократно полученную величину СКФ следует оценивать в этом контексте. Обычно СКФ стандартизую т по площади поверхности тела, а именно по 1,73 м 2. У здоровы х пациентов в е личина СКФ/1,73 м 2 одинакова у мужчин и женщин, но обычно снижается с возрастом - от 115 мл/мин у молодых до 100 мл/мин в среднем возрасте, далее сниж аясь до 90, 80 и 70 мл/мин по достиж ении 60, 70 и 80 лет со о тветственно.
2. Сывороточный креатинин. Креатинин продуцируется с относительно постоянной скоростью из креатина в мыш цах и экскретируется почками как клубочковой фильтрацией, так и канальцевой секрецией. Нормальный диапазон составляет 5 3 -8 8 мкмоль/л (0 ,6 -1 мг/дл) у женщин, и 7 0 -1 1 5 мкмоль/л (0 ,8 1,3 мг/дл) у мужчин. Измерение креатинина - простой способ грубо оценить функцию почек, с ее падением уровень креатинина будет возрастать, поскольку его продукция сохранится на прежнем уровне. Отношение между сы вороточны м креатинином и функцией почек нелинейное, удвоение креатинина соответствует снижению СКФ примерно на 50%. Удвоение креатинина от исходно низкой величины приведет к сохранению уровня креатинина в «нормальном диапазоне», несмотря на сущ ественное снижение функции почек. На уровень сы вороточного креатинина влияет мыш ечная масса, недавнее потребление м яса и определенных препаратов (например, циметидин блокирует канальцевую секрецию креатинина, несколько увеличивает его уровень в сы воротке без какого-либо эффекта на СКФ). У пациентов с циррозом и асцитом оценка почечной функции по уровню креатинина о собенно сложна. Продукция креатинина м ож ет быть низкой из-за снижения мыш ечной массы, кроме того, часто трудно оценить истинный вес тела без асцита для стандартизации по размеру тела. У этих пациентов уровень креатинина 4 4 -8 8 мкмоль/л (0 ,5 -1 мг/дл) - формально нормальный, мож ет отраж ать умеренно и выраженно сниженную функцию почек. Даже у пациентов без кахексии уровень сы вороточного креатинина следует интерпретировать в контексте с мыш ечной массой. Например, сы вороточны й креатинин 115 мкмоль/л (1,3 мг/дл) м ож ет со ответствовать клиренсу креатинина 94 мл/ мин у молодого мужчины 80 кг или клиренсу креатинина только в 28 мл/мин у пожилой женщ ины 50 кг (M acgregor and M ethven, 2011).
До последнего времени сы вороточны й креатинин измерялся рядом методов, некоторые из которых (и з-за взаимодействия с другими вещ ествами в крови) давали сущ ественны е отклонения от «истинной» концентрации креатинина в крови, измеренного методом радиоизотопной дилюционной масс-спектрометрии (ID M S). В США и многих других странах лаборатории в настоящ ее время стандартизую т свои методы измерения по ID M S, и стан дартизованные величины оказы ваю тся несколько ниже.
3. клиренс креатинина по сбору мочи. Сбор мочи за определенное время (обычно за 24 часа) с измерением экскреции креатинина можно использовать для расчета клиренса креатинина (C lC r), который определяется как объем сы вор отки, очищенной от креатинина за минуту. Нормальное значение составляет примерно 95 ± 20 мл/мин у среднего размера женщ ины и 125 ± 25 мл/мин у среднего размера мужчины. П ациентов просят утром помочиться в туалет, отметить время начала сбора и в последующем собирать все порции мочи в контейнер в течение суток. На следующее утро пациент помещ ает последнюю порцию мочи в контейнер и отмечает время заверш ения периода сбора. Делением количества креатинина в собранной моче на число минут периода сбора лаборатория м ож ет рассчитать минутную скорость экскреции креатинина. В течение этих суток необходимо получить образец крови для измерения креатинина. Для расчета клиренса креатинина скорость экскреции креатинина в минуту делится на сы вороточны й уровень креатинина. Это дает оценку объема сы воротки, «очищенной» от креатинина почками. Например, если минутная экскреция креатинина составляет 1 мг/мин, а сывороточный уровень креатинина - 1 мг/дл (0,01 мг/мл), тогда 1,0/0,01 = 100 мл/мин: такое количество сы воротки очищ алось почками в среднем за минуту в течение периода сбора. Х отя технически сбор мочи в течение суток представляет определенные слож ности, этот метод измерения функции почек очень полезен у пациентов с кахексией, вклю чая таковы х с циррозом и асцитом, так ж е, как и у пациентов с ожирением. Полноту сбора мочи можно оценить, сравнивая количество полученного креатинина с ожидаемой суточной его экскрецией для пациента данного веса и пола. Следует ожидать экскреции креатинина около 1 5 -2 0 мг/кг тощей массы тела у женщин, и 2 0 -2 5 мг/кг у мужчин. Более точную оценку экскреции креатина можно получить по формуле, включающей вес тела, пол, возр аст и расу, такую, как разработана Ix (2011); расчет представлен в номограмме в Приложении А. Если экскреция креатинина значимо ниже ожидаемой, можно предположить неполный сбор мочи.
П оскольку креатинин помимо клубочковой фильтрации вы водится канальцевой секрецией, клиренс креатинина выш е, чем СКФ. При очень низкой СКФ/1,73 м 2 (например, ниже 1 0 -1 5 мл/мин) вы сока доля экскреции креатинина путем канальцевой секреции. Для получения более надежной оценки СКФ при низкой функции почек можно измерить клиренс креатинина и мочевины, а такж е уровень мочевины в крови. Клиренс мочевины рассчиты вается так ж е, как и для креатинина. М очевина фильтруется в клубочках, но некоторая доля ее реабсорбируется в канальцах. Таким образом, для мочевины ситуация обратная: из-за канальцевой реабсорбции клиренс мочевины ниже, чем СКФ. Показано, что средняя величина клиренсов по мочевине и по креатинину дает хорош ую оценку СКФ у пациентов с уровнем функции почек ниже 1 0 -1 5 мл/мин.
4. расчетный клиренс креатинина. Чтобы избеж ать неточности и неудобства со сбором мочи за определенное время, ClC r можно оценить по формулам, которые рассчиты ваю т минутную экскрецию креатинина на основе возраста, размера тела, пола и иногда расы. Одной из формул, которая для этого использовалась, является формула Кокрофта-Голта:
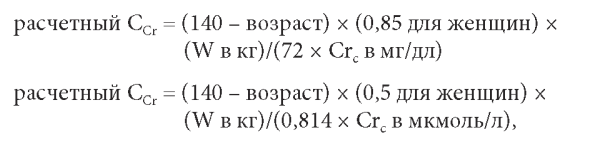
где W - это вес тела. Эта формула дает быструю и довольно точную оценку почечной функции. М ож но использовать позднее разработанную формулу Ix (2011), приведенную в Приложении А. Формула Ix была разработана и подтверждена на значительно большей популяции и основана на современных калиброванных по ID M S измерениях креатинина. Ни одна из формул не точна у пациентов со значимым ожирением или кахексией. Н екоторые авторы предполагают, что точность формулы Кокроф та-Голта можно улучшить, используя фактический вес тела при кахексии, идеальный вес тела для обычных пациентов и скорректированный вес тела при ожирении (Brown, 2013). См. Приложение В.
5. расчетная СкФ.
а) Формула Modification of Diet in Renal Disease (MDRD). Эта формула была разработана в исследовании MDRD и дает рСКФ, стандартизованную по площади поверхности тела в 1,73 м 2, для лабораторий, использующих стандартизованную по ID M S величину креатинина:
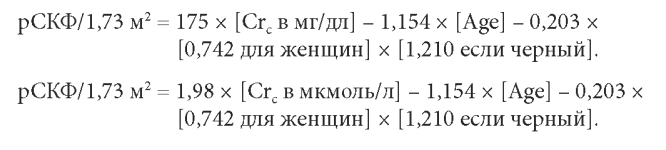
Величина «175» в формуле используется вм есто «186» в оригинальной публикации в связи с коррекцией по ID M S, для сопоставления с наборами, использованными в исследовании M D RD . При использовании величины креатинина, измеренного в мкмоль/л, нужно разделить величину сы вороточного креатинина на 88,5 для перевода в мг/дл.
Формула M D R D отличается от формул К окроф та-Голта и Ix. Вопервых, она была разработана по данным измерения СКА по иоталамату - вещ еству, которое не секретируется канальцами, и соответственно, представляет клубочковую фильтрацию, а не клиренс креатинина. При прочих равны х условиях формула M D R D дает более низкие значения почечной функции (СКФ ), чем клиренс креатинина, который включает в себя компонент канальцевой секреции. Во-вторы х, формула M D RD вклю чает стандартизацию по размеру тела и вы раж ает рСКФ/1,73. Клиренс креатинина, как полученный по результатам сбора мочи, так и по формулам К окроф та-Голта и Ix, является первичной оценкой клиренса креатинина, которая нуждается в коррекции по размеру тела.
b) Формула CKD-EPI. Она похож а на формулу M D RD , но подтверждена в большей группе пациентов, в которую входили и лица с легким снижением функции почек. Формула C K D -EP I представлена в Приложении А. Р азличия меж ду двумя формулами не являю тся клинически важными, поскольку они применяются, как правило, у пациентов с СКФ выш е 60 мл/ мин, где знание о точном уровне функции почек не так сущ ественно.
c) Формула на основе цистатина C. Альтернативным методом оценки СКФ я в ляю тся формулы, использующие сы вороточны й уровень цистатина C. Это белок молекулярным весом 13 кДа, продуцируемый всеми клетками, которые фильтруются в клубочках, но не реабсорбирую тся. Продукция цистатина C не связана с мыш ечной массой или потреблением мяса. В некоторых исследованиях показано, что в сравнении с формулами, осн ованными на креатинине, оценка СКФ по цистатину C лучше коррелирует с исходами лечения пациентов с ХБП . Н екоторые новейшие попытки предсказать СКФ комбинируют данные по сы вороточном у креатинину и цистатину C (Levey, 2014). Лабораторные методы измерения цистатина C не стандартизованы (хотя этот процесс идет), и в настоящее время формулы с цистатином C не использую тся широко.
6. Проблемы с оценкой клиренса при остром почечном повреждении. Расчетные формулы, основанные на креатинине или цистатине, предполагают стабильную ситуацию. Если бы удалить обе почки, сы вороточны е уровни креатинина и цистатина C начали бы подниматься, но это заняло бы несколько дней. П оэтому никакие из описанных выш е формул неполезны в ситуации, когда функция почек быстро изменяется. Сбор мочи за определенное время может быть полезен для измерения клиренса креатинина, но его уровень следует измерять в начале и в конце периода сбора, и минутную экскрецию креатинина нужно делить на среднюю по времени величину креатинина сы во ротки.
C. Ультразвуковое исследование и электролиты сыворотки. У пациентов с вы явленной ХБП следует получить изображение почек, как правило, ультразвуковое, чтобы оценить структурные аномалии и возм ож ную обструкцию. Следует такж е измерить сы вороточны е электролиты (Na, K, Cl, H C O 3) на предмет поиска м етаболического ацидоза и электролитных нарушений, наличие которых мож ет дать ключ к диагностике почечной патологии.
D. Поиск этиологического диагноза. Идентификация причины Х БП является весьм а важной. Х БП мож ет быть обратима, например, у пациентов с билатеральным реноваскулярным стенозом или хронической обструкцией шейки мочевого пузыря при гипертрофии простаты. Причина Х БП м ож ет дать представление о темпе ее прогрессирования. П оскольку некоторые почечные заболевания с высокой вероятностью развиваю тся в почечном трансплантате, их выявление важ но для дальнейшего принятия решений.
E. Стадии. Широко принято разделение по стадиям Х БП в соответстви и с инициативой K D O Q I1 Национального почечного фонда2. Стадии разделяю тся от первой, самой легкой, до пятой, наиболее тяжелой на основе уровней рСКФ, стандартизованны х по площади поверхности тела. Д ве легкие стадии (1 и 2), при которых СКФ все еще выш е 60 мл/мин, требую т наличия признаков почечного повреждения, помимо сниженной СКФ. Почечное повреждение мож ет м анифестировать патологическими изменениями по результатам почечной биопсии, аномалиями в составе крови и мочи (протеинурия или изменение осадка мочи) или аномалиями на визуализирующ их исследованиях. Более тяжелые стадии Х Б П - 3, 4, 5-я - имеются по определению, когда СКФ ниже 60, 30 и 15 мл/мин соответственно. Н екоторые пож илые пациенты с рСКФ в диапазоне 4 5 -6 0 мл/мин могут не иметь признаков почечного повреждения и повыш енных рисков ускоренного снижения почечной функции или летальности. Это обстоятельство было отчасти учтено в последующем развитии системы разделения по стадиям Х Б П в инициативе K D IG O (Kidney Disease: Improving Global O utcom es). Стадия Х Б П 3 была разделена на два уровня: 3а с рСКФ 4 5 -5 9 мл/ мин и 3б с рСКФ 3 0 -4 4 мл/мин. Также в новую систему была внесена степень протеинурии, измеренная по АКО. Н овая система представлена в табл. 1.2, где низкий риск осложнений и прогрессирования Х Б П обозначен зеленым, а его последовательное возрастание - ж елты м, оранжевым и красным.
II. замедление прогрессирования хбп и сердечно-сосудистой патологии. У пациентов с ХБП факторы риска прогрессирования заболевания очень похож и на риски сердечно-сосудистой патологии. Одной из целей раннего вы явления пациентов с ХБП является попытка скорректировать или ослабить эти риски в надежде поддержать функцию почек и минимизировать сердечно-сосудистые риски. Главными ф акторами риска являю тся: курение, артериальная гипертензия, гипергликемия у пациентов с сахарным диабетом (а возм ож но и у пациентов без него), гиперлипидемия, анемия и гиперфосфатемия. Протеинурия и даже микроальбуминурия значимо повыш аю т риски как прогрессирования ХБП , так и сердечно-сосудисты х ослож нений. Уровни воспалительны х медиаторов, особенно С-реактивного белка (С РБ), возр астаю т при ХБП и связаны с повыш енными рисками атеросклероза.
A. Прекращение курения. Курение является традиционным сердечно-сосудистым риском, и его прекращение важ но с этой точки зрения. Сущ ествую т свидетельства, что курение такж е ускоряет прогрессирование ХБП , что подчеркивает важ ность его прекращения у этих пациентов.
B. контроль АД и протеинурии. Представление о целевы х уровнях АД у пациентов с Х Б П находится в продолжающ емся развитии. KDIGO и KDOQI рекомендуют в этом качестве уровень меньше 130/80 мм рт. ст. для всех пациентов с ХБП независимо от наличия диабета и степени протеинурии. Однако рекомендации Eighth Joint National Com m ittee (JN C 8), опубликованные в 2013 году, предлагаю т менее агрессивную цель - меньше 140/90 мм рт. ст. у пациентов моложе 60 лет с диабетом и ХБП.

Примечание. Зелены й - нет повышенного риска, если нет других маркеров болезни почек, нет ХБП; желтый - умеренно повышенный риск; оранжевый - высокий риск; красный - очень высокий риск. * - нет ХБП, если нет изменений в моче, структурных или патологических изменений. Риск прогрессирования может быть умеренно повыш ен при определенны х болезнях почек. Модифицировано из: Kidney Disease: Im proving Global Outcomes (KDIGO) CKD W ork Group. KDIGO 2012 Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease. KidneyIntSuppl. 2013; 3: 1 -1 5 0 .
Н езависимо от того, имеется ли гипертензия, использование ингибиторов АПФ/блокаторов рецепторов ангиотензина (иАПФ/БРА) рекомендуется для замедления прогрессирования Х Б П у пациентов с диабетической нефропатией, а такж е у недиабетических пациентов с Х БП с протеинурией (отнош ение белка к креатинину в разовом анализе больше 200 мг/г). Тиазидовые диуретики являю тся препаратом вы бора среди диуретиков для ранних стадий Х Б П при уровне креатинина ниже 160 мкмоль/л (меньше 1,8 мг/дл). При более вы соких уровнях рекомендую тся петлевые диуретики (дваж ды в день) из-за предполагаемой неэффективности тиазидовы х диуретиков. Однако отсутствие эффективности последних у пациентов со сниженной СКФ не доказано. Хлорталидон, пролонгированный диуретик, эффективен при ХБП в снижении гидратации (Agarwal, 2014) до степени, когда наблюдались признаки дегидратации.
Дозы иАПФ/БРА титруются до минимизации протеинурии, но после начала лечения и после каждого изменения дозы требуется мониторинг АД, калия и креатинина. Ограничение соли и использование диуретиков повыш ает антипротеинурический эффект иАПФ/БРА. П ротивопоказаны иАПФ/БРА беременным, особенно позднее первого триместра, и пациентам с анамнезом ангионевротического отека. У пациентов с СКФ больше 15 мл/мин редко требуется уменьш ать дозу гипотензивны х препаратов с учетом сниженной экскреции. Х отя время полужизни в плазме некоторых классов гипотензивны х препаратов возр астает.
C. Бета-блокаторы и аспирин: кардиопротективные эффекты. Бета-блокаторы обеспечиваю т кардиопротекцию у пациентов с ХБП , хотя они более не рекомендуются JN C 8 как препараты первой линии в лечении гипертензии. Кардиопротекция аспирином и бета-блокаторами после инфаркта миокарда у пациентов с ХБП и с нормальной функцией почек одинакова. Применение аспирина связы вали с желудочно-киш ечными кровотечениями у пациентов с ХПН. П рисутствует ли этот риск у пациентов с ХБП 1 -4, достоверно неизвестно.
D. Строгий контроль гликемии у пациентов с диабетом при ХБП. И сследования пациентов с диабетом I или II типа продемонстрировали, что строгий контроль гликемии замедляет развитие микро- и макроваскулярной патологии. Он такж е снижает скорость прогрессирования почечной патологии у диабетических пациентов с ХБП . Целью гликемического контроля следует считать уровень гликозилированного гемоглобина меньше 7%. Однако последние рекомендации Американской диабетологической ассоциации (АДА) подчеркивают важ н ость индивидуализации целевых уровней H bA 1C у пациентов с диабетом II типа, а рекомендации KDIGO предлагают ослабить эти требования у пациентов с риском гипогликемии или существенной сопутствующей патологией.
E. гиполипидемическая терапия. Повышенный уровень холестерина и липопротеидов низкой плотности (ЛН П) и других липидных маркеров является традиционным фактором риска для сердечно-сосудистой патологии, и кардиопротективный эффект статинов у пациентов без ХБП даже с уровнем холестерина в нормальном диапазоне описан в нескольких исследованиях. В экспериментальных исследованиях показано, что нагрузка холестерином мож ет утяж елить гломерулярное повреждение, таким образом, лечение пациентов с ХБП статинами для снижения уровня липидов мож ет как предотвратить прогрессирование ХБП, так и понизить сердечно-сосудистые риски. Последние рекомендации Am erican College of Cardiology (ACC) и A m erican Heart Association (AHA), которые адресованы общей популяции, а не пациентам с ХБП, идентифицируют четыре группы пациентов для первичной и вторичной профилактики статинами.
1. Лица с клиническими признаками атеросклеротической сердечно-сосудистой патологии.
2. Лица с уровнем ЛНП выше 4,9 ммоль/л (190 мг/дл).
3. Пациенты с диабетом 40 -7 5 лет без сердечно-сосудистой патологии с уровнем ЛНП от 1,8 до 4,9 ммоль/л (70 -189 мг/дл).
4. Пациенты без признаков сердечно-сосудистой патологии с уровнем ЛНП от 1,8 до 4,9 ммоль/л (70 -189 мг/дл) и 10-летним риском атеросклеротической сердечно-сосудистой патологии больше 7,5%.
Теоретически пациенты с ХБП могут лечиться по той же схеме, поскольку при использовании калькулятора риска AHA (см. ссылку на калькулятор AHA по Goff [2014]) почти все пациенты старше 63 лет даже при «оптимальных уровнях» (по меркам калькулятора) систолического АД, холестерина ЛНП и ЛВП без диабета будут иметь 10-летний риск сердечно-сосудистой патологии выше 7,5% и без ХБП. Тем самым рекомендации вызывают вопросы в отношении интенсификации терапии статинами. В 2013 году рекомендации KDIGO предложили, чтобы все пациенты с ХБП (СКФ меньше 60 мл/мин) не на диализе и в возрасте старш е 50 лет получали лечение статинами или комбинацией статин/ эзетимиб. Пациентам старше 50 лет, с СКФ выш е 60 мл/мин (то есть ХБП 1-2 ) следует назначать только статины, поскольку нет достоверны х данных об эффективном применении комбинации статин/эзетимиб в этой группе. Наконец, более молодые пациенты с ХБП (18 -49 лет) не на диализе должны получать лечение статинами, если у них имеется коронарная патология, сахарный диабет, инсульт в анамнезе или 10-летний сердечно-сосудистый риск выше 10%. Рекомендации KDIGO 2013 года предлагают не начинать терапию статинами у диализных пациентов, но если статины были назначены пациентам ранее, их отменять не следует.
У недиализных пациентов с ХБП преимущ ества от терапии гиполипидемическими препаратами, по-видимому, присутствую т независимо от уровня ЛНП. Сущ ествует тенденция использовать сердечно-сосудистый риск и наличие коморбидности, а не уровень ЛДЛ в качестве показания к терапии. Для более детального обсуждения дислипидемии при ХБП 5 ст. у пациентов, получающих диализ.
1. Статины: кардиопротективные эффекты. Кардиопротективные эффекты статинов, хорош о документированные у пациентов без уремии, не вполне убедительны у диализных пациентов, хотя эф фективность у пациентов без диализа подтверждена. И спользование статинов замедляет прогрессирование ХБП в некоторых исследованиях (Deedwania, 2014).
а) коррекция дозы при почечной недостаточности. Применение статинов (как класса) связано с рабдомиолизом, и при почечной недостаточности рекомендуется снижение дозы для некоторых статинов (например, розувастатина) или при использовании в комбинации с фибратами.
2. Эзетимиб. Эзетимиб является ингибитором абсорбции холестерина и снижает уровни ЛНП , триглицеридов и аполипопротеина В в плазме, повышая ур овни ЛВП . Как и статины, эзетимиб имеет выраженный антиатеросклеротический, противовоспалительны й и антиоксидантный эффект (Katsiki, 2013). Исследование SHARP, где как диализные, так и додиализные пациенты получали комбинацию симвастатина с эзетемибом (Sharp Collaborative Group, 2010), сформировало базу для рекомендаций по использованию эзетимиба у пациентов с ХБП без диализа. Однако осталось неясным, в какой мере полученные эффекты следует относить к использованию симвастатина, а в какой мере к добавлению эзетимиба.
B. Ограничение белка. Тезис обограничении белка в качестве лечебного мероприятия для замедления прогрессирования ХБП остается противоречивым. В экспериментальных исследованиях продемонстрировано, что диета с высоким содержанием белка приводит к гистологическим аномалиям в почках и к протеинурии. Более того, ограничение потребления белка замедляет прогрессирование. Однако в рандомизированных клинических исследованиях эффект ограничения белка оказы вается очень малым и труднодостижимым. Тем не менее свидетельства, полученные в метаанализе, предполагают некоторые преимущества от ограничения белка в снижении прогрессирования ХБП. Одним из рациональных подходов является ограничение белка до 0,8 г/кг в день у всех пациентов с ХБП . Рекомендации отличаются от многих других предложений в отношении преимущества от дальнейшего ограничения. Рекомендации KDOQI 2000 года предлагают ограничить потребление уровнем 0,6 г/кг в день при рСКФ меньш е 25 мл/мин. При этом канадские, многие европейские и недавние KDIGO не рекомендуют понижать уровень потребления белка ниже 0,8 г/кг в день при любом уровне почечной функции. Особенно внимательно при принятии решения об ограничении белка следует относиться к пациентам с нарушениями питания. Пациенты с белково-энергетической недостаточностью на старте диализа имеют худшую выживаемость, чем пациенты с нормальным питанием, а ограничение вы бора питания всегда несет в себе риски ухудш ения нутриционного статуса. Тщательное наблюдение за любыми проявлениями белково-энергетической недостаточности - по клиническим параметрам или по уровню альбумина - исключительно важно. Таких пациентов должны тщ ательно наблюдать диетологи. Рекомендуемое потребление энергии составляет 30 -35 ккал/кг/день. У пациентов с Х БП 4 -5 признаки ухудшения нутриционного статуса являю тся одним из ключевых факторов в принятии решения о начале диализной терапии.
III. ВЕДЕНИЕ ОСЛОЖНЕНИЙ ХБП
A. коррекция анемии. Анемия часто встречается у пациентов с ХБП . С прогрессированием Х Б П частота и распространенность анемии возрастаю т. Она имеет многофакторную этиологию. Наиболее частыми причинами являю тся дефицит эритропоэтина и железа, а такж е воспаление. Наблюдательные исследования демонстрируют увеличение риска сердечно-сосудисты х и почечных ослож нений, низкое качество ж изни и более вы сокую летальность с нарастанием анемии. Однако крупные рандомизированные исследования показали, что коррекция анемии до уровня гемоглобина в 130 г/л и выше при помощи эритропоэзстимулирующ их средств (ЭСС ) связана с возрастанием риска сердечно-сосудистых осложнений, инсультов, и/или смерти. Кроме того, коррекция анемии не приводила к замедлению прогрессирования ХБП или снижению частоты развития ХПН . Недавние исследования показали связь меж ду использованием вы соких доз ЭСС и повыш енными рисками побочны х эффектов. Неясно, в какой мере данную связь можно считать причинно-следственной, либо она отражает известную взаимосвязь меж ду резистентностью к ЭСС с плохими исходами при использовании относительно высоких целевых значений гемоглобина. Современный подход к коррекции анемии подчеркивает важ ность лишь частичной коррекции анемии с использованием возм ож но более низких доз ЭСС параллельно с коррекцией дефицита анемии и воспаления.
1. Начало терапии ЭСС и границы гемоглобина. Диагностика и ведение анемии у пациентов до диализа аналогичны таковым при ХПН и обсуждены в деталях в главе 34. Рекомендации KDIGO предлагают не начинать терапию эритропоэтином, пока гемоглобин не опускается ниже 100 г/л. Они предлагают поддерж ивать уровень гемоглобина между 90 и 115 г/л, хотя US FDA рекомендует уменьш ать дозировку или отменять эритропоэтин, если уровень гемоглобина превыш ает 110 г/л. Терапию анемии при ХБП следует индивидуализировать, и одной из главных целей должно стать снижение потребности в гемотрансфузиях. Рекомендации KDIGO предлагают проявлять осторож ность у пациентов с инсультом или опухолями в анамнезе. Таким образом, целевой уровень гемоглобина, по крайней мере в США, составляет от 90 до 110 г/л. Сущ ествуют противоречивы е мнения относительно того, не явл яется ли слишком низким уровень гемоглобина в 90 г/л, поскольку он может увеличивать трансплантацию почки их сенсибилизирующ ему эффекту.
2. Типы терапии ЭСС. Сущ ествую т ЭСС короткого и длительного действия. Эритропоэтин альфа, одобренный в 1989 году и доступны й во всем мире, является препаратом короткого действия со временем полужизни около 8 часов при внутривенном введении и 16 -24 часа - при подкожном. Несколько различных ЭСС короткого действия и их биоаналогов доступны на рынках вне США. Типичной дозой для этих препаратов является 4000 -6000 ЕД подкож но один раз в неделю. Чаще всего используемый препарат длительного действия - дарбэпоэтин альфа с временем полужизни 25 и 50 часов при внутривенном и подкожном введении соответственно. Оптимальной схемой применения дарбэпоэтина у стабильны х пациентов является еженедельное введение в дозе 2 0 -3 0 мкг или каждые две недели - 40 -60 . Дозы не различаются при внутривенном и подкожном введении. Вне США одобрен и применяется другой препарат длительного действия CERA 3, который является соединением водорастворимого полиэтиленгликоля и молекулы эпоэтина бета. Время полужизни составляет 136 часов, и CERA рекомендуется для применения один раз в две недели и раз в месяц в поддерживающую фазу. Типичная доза - 150 мкг/месяц.
3. Частота и путь применения ЭСС. Частота применения ЭСС учитывает удобство пациента и эффективность терапии. У додиализных пациентов препараты длительного действия предпочтительнее, поскольку связаны с меньшей частотой введений и посещений врача, в случае если пациент неможет вводить препарат самостоятельно. Впрочем, короткодействующие препараты можно применять один раз в неделю или даже в две недели с сопоставимым эффектом.
4. Резистентная анемия. Резистентность к терапии ЭСС определяется по отсутствию увеличения гемоглобина после первого месяца терапии в адекватной дозе. KDIGO рекомендует при эскалации дозы не превыш ать двойную начальную дозу с учетом веса тела. Более того, KDIGO рекомендует избегать превыш ения четырехкратной начальной дозы с учетом веса тела. У пациентов с исходной или приобретенной резистентностью следует провести поиск ее конкретных причин.
B. коррекция дефицита железа. Дефицит железа присутствует у 40% преддиализных пациентов и является наиболее частой причиной кажущейся резистентности к ЭСС. Существует много причин для дефицита железа, включая снижение абсорбции железа, потерю крови в связи с частыми заборами или в результате скрытых желудочно-кишечных потерь, сниженное потребление с пищей.
1. Оценка дефицита железа. Состояние обмена железа (запасы железа и уровень биодоступного железа) необходимо регулярно оценивать у пациентов с ХБП . Ферритин является белком для хранения железа, и уровень сывороточного ферритина отражает запасы железа. Кроме того, сывороточный ферритин является белком острой фазы, а пациенты с ХБП часто демонстрируют состояние хронического воспаления. Поэтому уровень ферритина с пациентами с признаками воспаления следует интерпретировать с осторожностью . Сывороточны й уровень ферритина - наилучший предиктор дефицита железа (при уровне меньш е 100 мкг/л), но вы сокие значения менее информативны. Насыщение трансферрина (TSA T = железо сы воротких 100 / общая железосвязы вающая способность сыворотки) - наиболее широко применяемый метод измерения биодоступности железа. TSA T <20% указывает на низкую доступность железа при ХБП . Дефицит железа может снижать эффективность терапии ЭСС , а терапия железом обычно неэффективна без ЭСС у пациентов с ХБП . Следовательно, перед началом терапии ЭСС необходимо оценить статус железа.
2. Лечение железодефицитной анемии. Лечение зависит от стадии Х Б П и включает в себя пероральную и внутривенную терапию. Пероральная терапия предпочтительна при лечении пациентов с ХБП без диализа и рекомендова на KDIGO как начальный подход к коррекции дефицита железа. Стратегии по улучшению всасывания перорального железа включают пероральный прием таблеток только натощак, отказ от применения кишечнорастворимых форм и исключение совместного приема с фосфатсвязывающими препаратами. Внутривенные препараты могут понадобиться пациентам, которые не отвечают на пероральную терапию или имеют продолжающиеся большие потери железа (например, хронические кровопотери из желудочно-кишечного тракта). Рекомендуется использование низкомолекулярных препаратов железа: низкомолекулярные декстраны, глюконат железа, сахарат железа, феррумокситол. И спользование высокомолекулярных декстранов железа было связано с риском тяжелых анафилактических реакций.
Целью пероральной терапии является поступление примерно 200 мг элементарного железа в день, что эквивалентно приему сульфата железа по 325 мг три раза в день; каждая таблетка содержит 65 мг элементарного железа. Если восполнение дефицита железа не произошло за 1 -3 месяца, следует рассмотреть внутривенную терапию. Внутривенное введение может осуществляться в одной большой дозе или повторно в меньших дозах, в зависимости от используемого препарата. Начальный курс внутривенной терапии предполагает введение 1000 мг железа. Курс можно повторить, если не удалось повысить уровень гемоглобина и/или снизить дозу ЭСС . Статус обмена железа следует мониторировать каждые три месяца (TSA T и ферритин), пока пациент получает ЭСС , и чаще - при начале или увеличении дозы ЭСС , в условиях продолжающихся кровопотерь или в других обстоятельствах, когда запасы железа могут истощаться.
C. Минеральные и костные нарушения при хронической болезни почек (МкН-ХБП). Патогенез МКН -ХБП представлен на рис. 1.1. Коррекция уровня фосфатов, витамина D и паратгормона (ПТГ) у пациентов на диализе детально обсуждена в главе 36. Ниже затронуты только вопросы, относящиеся к додиализной ХБП.
1. гиперфосфатемия. Гиперфосфатемия является фактором риска летальности и неблагоприятных сердечно-сосудисты х исходов как при ХБП , так и при ХПН . Даже у пациентов без ХБП легкое повышение уровня фосфатов связано с увеличенными сердечно-сосудистым и рисками. Гиперфосфатемия связана с риском сосудистой кальцификации и левожелудочковой гипертрофии при ХПН . В ряде экспериментальных моделей гиперфосфатемия ускоряла прогрессирование почечной недостаточности. В этих моделях она стимулировала рост паращитовидных желез и секрецию ПТГ.
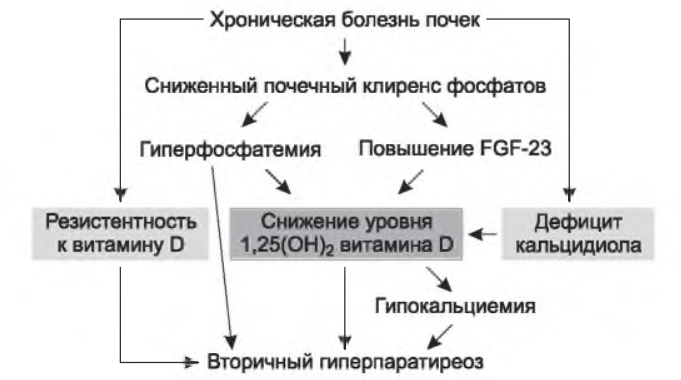
РИСУНОК 1.1. Патогенез минеральных и костных нарушений. Воспроизведено с разрешения Macmillan Publishers Ltd из: Nigwekar SU, Tamez H, Thadhani RI. Vitamin D and chronic kidney disease-mineral bone disease (CKD-MBD). Bonekey Rep. 2014; 3: 498. eCollection 2014
a) коррекция диетой. Диетические ограничения вклю чают в себя тщательный анализ избыточного потребления богатых фосфатами продуктов, включая молочные продукты, определенные напитки и полуфабрикаты. Кроме того, следует тщательно проанализировать диету с точки зрения содержания в ней продуктов с фосфатными добавками. Потребление фосфора должно быть ограничено до 800 -1000 мг в день (26 -32 ммоль/день).
b) Целевые уровни кальция и фосфатов. Предыдущие рекомендации предлагали поддерживать кальций на верхней границе нормы для обеспечения подавления секреции паратгормона. В настоящее время они заменены на установку стремиться к средней или нижней части диапазона, чтобы минимизировать сосудистую кальцификацию. Аналогично уровень фосфатов следует поддерживать в нормальном диапазоне.
c) Фосфатсвязывающие препараты (ФСП). Пациентам с додиализными стадиями ХБП мож ет потребоваться применение ФСП. Их выбор рассмотрен в главе 36. Ж елательно ограничить прием кальция до 1,5 г/день (37 ммоль/ день), чтобы минимизировать риск кальцификации; рекомендации K DOQI менее строги и предлагают предел в 2 г/день (50 ммоль/день). Это означает, что при использовании солей кальция в качестве ФСП мож ет потребоваться комбинировать их с севеламером, лантаном или, возм ож но, с магнием или одним из новы х железосодерж ащ их ФСП, описанны х в главе 36. Как правило, алюминий-содержащие ФСП не следует использовать. И спользование севеламера, вероятно, стабилизирует скорость сосудистой кальцификации у пациентов с ХБП и улучшает исходы, хотя результаты исследований не очень определенны в этой области. Высказывается суждение, что если и существует положительный эффект, он может частично объясняться эффектом снижения уровня липидов при терапии севеламером, кроме того, он имеет дополнительный проти вовоспалительный эффект и может снижать уровень FG F23; уровень последнего значимо повышается у пациентов с ХБП и связан с худшими исходами. Это остается темой продолжающихся исследований.
2. Уровень паратгормона в сыворотке. Для контроля уровня ПТГ важно минимизировать степень паратиреоидной гипертрофии и риск развития крупных неподавляемых узлов в паращитовидных железах. Контроль секреции ПТГ детально обсуж ден в главе 36.
a) Частота измерений. Рекомендации KDIGO 2009 по МНК -ХБП предлагают измерять уровень ПТГ у пациентов с рСКФ меньше 60 мл/мин, хотя у п ож илы х пациентов с рСКФ 40 -65 мл/мин и с низкими факторами риска прогрессирования ХБП в этом, возможно, нет необходимости. Частота измерений для пациентов с рСКФ в диапазоне 3 0 -6 0 мл/мин - один раз в 12 месяцев, и каждые три месяца у пациентов с рСКФ в диапазоне 15 30 мл/мин.
b) Целевые уровни ПТг. Наборы для определения «интактного» ПТГ доступны с 90-х годов и выявляю ткак целую молекулу (1,84), так и фрагмент (7,84); большинство биопсийных исследований, на основании которых установлены целевые диапазоны, выполнены с использованием этих наборов. Биоинтактный ПТГ, обозначаемый также как biPTH или whole PTH (целая молекула), определяется новым набором, обеспечивающим вы явление только целой молекулы ПТГ 1,84; уровни П ТГ оказались вдвое ниже таковых для «интактного» ПТГ. Оба набора можно использовать для диагностики и контроля лечения у пациентов с ХБП, но целевые уровни будут различными. С прогрессированием ХБП костная ткань становится резистентной к действию ПТГ, соответственно, необходимо устанавливать целевые диапазоны для различных уровней функции почек. П ервоначальные рекомендации KDOQI определяли разные целевые диапазоны при различны стадиях почечной недостаточности. Но, учитывая широкие вариации среди используемых наборов и неопределенность преимуществ достижения целей, рекомендации KDIGO 2009 просто предлагали у додиализных пациентов определять ПТГ и любое (специфичное для каждого набора) стабильное повышение или рост ПТГ считать основанием для начала терапии препаратами витамина D. У диализных пациентов целевой диапазон ПТГ определен как 2-9-кратное превышение верхней границы нормы.
3. Уровень щелочной фосфатазы сыворотки. Щелочная фосфатаза присутствует в костной ткани и является индикатором скорости костного обмена. Высокий ее уровень, особенно в сочетании с повыш енным ПТГ, является надежным индикатором повыш енной активности паращ итовидных желез, которую требуется подавлять. Текущие рекомендации KDIGO предлагают определять щелочную фосфатазу ежегодно, начиная с уровня ХБП 4.
4. Витамин D. Уровень 2 5(O H )D 3 довольно низкий, возможно, и з-за дефицита инсоляции и снижения потребления продуктов, богатых витамином. С прогрессированием Х Б П превращение 25(O H )D 3 в 1,25(O H )2D 3 при помощи 1-альф а-гидроксилазы снижается, и даже при адекватном поступлении 2 5(O H )D 3 уровень 1,25(O H )2D 3 может быть снижен, и подавление секреции ПТГ будет неадекватным. Витамин D воздействует на многие органы и системы. Большинство этих эффектов позитивны, хотя избыток витамина связывали с сосудистой кальцификацией и даже прогрессированием почечной недостаточности. Фермент 1-альф а-гидроксилаза присутствует в ряде тканей, что, возможно, указывает на необходимость для оптимального состояния здоровья обеспечить нормальный уровень в циркуляции как 2 5(O H )D 3, так и 1,25(O H )2D 3. Недавно применение активных форм витамина D связали с улучшением выживаем ости и сердечно-сосудисты х исходов у пациентов с ХПН. Механизм этого неясен; данные получены в наблюдательных исследованиях и требуют подтверждения. В небольшом рандомизированном исследовании витамин D снижал протеинурию и замедлял прогрессирование ХБП. Витамин В также может улучшать чувствительность к эритропоэз-стимулирующим средствам и улучшать течение анемии, снижая воспаление.
а) Целевые уровни 25(OH)D3 при ХБП. Уровень витамина в сыворотке должен составлять как минимум 30 нг/мл (75 ммоль/л). Низкий уровень был связан с мышечной слабостью у пожилых пациентов без ХБП. Поскольку пациенты с ХБП имеют, как правило, очень низкие уровни 25(O H )D 3, они должны получать 1000-2000 ЕД холекальциферола в день; возможно, потребуется большая доза. Холекальциферол в СШ А доступен только как безрецептурная добавка. Эта добавка не влияет на желудочно-кишечную абсорбцию кальция или фосфатов. В 2003 году KDOQI рекомендовала использовать для коррекции низкого уровня 2 5(O H )D 3 эргокальциферол, который несколько менее эффективен, чем холекальциферол и доступен в относительно больш их дозах, рассчитанных на применение еженедельно или ежемесячно. Для США его преимущество состоит в том, что он доступен в форме лекарственного препарата.
b) когда применять активные формы витамина D. В более тяжелых стадиях ХБП переход 2 5(O H )D 3 в 1,25(O H 2)D 3 становится недостаточным, и даже при нормальных запасах 2 5(O H )D 3 сывороточный уровень 1,25(O H )2D 3 может оставаться низким. В такой ситуации секреция паратгормона адекватно не подавляется. У пациентов с Х БП 3 - 4 при превышении паратгормона целевых уровней, несмотря на адекватное содержание 25(O H )D 3, показано применение активной формы витамина D. Выбор и дозы активных форм (кальцитриол, парикальцитол, доксеркальциферол) обсуждены в главе 36. Как и у диализных пациентов, дозу витамина D следует снижать при развитии гиперкальциемии и гиперфосфатемии.
5. Цинакальцет. Цинакальцет является кальцимиметиком, который повышает чувствительность рецепторов к кальцию на паращ итовидных железах, приводя к снижению секреции ПТГ. Одним из главных преимущ еств цинакальцета является возм ож н ость использовать его у пациентов с высоким уровнем фосфатов, где применение активны х форм витамина D для подавления ПТГ противопоказано (активные формы повыш аю т желудочно-киш ечную абсорбцию фосфатов и могут привести к гиперфосфатемии). Показано, что цинакальцет сниж ает уровень П ТГ у пациентов с ХБП3 -4 . Относительная роль цинакальцета и активны х форм витамина D у додиализных пациентов не определена. В действующей в США инструкции цинакальцет не показан для преддиализных пациентов, и KDIGO 2009 также не рекомендует его использование в додиализной популяции.
D. Осложнения, связанные с нарушениями электролитного и кислотно-основного баланса. Разнообразные электролитные нарушения могут проявиться по мере снижения функции почек. Наиболее явной является гиперкалиемия. Часто развивается ацидоз, но он, как правило, легкий, с нормальным анионным разры вом, пока снижение почечной функции не становится тяжелым. Лечение острой гиперкалиемии будет обсуж дено в дальнейшем. Хроническая гиперкалиемия обычно является результатом вы сокого потребления калия с богатыми калием продуктами, такими как фрукты. Гиперкалиемия такж е часто вы является у пациентов, получающих ингибиторы АПФ/БРА или антагонисты минерал-кортикоидных рецепторов, таких как альдостерон. Также часто она наблюдается у пациентов, принимающих противовоспалительны е нестероидные препараты и триметоприм. Недавняя разработка новы х желудочно-киш ечных сорбентов для всасы вания калия п озволяет шире использовать антагонисты к системе «ренин-ангиотензин-альдостерон».
Хронический метаболический ацидоз приводит к повыш енной резорбции костей и связан с большей скоростью прогрессирования ХБП . Рекомендуется прием натрия бикарбоната для поддержания сы вороточного уровня бикарбоната выш е 22 ммоль/л. Обычное количество бикарбоната на прием составляет 0 ,5 -1 ,0 ммоль/кг/день. В нескольких небольш их рандомизированных исследованиях показано замедление прогрессирования Х Б П в результате этой терапии.
IV. подготовка ПАЦИЕНТА к ДИАЛИЗУ. В задачи по подготовке пациента к диализу или додиализной трансплантации входят установка сосудистого или перитонеального доступа, выбор наиболее подходящей модальности диализа и места ее проведения (перитонеальный диализ, гемодиализный центр, домашний гемодиализ), вакцинация, продолжаю щ аяся нутриционная поддержка, особенно в части контроля фосфатемии, предотвращ ение перегрузки ж идкостью и гипертензии. Эти задачи в деталях определены в следующ их главах.
Ссылки и рекомендуемая литература
Agarwal R, et al. Chlorthalidone for poorly controlled hypertension in chronic kidney disease: an interventional pilot study. Am JN ep h ro l. 2014; 39: 171-182.
Am erican Diabetes Association. Executive summary: standards of medical care in diabetes - 2012. D iabetes C are. 2012; 35 (suppl 1): S4-S10.
Brown DL, Masselink AJ, Lalla CD. Functional range of creatinine clearance for renal drug dosing: a practical solution to the controversy of which weight to use in the Cockcroft-G ault equation. A nn Pharm acother.
2013; 47: 1039-1044.
Daugirdas JT, ed. H an d book o f Chronic Kidney D isease M anagem ent. Wolters Kluwer; Philadelphia, 2011.
Deedwania PC. Statins in chronic kidney disease: cardiovascular risk and kidney function. Postgrad M ed. 2014;
126: 2 9 -3 6 . Eckardt KU, et al. Evolving importance of kidney disease: from subspecialty to global health burden. Lancet. 2013; 382: 158-169.
Fink HA, et al. Screening for, m onitoring, and treatm ent of chronic kidney disease stages 1 to 3: a systematic review for the U.S. Preventive Services Task Force and for an Am erican College of Physicians Clinical Practice Guideline. A nn Intern M ed. 2012; 156: 570-581.
G off DC Jr, et al. 2013 ACC/AHA Guideline on the Assessment of Cardiovascular Risk: J A m Coll Cardiol. 2014;
63: 2 9 3 5 -2 9 5 9 . Downloadable CV Risk calculator in Excel format: http://static.heart.org/ahamah/risk/Omnibus_Risk_Estimator.xls. Доступ 28 апреля 2014 г. Ix JH, et al. Equations to estimate creatinine excretion rate: the CKD epidemiology collaboration. Clin J A m Soc N ephrol. 2011; 6: 184-191.
James PA, et al. 2014 evidence-based guideline for the management of high blood pressure in adults: report from the panel members appointed to the Eighth Joint National Com mittee (JNC 8). JA M A . 2014; 311: 50 7-520.
Katsiki N, et al. Ezetimibe therapy for dyslipidemia: an update. Curr P harm Des. 2013; 19: 3107-3114. Kidney Disease: Improving Global Outcomes (KD IG O) Anemia W ork Group. KD IG O Clinical Practice G uideline for Anem ia in Chronic Kidney Disease. K idney Int Suppl. 2012; 2: 2 7 9-335.
Kidney Disease: Improving Global Outcomes (KDIGO) CKD -M BD W ork Group. KD IG O clinical practice guideline for the diagnosis, evaluation, prevention, and treatment of chronic kidney disease-mineral and bone disorder (C K D -M BD ). K idney Int. 2009; 76 (suppl 113): S1-S130.
Kidney Disease: Improving Global Outcomes Lipid Guideline Development W ork Group Members. KD IG O Clinical Practice Guideline for Lipid Management in CKD : summary of recommendation statements and clinical approach to the patient. K idney Int Suppl. 2013; 3: 2 5 9-305.
Levey AS, et al. The definition, classification, and prognosis of chronic kidney disease: a KD IG O Controversies Conference report. K idney Int. 2011; 80: 7 -2 8 .
Levey AS, Coresh J. Chronic kidney disease. L ancet. 2012; 379: 165-180.
Levey AS, Inker LA, Coresh J. G FR estimation: from physiology to public health. A m J K idney Dis. 2014; 63: 82 0-834.
Macgregor M S, Methven S. Assessing kidney function. In: Daugirdas JT, ed. H an d book o f Chronic K idney Disease M anagem en t. Philadelphia, PA: Wolters Kluwer; 2011: 1-18.
National Kidney Foundation (N KF). K D O Q I clinical practice guidelines for bone metabolism and disease in chronic kidney disease. A m J K idney Dis. 2003; 42 (4 suppl 3): S1-S201.
Palmer SC, Strippoli GF. Proteinuria: does vitamin D treatment improve outcomes in CKD? N at Rev Nephrol.
2013; 9: 638-640. Ptinopoulou AG, Pikilidou M I, Lasaridis AN. The effect of antihypertensive drugs on chronic kidney disease: a comprehensive review. Hypertens Res. 2013; 36: 91-101.
Sharp Collaborative Group. Study of Heart and Renal Protection (SHARP): randomized trial to assess the effects of lowering low-density lipoprotein cholesterol among 9,438 patients with chronic kidney disease. A m H eart J . 2010; 160: 7 8 5-794.
Stone NJ, et al. 2013 ACC/AHA guideline on the treatment of blood cholesterol to reduce atherosclerotic cardiovascular risk in adults: a report of the Am erican College of Cardiology/American Heart Association Task Force on Practice Guidelines. C irculation. 2014; 129 (25 suppl 2): S1-S45.
