- Диализному врачу
- 1. Ведение пациентов с ХБП 4-5-й стадии.
- 2. Подготовка к трансплантации, диализу или к консервативной терапии
- 3. Физиологические принципы и моделирование кинетики мочевины
- 4. Оборудование для гемодиализа и расходные материалы
- 5. Вода для диализа и диализирующий раствор
- 6. Артериовенозные фистулы и протезы. Основные положения
- 7. Центральный венозный катетер в качестве доступа: основы
- 8. Мониторинг артериовенозного доступа и осложнений
- 9. Инфекции и другие осложнения центральных венозных катетеров
- 10. Назначение острого гемодиализа
- 11. Назначение хронического гемодиализа
- 12. Осложнения в ходе процедуры гемодиализа
- 13. Повторное использование диализаторов
- 14. Антикоагуляция
- 15. Продленная заместительная почечная терапия
- 16. Гемодиафильтрация
- 17. Терапевтический аферез
- 18. Актуальность сорбционных технологий сегодня
- 19. Руководство по диализу
Осложнения в ходе процедуры гемодиализа
Самыми распространенными осложнениями процедуры гемодиализа в порядке убывания их частоты являются: гипотензия, судороги, тошнота и рвота, головная боль, боль за грудиной, боль в спине и зуд.
I. ИНТРАДИАЛИЗНАЯ ГИПОТЕНЗИЯ. Интрадиализная гипотензия (ИДГ) - осложнение, требующее повышенного внимания. Это важно не только потому, что ИДГ может вызвать резкое ухудшение самочувствия пациента во время диализа, а еще и потому, что она связана с высокой летальностью (Flythe, 2014) и увеличением частоты локальных аномалий сокращения сердечной стенки, обозначаемых как «станнинг» или оглушение миокарда (McIntyre и Odudu, 2014). Существуют различные определения ИДГ, включая максимальное снижение систолического давления ниже 90 мм рт. ст., или снижение систолического давления на 20-30 мм рт. ст., или снижение АД на определенный процент от исходного (додиализного). Для целей оценки качества лечения определение ИДГ как снижение систолического давления ниже 90 мм рт. ст. может быть наиболее полезным, поскольку именно в этом случае имеется четкая связь с повышением летальности (Flythe, 2014). Чаще всего ИДГ встречается у пациентов с низким артериальным давлением перед сеансом диализа. Это может являться признаком функциональных или органических нарушений в сердце, из-за которых оно не способно обеспечить необходимую гемодинамику во время выведения из организма жидкости. ИДГ также увеличивает риск тромбоза сосудистого доступа (Chang, 2011). Причины, приводящие к возникновению ИДГ, представлены в табл. 12.1.
А. Гипотензия, связанная с изменением объема крови. Причины ИДГ, связанные с изменением объема крови, являются самыми важными. Во время диализа артериальное давление (АД) у пациента не снижается или снижается незначительно, если процедура не сопровождается выведением жидкости из организма - ультрафильтрацией (УФ). Таким образом, любые действия, направленные на снижение скорости УФ (увеличение общей продолжительности диализа за неделю, снижение потребления пациентом жидкости или увеличение объема выделяемой мочи), должны привести к снижению риска возникновения ИДГ.
1. Исключение больших междиализных прибавок веса. В контроле междиализной прибавки веса подчеркивается большая значимость ограничения потребления соли, чем ограничения потребления жидкости (Tomson, 2001). По имеющимся данным, существует четкая связь между повышенным употреблением натрия и неблагоприятными исходами на диализе (McCausland, 2012).
Таблица 12.1 Причины ИДГ

2. Увеличение общего недельного диализного времени. Увеличение недельной длительности диализа позволяет снизить объем необходимой УФ за единицу времени, что снижает риск развития ИДГ. Большой перерыв в процедурах диализа на выходные приводит к большей междиализной прибавке веса. Это значит, что с целью достижения оптимального постдиализного веса пациента необходимо соответственно увеличивать скорость УФ. В диализных центрах у пациентов с проблемами выведения жидкости зачастую применяют график диализа «пн-ср-пт-сб». Это позволяет сократить длинные выходные и увеличить недельное диализное время.
В руководстве KDOQI по адекватности диализа (2006) длительность процедур рекомендована не менее 3 часов при диализе 3 раза в неделю у пациентов с незначительным объемом мочи или при отсутствии диуреза независимо от достигнутого на процедуре показателя Kt/V. Европейские рекомендации по наилучшей клинической практике предписывают длительность процедуры не менее 4 часов для всех пациентов при диализе 3 раза в неделю независимо от их веса. Повышение частоты процедур без увеличения общего недельного времени диализа не всегда снижает риск возникновения ИДГ. Впрочем, в одном исследовании при переходе на короткий ежедневный диализ отмечено снижение проявлений оглушения миокарда (Jeffries, 2011).
3. Сохранение и увеличение суточного объема мочи. У пациентов с остаточной функцией почек и значительным количеством мочи требуется гораздо меньший объем УФ. Сохранить суточный объем мочи у пациентов можно с помощью приема диуретиков (Lemes, 2011).
4. Подбор целевого веса пациента. Целевой вес или «сухой» вес пациента подбирается на основании клинической картины: динамики артериального давления пациента, наличия отеков и индивидуальной переносимости определенной скорости УФ. Помочь врачу принять решение о целевом весе пациента могут дополнительные методы обследования (данные биоимпедансометрии, уровень предсердного натрийуретического фактора, мониторинг изменения объема крови в течение диализа, УЗИ легких). Термин «целевой вес» уместнее использовать вместо термина «сухой вес», потому что некоторым пациентам необходимо сохранить небольшой излишек жидкости в организме для предотвращения гипотензии и других неприятных симптомов. Особенно это касается пациентов с потребностью удаления большого объема жидкости за процедуру. В процессе УФ вес пациента начинает приближаться к «сухому», и скорость поступления жидкости из тканей в сосудистое русло прогрессивно снижается. В результате к концу процедуры возникает гиповолемия, проявляющаяся гипотензией, судорогами, головокружением, а после диализа - слабостью и недомоганием. Большую угрозу может нести в себе нарушение кровоснабжения сердца, мозга и кишечника, приводящие к кумулятивным неблагоприятным последствиям. По этой причине пациенты, которым требуются большие объемы УФ, могут не достигать своего фактического «сухого веса».
Мониторинг гематокрита во время диализа помогает распознать завышенный «сухой вес». Если, несмотря на выведение жидкости, график гематокрита выглядит в виде прямой линии (нет роста на протяжении диализа), это указывает на быстрое перемещение жидкости из тканей в сосудистое русло и свидетельствует о гипергидратации. Однако в одном из рандомизированных исследований, использование такого мониторинга в клинической практике привело, как ни странно, не к снижению, а к увеличению случаев госпитализации (Reddan, 2005). Определение критического уровня гемоконцентрации (crash-crit) не показало особой практической значимости для предотвращения ИДЕ
В настоящее время более популярным становится использование метода многочастотного биоимпеданса для корректировки целевого постдиализного веса пациента. Снижение гипергидратации ведет к уменьшению распространенности гипертрофии миокарда левого желудочка как фактора неблагоприятного прогноза. Попытки агрессивного снижения артериального давления без использования инструментальных методов могут привести к увеличению распространенности ИДГ (Davenport, 2008), а также частым дисфункциям сосудистого доступа и повышению частоты госпитализаций, связанной с сердечно-сосудистыми осложнениями (Curatola, 2011). Использование же монитора многочастотного биоимпеданса сопровождается снижением артериального давления и уменьшением массы миокарда левого желудочка (Hur, 2013) без выраженных побочных эффектов, хотя уменьшение суточного объема мочи происходит быстрее у пациентов, у которых для коррекции целевого постдиализного веса используют биоимпеданс.
5. Использование оптимальной концентрации натрия в диализирующем растворе. Когда концентрация натрия в диализирующем растворе ниже его уровня в плазме крови, то кровь, проходящая через диализатор, тоже становится гипотонич-ной относительно жидкости в тканях тела. Для поддержания осмотического равновесия жидкость переходит из крови в ткани, вызывая резкое уменьшение объема циркулирующей крови. Повышенное же содержание натрия в диализирующем растворе ограничивает уменьшение объема крови, сопровождающее УФ, однако, с другой стороны, приводит к постдиализной жажде, значительной междиализной прибавке веса, высокому артериальному давлению.
Широко практикуется так называемое профилирование натрия (или диализ с градиентом натрия). Оно заключается в повышении концентраций натрия (145-155 ммоль) в диализирующем растворе в начале процедуры с последующим снижением (линейным, пошаговым или логарифмическим) его до уровня 135-140 ммоль к концу диализа. Целью является использование преимуществ раствора с повышенным содержанием натрия без негативных последствий. Однако опубликованные в литературе данные на эту тему не подтверждают значимых преимуществ профилирования натрия (Stiller, 2001). Следует также отметить, что постдиализный уровень натрия в плазме зависит не от конечной, а от средневременной концентрации его в диализирующем растворе на протяжении всей процедуры.
Вместо использования диализирующего раствора с какой-то одной для всех концентрацией натрия по принципу «один размер подходит всем» переход к «индивидуализации» раствора с содержанием натрия, близким к его преддиализному уровню каждого пациента, может уменьшить вышеуказанные симптомы, в том числе и постдиализную жажду (Santos, 2010). Результаты последних исследований показали, что применение диализирующих растворов с повышенным уровнем натрия (>142 ммоль/л) может быть целесообразно для ослабленных пациентов с повышенным риском развития ИДГ, потому что ее последствия гораздо опаснее последствий повышенного содержания натрия в диализирующем растворе (Marshall и Dunlop, 2012). Применение же растворов с пониженным содержанием натрия может уменьшить риск ИДГ за счет снижения междиализной прибавки веса и избавления от необходимости большого объема УФ за процедуру (Shah и Davenport, 2012).
6. Контроль объема крови по принципу обратной связи. В течение нескольких лет используется аппаратура с программным обеспечением, основанным на мониторинге изменения объема крови в процессе диализа, позволяющая контролировать скорость УФ по принципу обратной связи. Результаты нескольких рандомизированных исследований говорят о том, что использование такого контроля снижает вероятность возникновения ИДГ, исключая положительный баланс натрия (Davenport, 2011).
В. Гипотензия вследствие нарушения вазоконстрикции. В условии гиповолемии сердечный выброс ограничен наполнением сердца; снижение либо периферического сосудистого сопротивления (ПСС), либо сердечного наполнения приводит к гипотензии. В условиях снижения наполнения сердца рефлекторное учащение сердечных сокращений оказывает слабое влияние на сердечный выброс. Учитывая, что 80% общего объема крови циркулирует в венозной части сосудистого русла, изменение венозной емкости может серьезно изменить эффективный объем циркулирующей крови и заполнение левого желудочка. Когда сопротивление в артериолах снижено, артериальное давление сильнее воздействует на венозное русло, вызывая пассивное растяжение вен с секвестрацией и депонированием крови. Не значимый при использовании вазодилататоров в условиях эуволемии (т. к. заполнение левого желудочка более чем адекватно) (Daugirdas, 1991), при гиповолемии этот механизм не обеспечивает адекватного возврата крови к сердцу и приводит к гипотензии. Степень сужения артериол или общего периферического сосудистого сопротивления (ОПСС) также играет важную роль, поскольку ОПСС будет определять кровяное давление при любом сердечном выбросе.
1. Понижение температуры диализирующего раствора. В идеале температура диализирующего раствора должна поддерживать температуру артериальной крови пациента на исходном уровне в течение всей процедуры. Когда температура выше оптимальной, происходит кожная вазодилатация, чтобы обеспечить теплоотдачу. Расширение сосудов уменьшает их сопротивление и увеличивает риск гипотензии. Для диализных аппаратов доступны опции модуля температуры крови, обеспечивающие эутермический диализ. Без таких устройств выбор температуры диализирующего раствора проблематичен, поскольку даже небольшая разница с температурой крови (1,1 °C) может значительно повлиять на артериальное давление пациента (Sherman, 1984). Наиболее часто используемая температура диализирующего раствора в 37 °C практически всегда превышает эутермическую. Изначально лучше использовать температуру диализирующего раствора 35,5-36,0 °C, увеличивая или снижая ее в процессе диализа, в зависимости от переносимости пациентом (озноб) и эффективности (артериальное давление). Низкая температура вызывает дискомфорт у пациента только когда она ниже оптимальной (как правило, неизвестной). Эутермический диализ протекает без дрожи и крайне редко с ознобом (Maggiore, 2002). В одной из групп устанавливалась индивидуальная температура диализирующего раствора, на 0,5 °C ниже температуры барабанной перепонки пациента. Этот метод позволил избежать появления у пациентов чувства холода и озноба, которые обычно наблюдаются при использовании одинакового для всех охлажденного диализирующего раствора (Odudu, 2012). Кроме того, индивидуальная температура охлажденной диализирующей жидкости приводит к уменьшению времени постдиализного восстановления пациента, улучшает контроль за уровнем артериального давления, снижает риск сердечно-сосудистого стресса и прогрессирующего ишемического поражения белого вещества мозга (McIntyre, 2014).
В ряде исследований использование гемодиафильтрации было связано с лучшей переносимостью УФ и меньшей частотой ИДГ в сравнении с гемодиализом. Однако велика вероятность, что преимущества гемодиафильтрации обусловлены прежде всего более низкой температурой в экстракорпоральном контуре из-за охлаждающего эффекта замещающего раствора. Когда же теплообмен в экстракорпоральном контуре во время диализа постоянно контролируется, преимуществ гемодиафильтрации над гемодиализом в отношении контроля артериального давления не наблюдается (Kumar, 2013).
2. Исключение приема пищи во время диализа пациентами, склонными к гипотензии.
Прием пищи во время диализа может ускорить или усугубить гипотензию (Sherman, 1988; Strong, 2001). Это связано с расширением сосудов брюшной полости, изменением сосудистого сопротивления и перераспределением крови за счет кровенаполнения внутренних органов (Barakat, 1993). Гипотензивный эффект от приема пищи длится не менее 2 часов. Поэтому пациенты, склонные к ИДГ, должны избегать приема пищи во время диализа или непосредственно перед процедурой.
3. Минимизация ишемии тканей во время диализа. Во время любого гипотензивного стресса происходит ишемия тканей с выделением аденозина, который блокирует высвобождение норадреналина из симпатических нервных окончаний, а также обладает собственным вазодилатирующим действием. Тяжелая гипотензия может усугубить себя сама: гипотензия -> ишемия -> выброс аденозина -> подавление высвобождения норадреналина -> вазодилатация -> гипотензия.
Это объясняет, почему пациенты с низким гематокритом (например, <20-25%) наиболее подвержены гипотензии во время диализа (Sherman, 1986). В настоящее время немногие имеют такую тяжелую анемию, которая может привести к возникновению гипотензии. Таким пациентам может быть полезна гемотрансфузия, хотя в настоящее время имеется тенденция к воздержанию от нее у тяжелобольных в отделениях интенсивной терапии. Использование назальной оксигенации у пациентов, склонных к гипотензии, может быть еще одним способом минимизации ишемии тканей и снижения риска ИДГ (Jhawar, 2011).
4. Мидодрин. Мидодрин, а-адренергический агонист, при пероральном приеме снижает частоту появления ИДГ. Обычно применяется доза 10 мг за 1,5— 2 часа до диализа, хотя есть сведения о применении больших доз (до 40 мг). Фактором, ограничивающим его применение и дозы, является повышение артериального давления в положении лежа. Применение мидодрина противопоказано пациентам с активными формами ишемической болезни сердца (а не просто с бессимптомным коронарным атеросклерозом). Одновременное применение а-адреноблокаторов с мидодрином нивелирует его эффект. Нет данных об эффективности мидодрина при автономной полинейропатии, которая имеется у половины диализных пациентов. Проблема приема мидодрина еще и в том, что его действие не превышает эффект от применения охлажденного диализата и не является аддитивным (Cruz, 1999).
5. Сертралин. По крайней мере, 3 исследования показали, что терапия в течение 4-6 недель селективным ингибитором обратного захвата серотонина, сертралином, снижает частоту появления ИДГ. Существуют доказательства, что он улучшает работу вегетативной нервной системы (Yalcin, 2003). Подобно мидодрину сертралин не показал дополнительную пользу при гипотензии в сравнении с использованием охлажденного диализата (Brewster, 2003).
6. Применение антигипертензивных препаратов. Антигипертензивные препараты, принятые пациентом перед диализом, могут отрицательно повлиять на адаптацию сердечно-сосудистой системы к выведению жидкости из организма во время процедуры. Недостаточно изучено, являются ли сосудорасширяющие препараты более проблемными по сравнению с имеющими другие механизмы действия.
7. Концентрация калия в диализирующем растворе. Низкое содержание калия в диализирующем растворе (1 ммоль/л) чаще всего связано с возникновением ИДГ, возможно за счет вегетативных эффектов. С целью улучшения гемодинамики и снижения риска аритмий рекомендуется использование растворов с повышенным содержанием калия.
8. Флудрокортизон. В предварительном сообщении (Landry, 2011) прозвучало, что в группе из пяти диализных пациентов с пониженным преддиализным артериальным давлением и устойчивой интрадиализной гипотензией выявлен низкий уровень альдостерона (проба бралась в произвольное время). У всех пациентов был нормальный результат теста с козинтропином. Артериальное давление нормализовалось после лечения флудрокортизоном, объемы УФ увеличились, а случаи ИДГ сократились. Снижения эпизодов ИДГ при применении флудрокортизона у пациентов с нормальным уровнем гормонов надпочечников не наблюдалось.
9. Вазопрессин. В норме при гипотензии уровень вазопрессина в организме повышается, однако у диализных пациентов это повышение оказывается недостаточным. Вазопрессин прежде всего сужает сосуды брюшной полости, что способствует централизации кровообращения во время выведения жидкости из организма В одном из исследований инфузии вазопрессина помогали предотвратить ИДГ (van der Zee, 2007).
C. Гипотензия, вызванная кардиальными факторами
1. Диастолическая дисфункция. В трудно растяжимом гипертрофированном сердце снижение сердечного выброса происходит даже при малейшем падении давления наполнения сердца. Диастолическая дисфункция у диализных пациентов обусловлена гипертензией, ишемической болезнью сердца и самой уремией. Некоторые ограниченные данные свидетельствуют о том, что применение верапамила в качестве антигипертензивного средства может уменьшить частоту возникновения ИДГ у таких пациентов.
2. Сердечный ритм и сократительная способность сердца. Большинство, но не все случаи гипотензии на диализе связаны со снижением наполнения сердца, когда компенсаторные механизмы могут лишь незначительно повлиять на увеличение сердечного выброса. У некоторых пациентов ОПСС может уменьшаться (из-за влияния температуры раствора, употребления пищи или тканевой ишемии) и без уменьшения заполнения левого желудочка. В этом случае нарушение работы компенсаторных механизмов сердца может напрямую влиять на развитие гипотензии.
3. Концентрация кальция в диализирующем растворе. Диализирующий раствор с содержанием кальция 1,75 ммоль повышает сократимость миокарда и помогает лучше контролировать артериальное давление во время диализа, чем раствор с концентрацией кальция 1,25 ммоль, особенно у пациентов с заболеваниями сердца (van der Sande, 1998). Тем не менее в условиях хронического амбулаторного лечения (в отличие от отделений интенсивной терапии) даже при применении диализных растворов с повышенным содержанием кальция симптоматическая гипотензия у пациентов случается не реже (Sherman, 1986). Однако использование растворов с высокой концентрацией кальция может способствовать кальцификации сосудов, поэтому сохраняется тенденция их непродолжительного использования. Уровень концентрации магния в диализирующем растворе может влиять на возникновение гипотензии во время диализа, однако вопрос, какой уровень магния лучше использовать - пониженный или повышенный, - остается открытым (см. главу 10).
D. Необычные причины гипотензии во время диализа. В редких случаях гипотензия может быть проявлением другого серьезного основного заболевания (см. табл. 12.1).
E. Выявление гипотензии. Во время гипотензии большинство пациентов жалуются на головокружение, слабость, спутанное сознание и тошноту. Некоторые испытывают мышечные судороги. У других же проявления гипотензии очень слабые и могут быть замечены только медперсоналом, которому известны особенности данного пациента (например, замедленная реакция или потемнение в глазах); однако чаще всего пациенты сами хорошо знакомы с признаками ИДГ. Есть и пациенты, у которых характерные симптомы не появляются до тех пор, пока артериальное давление не упадет до экстремально низких значений. Исходя из этого, артериальное давление пациентам на диализе необходимо измерять регулярно. Интервалы между измерениями должны определяться индивидуальными особенностями гемодинамики каждого пациента.
F. Контроль гипотензии на диализе. Взять контроль над ситуацией при остро возникшем эпизоде гипотензии достаточно просто. Пациент незамедлительно должен быть переведен в положение Тренделенбурга (если позволяет его респираторный статус) и через магистраль крови необходимо быстро выполнить болюсное введение 0,9% раствора хлорида натрия (100 мл или более, по необходимости). Скорость УФ при этом следует снизить до минимума, лучше до нуля. Далее необходимо обеспечить тщательное наблюдение. После стабилизации жизненно важных функций ультрафильтрацию можно постепенно возобновить (с небольшой скорости). В качестве альтернативы физиологическому раствору при гипотензии можно использовать растворы глюкозы, маннитола или альбумина. Раствор альбумина более дорогостоящий и в данной ситуации не эффективнее других препаратов (Knoll, 2004); маннитол же имеет свойство накапливаться в организме, отчего снижается эффективность его последующего введения. Коррекция ИДГ происходит лучше при быстром введении гипертонического раствора хлорида натрия (в течение 2 минут), чем при более медленном введении (в течение 5 минут) эквивалентной дозы натрия в физрастворе. Эти различия обусловлены тем, что стимуляция секреции вазопрессина происходит при повышении осмотического давления крови (Shimizu, 2012). Однако следует соблюдать осторожность при использовании диализирующих растворов с повышенным содержанием натрия. Назальное введение кислорода может оказать дополнительный положительный эффект в процессе купирования гипотензии у некоторых пациентов (Jhawar, 2011).
1. Снижение скорости потока крови. Снижение скорости потока крови во время эпизода ИДГ применялось во времена плоскопараллельных диализаторов и ацетатных диализирующих растворов, когда не было системы точного контроля УФ. Эта методика приводила к уменьшению: а) объема крови в диализаторе, б) поступления ацетата (вазодилататора) в организм пациента, в) скорости УФ, г) проявления синдрома «обкрадывания». Последний пункт предполагал, что уменьшение скорости потока крови по контуру, снижающее поток крови через сосудистый доступ, приводит к увеличению системного кровотока. Это утверждение, вероятнее всего, ошибочно, за исключением ситуации, когда имеется стеноз сосудистого доступа (Trivedi, 2005). Таким образом, в настоящее время снижение скорости потока крови с целью уменьшения риска ИДГ считается бесполезным. Однако при тяжелой гипотензии, когда нет должного эффекта от остановки УФ и мероприятий по восстановлению объема, скорость насоса крови может быть временно снижена. Повторные снижения скорости кровотока в течение процедуры могут привести к недодиализу.
G. Профилактика гипотензии. Мероприятия, помогающие предотвратить интрадиализную гипотензию, приведены в табл. 12.2
Таблица 12.2 Мероприятия по предотвращению гипотензии во время сеанса диализа

II. МЫШЕЧНЫЕ СУДОРОГИ
А. Этиология. Патогенез мышечных судорог во время диализа неизвестен. Четыре наиболее важных фактора, предрасполагающих к их появлению: гипотензия, гиповолемия (пациенты с весом ниже «сухого»), высокая скорость УФ (при большой междиализной прибавке веса) и использование диализирующих растворов с пониженным содержанием натрия. Все эти факторы приводят к вазоконстрикции с последующей гипоперфузией мышечной ткани и вторичному нарушению расслабления мышц. Чаще всего мышечные судороги сопровождают гипотензию, хотя могут не прекращаться и после восстановления артериального давления. Частота возникновения судорог увеличивается в логарифмической зависимости от снижения веса на процедуре. Так, при снижении веса на 2, 4 или 6% возникновение судорог регистрируется в 2, 26 и 49% случаев соответственно.
Судороги чаще возникают в первый месяц диализа, чем в последующие периоды, чаще встречаются у пациентов с низким сердечным выбросом. Необъяснимое повышение уровня креатининфосфокиназы в плановых анализах крови может быть следствием мышечных судорог во время диализа. Гипомаг-неземия может быть также причиной их возникновения. Гипокальциемия тоже должна рассматриваться в качестве потенциальной причины судорог, особенно при использовании диализирующего раствора с относительно низким содержанием кальция (1,25 ммоль), а также при приеме фосфатсвязывающих препаратов и/или цинакальцета. Спровоцировать судороги на диализе может и гипокалиемия, которая усугубляется использованием диализирующих растворов с концентрацией калия 2 ммоль/л.
B. Лечение. Если гипотензия и мышечные судороги появляются одновременно, может помочь введение физиологического раствора; однако нередко судороги повторяются. Гипертонические растворы (хлорида натрия, глюкозы, ман-нитола) расширяют кровеносные сосуды мышц и достаточно эффективны в качестве средства неотложной помощи при мышечных судорогах. Поскольку гипертонический раствор хлорида натрия содержит большую концентрацию натрия, то его широкое применение проблематично. Поэтому для купирования мышечных судорог у пациентов без диабета предпочтительнее использовать гипертонический раствор глюкозы (Sherman, 1982). У диализных пациентов раствор маннитола может накапливаться в организме и быть неэффективным, особенно если применяется в конце процедуры - тогда, когда появление судорог наиболее вероятно. Нифедипин (10 мг) иногда помогает остановить судороги. Хотя нет данных, что он вызывает значимое снижение артериального давления, его следует применять только у пациентов со стабильной гемодинамикой. Также принести облегчение пациентам, испытывающим судороги, может принудительное растяжение мышц (например, голеностопное сгибание при судороге икроножной мышцы). В индивидуальном порядке можно применить массаж.
C. Профилактика. Предотвращение эпизодов гипотензии в большинстве случаев предупреждает и появление судорог.
1. Упражнения на растяжение мышц. Комплексы упражнений для подверженных судорогам групп мышц могут быть полезны и должны быть терапией выбора при диализных и ночных судорогах (Evans, 2013).
2. Уровень натрия в диализирующем растворе. Частота появления судорог во время диализа обратно пропорциональна содержанию натрия в диализирующем растворе. Поэтому повышение концентрации натрия чуть ниже порога постдиализной жажды может оказаться весьма полезным, а использование диализа с профилированием (градиентом) натрия значительно снижает вероятность появления судорог, но способствует большой междиализной прибавке веса и повышению артериального давления.
3. Уровень магния в диализирующем растворе. Для предотвращения судорог следует избегать пониженных преддиализных уровней магния, кальция и калия в крови. В одном из исследований использование раствора с концентрацией магния 0,5 ммоль (1 мЭкв/л) привело к меньшему числу случаев судорог по сравнению с использованием раствора, содержащего 0,375 ммоль (0,75 мЭкв/л) магния (Mowa, 2011). Препараты магния неэффективны у пациентов без уремии, и диализным пациентам такие препараты следует назначать с большой осторожностью. Так, применение осварена (ацетат кальция + карбонат магния) в качестве фосфатсвязывающего препарата по сравнению с севеламером не привело к изменению частоты судорог.
4. Биотин. Биотин в дозе 1 мг в день положительно зарекомендовал себя в качестве средства, контролирующего судороги во время диализа, несмотря на то что уровень биотина в плазме у диализных пациентов был выше такового у пациентов контрольной группы (Oguma, 2012). Данные этого исследования необходимо подтвердить, прежде чем рекомендовать биотин для широкого использования.
5. Применение карнитина, оксазепама и витамина Е. Дополнительный прием карнитина может уменьшить судороги у диализных пациентов во время процедуры (Ahmad, 1990), так же как и применение оксазепама (5-10 мг за 2 часа до процедуры) и витамина Е (см. обзор Evans, 2013).
6. Компрессионные устройства. Положительный эффект можно получить и от применения приспособлений с режимом последовательной компрессии (Ahsan, 2004).
7. Применение хинина. Применение хинина сульфата перед диализом, несмотря на свою эффективность для профилактики судорог, не рекомендуется, потому что с его использованием связано возникновение тромбоцитопении, гиперчувствительности и удлинения интервала QT. В соответствии с рядом указаний FDA (США) следует отказаться от применения хинина в качестве средства против судорог нижних конечностей.
III. ТОШНОТА И РВОТА
A. Этиология. Тошнота и рвота возникают в 10% случаев рутинного диализного лечения. Многие факторы могут быть тому причиной. Большинство эпизодов у стабильных пациентов связано с гипотензией. Также тошнота и рвота могут быть ранними проявлениями дизэквилибриум-синдрома и обоих типов (А и В) реакций на диализатор. Гастропарез, чаще всего встречающийся у больных сахарным диабетом, в процессе диализа усиливается и может стать причиной тошноты и рвоты у некоторых пациентов. Кроме того, подобные проявления могут быть результатом использования недостаточно чистого диализирующего раствора или раствора с нарушенными пропорциями электролитов (высокое содержание натрия и кальция). Диализные пациенты больше подвержены тошноте и рвоте, чем другие пациенты (с инфекциями верхних дыхательных путей; наркоманы; страдающие гиперкальциемией); процедура диализа предрасполагает и усиливает эти симптомы.
B. Лечение. В первую очередь необходимо принять меры по выявлению и устранению гипотензии, поскольку если у пациента имеет место вызванная гипотензией спутанность сознания, то рвота может быть опасна из-за риска аспирации рвотными массами. В случае возникновения рвоты по другим причинам можно использовать противорвотные средства.
C. Профилактика. Чтобы избежать тошноты и рвоты во время диализа, необходимо принять меры по снижению риска ИДГ. При часто повторяющихся симптомах, не связанных с нарушением гемодинамики, можно использовать 5-10 мг метоклопрамида перед процедурой.
IV. ГОЛОВНАЯ БОЛЬ
A. Этиология. Головная боль во время диализа возникает примерно у 70% пациентов, в большинстве случаев - по непонятным причинам. Иногда ее появление может быть проявлением дизэквилибриум-синдрома (см. раздел VII далее). У пациентов, употребляющих кофе, головная боль может быть вызвана снижением концентрации кофеина в процессе диализа. Кроме того, если пациент страдает от мигрени, то диализ может спровоцировать приступ. В случае возникновения необычной или очень интенсивной головной боли у пациента следует думать о неврологических причинах (особенно о кровоизлиянии в мозг на фоне применения антикоагулянтов).
B. Лечение. Во время диализа пациенту можно дать обезболивающий препарат на основе парацетамола (ацетаминофена).
С. Профилактика. Для профилактики головной боли во время диализа может оказаться полезным снижение уровня натрия в диализирующем растворе, если используется раствор с повышенным его содержанием. Чашка крепкого кофе может помочь предотвратить (или купировать) симптомы, связанные с выведением кофеина из организма на диализе. Если пациент испытывает частые мучительные головные боли во время процедуры, можно предположить дефицит магния в организме (Goksel, 2006). В таком случае имеет смысл назначить препарат магния, не забывая о рисках, связанных с приемом таких препаратов пациентами с почечной недостаточностью.
V. БОЛЬ В ГРУДИ И СПИНЕ. Умеренная боль в груди или дискомфорт за грудиной (часто ассоциируемые с болью в спине) наблюдаются в 1-4% случаев диализного лечения. Причина их неизвестна. Для профилактики и лечения не выработано определенной тактики, но переход на другой тип мембраны диализатора бывает полезен. Приступы стенокардии на диализе должны подвергаться дифференциальной диагностике с другими возможными причинами боли за грудиной (гемолиз, воздушная эмболия, перикардит). Профилактика и купирование стенокардии обсуждаются в главе 38.
VI. ЗУД. Зуд - нередкая проблема у диализных пациентов, часто возникает и усугубляется на диализе. В случае когда зуд беспокоит пациента только во время процедуры, особенно если имеют место некоторые аллергические проявления, он может быть признаком реакции гиперчувствительности на диализатор или компоненты экстракорпорального контура. Однако чаще всего зуд является хроническим, просто более заметен во время процедуры из-за длительного ограничения движения пациента. В качестве потенциальных причин зуда не следует упускать из виду вирусный (или лекарственный) гепатит и чесотку.
При хроническом зуде в качестве первого средства необходимо смазывать кожу увлажняющими и смягчающими средствами. Далее следует убедиться, что доза проводимого диализа адекватна, а уровень Kt/V не менее 1,2, хотя доказательств, что повышение Kt/V уменьшает зуд, недостаточно. Зуд часто встречается у пациентов с повышенными уровнями кальция и фосфора и/или значительно повышенном уровне ПТГ; показано снижение фосфора, кальция (до нижнего предела нормальных значений) и уровня ПТГ.
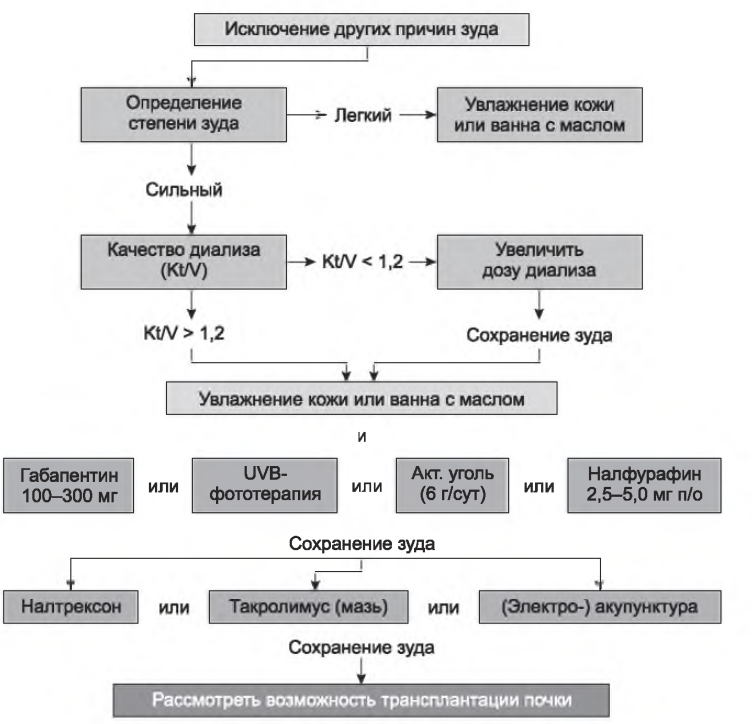
Эффективно и стандартное симптоматическое лечение антигистаминными препаратами. Следующий шаг - лечение габапентином (прегабалином), ультрафиолетовым В-излучением, прием внутрь активированного угля или нальфурафи-на. В крайнем случае могут быть использованы налтрексон и такролимус (мазь) -см. рис. 12.1 (Mettang and Kremer, 2014).
VII. ДИЗЭКВИЛИБРИУМ-СИНДРОМ
A. Определение. Дизэквилибриум-синдром - это сочетание системных и неврологических симптомов, часто характеризующееся определенными изменениями на электроэнцефалограмме, возникающими во время или после диализа. Ранними и легкими проявлениями являются тошнота, рвота, беспокойство и головная боль. В более серьезных случаях могут случиться системные судороги, нарушение сознания и кома (см. также главу 40).
B. Этиология. О причинах дизэквилибриум-синдрома ведутся споры. Большинство считают, что в процессе диализа концентрация растворенных в плазме веществ уменьшается, плазма становится гипотоничной по отношению к клеткам мозга, и вода перемещается из плазмы в ткани мозга. Другие думают, что причиной синдрома нарушения равновесия является резкое изменение уровня pH спинномозговой жидкости во время диализа.
РИСУНОК 12.1. Алгоритм лечения зуда. UVB - ультрафиолет В. Воспроизведено с разрешения из Mettang Т, Kremer АЕ. Uremic pruritus. Kidney Int. 2014
Дизэквилибриум-синдром был большой проблемой несколько десятилетий назад, когда пациенты с очень высокими уровнями мочевины крови, как правило, сразу подвергались длительному диализу. Однако этот синдром в легкой форме все еще встречается у пациентов, долго находящихся на хроническом диализе, и проявляется в виде тошноты, рвоты или головной боли. Развернутая картина дизэквилибриум-синдрома, в том числе судороги и кома, все еще может встретиться, если пациенту с высоким уровнем уремических токсинов в крови провести слишком интенсивный диализ.
С. Лечение
1. Легкое проявление дизэквилибриум-синдрома. Такие симптомы, как тошнота, рвота, беспокойство и головная боль, являются неспецифическими. Когда они появляются, трудно быть уверенным, что они обусловлены дизэквилибри-ум-синдромом. Лечение симптоматическое. Если же такие симптомы возникают во время диализа у пациента с уремией при остром почечном повреждении, необходимо уменьшить скорость потока крови для снижения эффективности удаления растворенных в крови веществ и изменения уровня pH, а также можно сократить время процедуры. В случае появления судорог можно применить гипертонический раствор хлорида натрия или глюкозы.
2. Тяжелый диээквилибриум-синдром. Если во время процедуры диализа у пациента внезапно развиваются судорожные припадки, нарушения сознания или наступает кома, процедуру следует прекратить и провести дифференциальную диагностику дизэквилибриум-синдрома (см. главу 40). Купирование судорог также рассматривается в главе 40. При коме необходимо поддерживать жизненные функции пациента: контролировать проходимость дыхательных путей, и если необходимо, приступить к искусственной вентиляции легких. Может принести пользу внутривенное введение маннитола. Если кома -следствие дизэквилибриум-синдрома, то улучшение состояния пациента наступит уже в течение суток.
D. Профилактика дизэквилибриум-синдрома
1. При проведении экстренного диализа. При проведении лечения пациенту с острой уремией следует избегать агрессивного диализа (см. главу 10). На начальном этапе достаточно снижения уровня азота мочевины крови на 40% от исходного. Использовать диализирующие растворы с пониженным содержанием натрия (более чем на 2-3 ммоль ниже, чем уровень натрия в плазме) не стоит, так как они могут усугубить отек мозга. У пациентов с гипернатриемией также не следует одновременно корригировать уровень натрия в плазме и уремию. Надежнее всего использовать в начале процедуры диализирующий раствор с концентрацией натрия, близкой к уровню в плазме пациента, а затем корригировать гипернатриемию медленно, применяя медленное постдиализное введение 5% раствора глюкозы.
2. При проведении хронического диализа. Частоту возникновения дизэквилибриум-синдрома можно свести к минимуму путем использования диализирующего раствора с концентрацией натрия не менее 140 ммоль. Такой же результат был достигнут при применении диализата с концентрацией глюкозы 11 ммоль/л вместо 5,5 ммоль/л (Raimann, 2012). Предлагали использование диализирующих растворов с повышенным содержанием натрия (145— 150 ммоль) в начале, с постепенным уменьшением его в процессе диализа. Первоначально высокий уровень натрия в растворе приводит к его повышению в плазме, что поддерживает осмотическое давление, снижающееся от быстрого падения концентрации мочевины и других растворенных в крови веществ в начале процедуры. Имеются доказательства, что такой подход уменьшает вероятность дизэквилибриум-синдрома, но может способствовать значительной междиализной прибавке веса и повышению артериального давления по причине диффузионного перехода натрия из диализирующего раствора в кровь.
VIII. РЕАКЦИИ НА ДИАЛИЗАТОР. Это группа широкого спектра реакций - как анафилактических, так и менее определенных, причина которых неизвестна (Jaber and Pereira, 1997). В прошлом многие из этих реакций объединялись термином «синдром первого использования», потому что они проявлялись гораздо чаще при использовании нового диализатора в сравнении с повторным использованием (реюзом). Однако похожие реакции были и при повторном использовании диализаторов, поэтому теперь мы их обсуждаем как обобщенные. Как упоминалось ранее, реакции на диализатор подразделяются на две основные группы: анафилактические (тип А) и неспецифические (тип В). В течение нескольких последних десятилетий количество реакций типа В значительно уменьшилось.
А. Реакции типа А (анафилактические)
1. Проявления. При классической тяжелой реакции появляется клиническая картина анафилаксии. Это общие симптомы - одышка, тревога, паника, чувство жара в области сосудистого доступа или во всем теле, - которые могут закончиться остановкой сердца и смертью. В более легких случаях появляются лишь кожный зуд, сыпь, кашель, чихание, насморк или слезотечение. Могут присоединиться реакции со стороны желудочно-кишечного тракта - спазмы в животе и диарея. Пациенты с атопией и эозинофилией в анамнезе предрасположены к появлению этих реакций. Симптомы обычно начинаются в первые минуты диализа, но иногда их появление может быть отсрочено до получаса и более от начала процедуры.
2. Этиология
a. Окись этилена. Большинство реакций типа А (анафилактические) раньше были проявлением гиперчувствительности пациента на окись этилена, широко используемого производителями в процессе стерилизации диализаторов. Окись этилена задерживается в компаунде - торцевой заливке, удерживающей полые волокна диализатора, и трудно удаляется методом дегазации. Реакции типа А наблюдались исключительно при первом использовании таких диализаторов. Сейчас производители используют различные методы стерилизации (гамма-излучение, электронно-лучевая и паровая стерилизация), и даже если применяется окись этилена, в диализаторах присутствуют лишь его незначительные остатки. В результате в настоящее время реакции на окись этилена - большая редкость.
b. АМ69-ассоциированные реакции. Впервые описаны у пациентов, принимающих ингибиторы ангиотензин-превращающего фермента (иАПФ), диализирующихся с использованием мембран AN69 (сополимера акрилонитрила и натрия металил-сульфоната). Считается, что реакции организма связаны с изменениями в брадикининовой системе. Так, отрицательно заряженная АП69-мембрана активирует систему брадикинина, эффект усиливается действием иАПФ, потому что они блокируют инактивацию брадикинина. Изначально повышенный уровень брадикинина при использовании на диализе АП69-мембран, значительно увеличивается при развитии реакций. Этот эффект менее выражен при применении блокаторов рецепторов ангиотензина вместо иАПФ (Ball, 2003). Пока не ясно, насколько выражены реакции организма при использовании других ПАН (полиакрилонитрильных) мембран или не-ПАН-мембран в присутствии иАПФ.
c. Недоочищенный диализирующий раствор. Реакции типа А могут возникать в случае проведения процедуры с диализирующим раствором, содержащим большое количество бактерий и эндотоксинов, особенно при применении высокопроницаемых (high-flux) диализаторов. Эти реакции развиваются быстро, в течение первых 2 минут от начала диализа, тогда как реакции системы комплемента начинаются позже, примерно через 15-30 минут. Самые распространенные проявления данного типа реакций - лихорадка и озноб. Риск их появления возрастает пропорционально содержанию в диализирующем растворе бактерий и эндотоксина.
d. Реюз (повторное использование диализаторов). Целый ряд реакций анафилактического типа происходили в результате повторного использования диализаторов. Проблема чаще всего была связана с неадекватной дезинфекцией диализатора перед процедурой, но во многих случаях причины остались неизвестными. Половина случаев бактериемии и пирогенных реакций на диализе, расследованных центрами по контролю и профилактике заболеваний США (CDC8) в течение 20 лет, связывают именно с повторным использованием диализаторов (Roth and Jarvis, 2000).
e. Гепарин. Иногда на гепарин у пациентов появляются аллергические реакции, такие как кожный зуд, заложенность носа, свистящие хрипы при дыхании и даже анафилаксия. Если у пациента подозревается реакция на разные типы диализаторов, независимо от способа их стерилизации, а реакция на диализирующий раствор исключена, то следует рассмотреть возможность пробного безгепаринового диализа или использования цитратного антикоагулянта. В случае выявления у пациента реакции на гепарин заменять его низкомолекулярным гепарином опасно из-за перекрестной аллергии.
f. Активация системы комплемента. Резкое повышение давления в легочной артерии было зафиксировано у животных и человека во время диализа с применением мембраны из незамещенной целлюлозы. Однако нет доказательств, что именно активация системы комплемента вызывает анафилаксию. Несколько проведенных исследований не выявили различий в частоте возникновения реакций типа А при использовании мембран, легко вызывающих активацию системы комплемента (купрофан) и мембран, не вызывающих такой активации (полисульфоновых, AN69).
д. Эозинофилия. Реакции типа А обычно возникают у пациентов с легкой или средней степенью эозинофилии. Тяжелые реакции на диализ или плазмаферез наблюдаются у пациентов с очень высоким уровнем эозинофилов. Считается, что это обусловлено внезапной дегрануляцией эозинофилов с высвобождением бронхоспастических и других медиаторов.
3. Лечение. Выявление истинной причины реакции организма на диализатор зачастую невозможно. Самое безопасное в данном случае - немедленное прекращение диализа, перекрытие магистралей экстракорпорального контура и отказ от возврата крови пациенту из всего экстракорпорального контура. Необходима немедленная кардиореспираторная поддержка. В зависимости от тяжести реакции внутривенно могут вводиться антигистаминные средства, стероиды и адреналин.
4. Профилактика. Всегда важна правильная промывка диализаторов перед использованием с целью тщательного удаления окиси этилена и других возможных аллергенов. Для тех, у кого в анамнезе присутствуют реакции типа А, лучше перейти на диализатор, стерилизованный другими способами (гамма-излучение, электронно-лучевая и паровая стерилизация). Необходимость прекращения использования кровепроводящих магистралей, стерилизованных этиленоксидом, при переводе на диализатор с другим методом стерилизации пока не установлена. При мягких реакциях типа А, персистирующих при переходе на диализатор с другим типом стерилизации, помогает введение антигистаминных препаратов перед процедурой. Перевод пациента на диализ с повторным использованием диализатора, а также применение процедуры реюза даже к новым диализаторам перед их первым использованием может оказаться полезным благодаря заблаговременному вымыванию из них потенциально вредных веществ и аллергенов. Целесообразны также замена гепарина или его отмена, применение диализатора с мембраной, не вызывающей активации системы комплемента, а также назначение БРА вместо иАПФ. Возможную роль контакта с латексом при подключении пациентов с повышенной чувствительностью также следует принимать во внимание.
В. Неспецифические реакции на диализатор (тип В).
1. Симптомы. Основным проявлением реакций типа В является боль за грудиной, иногда сопровождающаяся болью в спине. Симптомы появляются примерно через 20-40 минут после начала диализа. Обычно реакции типа В гораздо менее тяжелые, чем реакции типа А.
2. Этиология. Причины этих реакций неизвестны. Ранее предлагали считать «виновником» активацию системы комплемента, однако этиологическая роль этого процесса остается неопределенной. Данные о том, что боль в груди и спине встречается реже при повторном использовании диализаторов, являются противоречивыми. Повышение биосовместимости при реюзе может быть обусловлено образованием слоя белков на мембране (чего не наблюдается при отмывке хлорсодержащими агентами) или удалением потенциально токсических веществ из диализатора. Необходимо прежде всего исключить другие причины боли в груди и спине, а вывод о реакции типа В на диализатор сделать методом исключения. В частности, должен быть исключен субклинический гемолиз. Острый респираторный дистресс-синдром, связанный с гепарин-индуцированной тромбоцитопенией (Popov, 1997), может иметь внешние проявления, сходные с реакцией на диализатор В-типа.
3. Лечение. Применяется симптоматическая терапия. Следует немедленно обеспечить больному интраназальное введение кислорода. Велика вероятность развития ишемии миокарда, и если возникает приступ стенокардии, следует выполнить соответствующие лечебные мероприятия, описанные в главе 38. Диализ можно не прерывать, поскольку симптомы уменьшаются уже после первого часа процедуры.
4. Профилактика. Следует пробно использовать другой тип мембраны.
IX. ГЕМОЛИЗ. Острый гемолиз во время диализа может стать осложнением, требующим немедленного энергичного вмешательства.
A. Проявления. Клинически гемолиз проявляется болью в спине, стеснением в груди и затруднением дыхания. Может резко измениться оттенок кожи. Кровь в венозной магистрали становится цвета портвейна, плазма после центрифугирования приобретает розовый оттенок, а гематокрит резко падает. Если обширный гемолиз не обнаружить своевременно, то из разрушенных эритроцитов высвобождается большое количество калия. Гиперкалиемия приводит к резкой мышечной слабости, значительным изменениям на электрокардиограмме и в итоге к остановке сердца.
B. Этиология. Острый гемолиз наблюдается чаще всего при двух обстоятельствах:
a) обструкции или сужении просвета магистрали крови, катетера или иглы и в проблемах с диализирующим раствором. Есть вероятность наступления гемолиза на фоне сочетания дефицита глюкозо-6-фосфат-дегидрогеназы (G6PD) с применением сульфата хинина до диализа.
1. Обструкция или сужение кровепроводяшей магистрали. Во время диализа в артериальной магистрали крови могут возникнуть перегибы (Sweet, 1996). Частые случаи гемолиза, носящие характер эпидемии, могут случаться при производственных дефектах отрезка магистрали, соединяющего диализатор с венозной воздушной ловушкой (данные CDC, 1998). Гемолиз (обычно субклинический) может также наступить при несоответствии высокой скорости потока крови и слишком малого диаметра используемых игл (De Wachter, 1997). При рутинном мониторинге давления в кровепроводящих магистралях резкое его изменение может указать на многие, но не все из отмеченных выше проблем.
2. Проблемы с диализирующим раствором
a. Перегретый диализирующий раствор.
b. Гипотонический диализирующий раствор (недостаточная концентрация компонентов в воде).
с Загрязнение диализирующего раствора формальдегидом, хлорной известью, хлорамином (из водопровода), медью (если используются медные трубы), фтором, нитратами (из водопровода), цинком или перекисью водорода (см. главу 5).
C. Помощь при гемолизе. Насос крови должен быть немедленно остановлен, а магистрали крови перекрыты. Гемолизированная кровь содержит очень большое количество калия, и ее не следует возвращать пациенту. Необходимо быть готовым к лечению возникшей в результате гиперкалиемии и падению гематокрита. Пациент должен быть внимательно осмотрен, и возможно, решен вопрос о его госпитализации. В течение какого-то времени после диализа гемолиз поврежденных эритроцитов может продолжаться с развитием тяжелой гиперкалиемии. Это состояние может потребовать проведения дополнительных процедур диализа или других мер (например, перорального или ректального введения Na/K-ионобменной смолы). Далее должен быть выполнен полный клинический анализ крови с подсчетом ретикулоцитов, измерением уровня гаптоглобина, свободного гемоглобина, лактатдегидрогеназы и метгемоглобина. Необходимо также исследовать диализирующий раствор на наличие в нем загрязнений (хлорамина, нитратов, металлов), а в случае повторного использования диализатора исключить присутствие в нем остатков стерилизующих веществ.
D. Профилактика гемолиза. Если исключены брак магистрали крови и неисправность роликового насоса, приводящие к травматизации элементов крови, можно предположить, что причиной гемолиза является диализирующий раствор, образцы которого необходимо исследовать.
X. ВОЗДУШНАЯ ЭМБОЛИЯ. Воздушная эмболия -это потенциальная катастрофа, которая может привести к смерти пациента, если ее вовремя не обнаружить и не начать быстро лечить.
А. Проявления
1. Симптомы. Симптоматика зависит от положения пациента во время процедуры. В положении сидя воздух из венозной магистрали преимущественно поступает по венозной системе в мозг, минуя сердце, вызывает обструкцию венозного оттока крови из мозга, приводит к потере сознания, конвульсиям и даже смерти. В положении пациента лежа воздух устремляется к сердцу, приводя к образованию пены в правом желудочке, попадает в легкие, вызывая удушье, кашель, стеснение в груди и аритмию. Дальнейшее продвижение воздуха по системе легочных капилляров в левый желудочек может привести к эмболии артерий сердца и мозга, вызвав острую неврологическую и сердечную недостаточность.
2. Объективные признаки. Пену зачастую видно в венозной магистрали диализатора. Если воздух пошел к сердцу, то при аускультации будет слышен специфический булькающий звук.
B. Этиология. Предрасполагающие факторы и возможные пути проникновения воздуха в кровеносное русло описаны в главе 4. Самыми частыми из них являются: место введения артериальной иглы, участок артериальной магистрали между сосудистым доступом и насосом крови, а также непреднамеренно открытый порт центрального венозного катетера.
C. Неотложная помощь. Во-первых, необходимо быстро закрыть зажим венозной магистрали и остановить насос крови. Пациент немедленно должен быть переведен в лежачее положение, на левом боку вниз головой. Далее действия должны быть направлены на кардиореспираторную поддержку, в том числе подачу чистого кислорода через маску или эндотрахеальную трубку. При значительном объеме воздуха возможно проведение аспирации его из предсердия или желудочка путем чрескожной катетеризации.
D. Профилактика. См. главы 4 и 10.
XI. ДРУГИЕ ОСЛОЖНЕНИЯ. Аритмия и тампонада сердца обсуждаются в главе 38. Тяжелый дизэквилибриум-синдром, судорожные припадки и внутримозговое кровоизлияние рассматриваются в главе 40.
Рекомендуемая литература
Ahmad S, et al. Multicenter trial of L-carnitine in maintenance hemodialysis patients. II. Clinical and biochemical effects. Kidney Int. 1990; 38: 912-918.
Ahsan M, et al. Prevention of hemodialysis-related muscle cramps by intradialytic use of sequential compression devices: a report of four cases. Hemodial Int. 2004; 8: 283-286.
Brewster UC, et al. Addition of sertraline to other therapies to reduce dialysis-associated hypotension. Nephrology (Carlton). 2003; 8: 296-301.
Brunet P, et al. Tolerance of haemodialysis: a randomized cross-over trial of 5-h versus 4-h treatment time. Nephrol Dial Transplant. 1996; 11 (suppl 8): 46-51.
Centers for Disease Control and Prevention (CDC). Multistate outbreak of hemolysis in hemodialysis patients. JAMA. 1998; 280: 1299.
Chang TI, et al. Intradialytic hypotension and vascular access thrombosis. J Am Soc Nephrol. 2011; 22: 15261533.
Che-yi C, et al. Acupuncture in haemodialysis patients at the Quchi acupoint for refractory uremic pruritus. Nephrol Dial Transplant. 2005; 20: 1912-1915.
Cruz DN, et al. Midodrine and cool dialysis solution are effective therapies for symptomatic intradialytic hypotension. Am J Kidney Dis. 1999; 33: 920-926.
Curatola G, et al. Ultrafiltration intensification in hemodialysis patients improves hypertension but increases AV fistula complications and cardiovascular events. J Nephrol. 2011; 24: 465-473.
Davenport A. Using dialysis machine technology to reduce intradialytic hypotension. Hemodial Int. 2011; 15: S37.
Davenport A, et al. Achieving blood pressure targets during dialysis improves control but increases intradialytic hypotension. Kidney Int. 2008; 73: 759-764.
Daugirdas JT. Dialysis hypotension: a hemodynamic analysis. Kidney Int. 1991; 39: 233-246.
Daugirdas JT, Ing TS. First-use reactions during hemodialysis: a definition of subtypes. Kidney Int. 1988; 24: S37-S43.
De Wachter DS, et al. Blood trauma in plastic haemodialysis cannulae. Int J Artif Organs. 1997; 20: 366-370. Evans EC. Hemodialysis-related cramps and nocturnal leg cramps - what is best practice? Nephrol Nurs J. 2013; 40:549-553.
Evans RD, Rosner М. Ocular abnormalities associated with advanced kidney disease and hemodialysis. Semin Dial. 2005; 18:252-257.
Flythe J, et al. Association of mortality risk with various definitions of intradialytic hypotension. J Am Soc Nephrol. 2014; in press.
Franssen CEM. Adenosine and dialysis hypotension. Kidney Int. 2006; 69:789-791.
Geller AB, et al. Increase in post-dialysis hemoglobin can be out of proportion and unrelated to ultrafiltration. Dial Transplant. 2010; 39: 57.
Goksel BK, et al. Is low blood magnesium level associated with hemodialysis headache? Headache. 2006; 46: 40-45.
Gunal AL, et al. Gabapentin therapy for pruritus in hemodialysis patients: a randomized placebo-controlled, double-blind trial. Nephrol Dial Transplant. 2004; 19: 3137-3139.
Gwinner W, et al. Life-threatening complications of extracorporeal treatment in patients with severe eosinophilia. Int I Ar tif Organs. 2005; 28: 1224-1227.
Herrero JA, et al. Pulmonary diffusing capacity in chronic dialysis patients. Respir Med. 2002; 96: 487-492.
Huang CC, et al. Oxygen, arterial blood gases and ventilation are unchanged during dialysis in patients receiving pressure support ventilation. Respir Med. 1998; 92: 534.
Hur E, Usta M, Toz H, et al. Effect of fluid management guided by bioimpedance spectroscopy on cardiovascular parameters in hemodialysis patients: a randomized controlled trial. Aw I Kidney Dis. 2013; 61: 857-965.
Jaber BL, Pereira JBG. Dialysis reactions. Semin Dial. 1997; 10: 158-165.
Jansen PH, et al. Randomised controlled trial of hydroquinine in muscle cramps. Lancet. 1997; 349: 528.
Jefferies HJ, et al. Frequent hemodialysis schedules are associated with reduced levels of dialysis-induced cardiac injury (myocardial stunning). Clin I Am Soc Nephrol. 2011; 6: 1326-1332.
Jhawar N, et al. Effect of oxygen therapy on hemodynamic stability during hemodialysis with continuous blood volume andO2 saturation monitoring [abstract]. J Aw Soc Nephrol. 2011; 22: 812A.
Kimata N, et al. Pruritus in hemodialysis patients: results from the Japanese Dialysis Outcomes and Practice Patterns Study (JDOPPS). Hemodial Int. 2014; 18: 657-667.
Kitano Y, et al. Severe coronary stenosis is an important factor for induction and lengthy persistence of ventricular arrhythmias during and after hemodialysis. Aw I Kidney Dis. 2004; 44: 328-336.
Knoll GA, et al. A randomized, controlled trial of albumin versus saline for the treatment of intradialytic hypotension. I Am Soc Nephrol. 2004; 15: 487-492.
Ko MJ, et al. Narowband ultraviolet В phototherapy for patients with refractory uraemic pruritus: a randomized controlled trial. Br I Dermatology. 2011; 165: 633.
Krieter DH, et al. Anaphylactoid reactions during hemodialysis in sheep are ACE inhibitor dose-dependent and mediated by bradykinin. Kidney Int. 1998; 53: 1026-1035.
Kumar S, et al. Haemodiafiltration results in similar changes in intracellular water and extracellular water compared to cooled haemodialysis. Aw I Nephrol. 2013; 37: 320-324.
Landry DL, Hosseini SS, Osagie OJ, et al. Aldosterone deficiency as the cause of intradialytic hypotension and its successful management with fludricortisone [abstract]. J Aw Soc Nephrol. 2011; 22: 94.
Lemes HP, et al. Use of small doses of furosemide in chronic kidney disease patients with residual renal function undergoing hemodialysis. Clin Exp Nephrol. 2011; 15: 554-559.
Lemke H-D, et al. Hypersensitivity reactions during haemodialysis: role of complement fragments and ethylene oxide antibodies. Nephrol Dial Transplant. 1990; 5: 264.
Locatelli F, et al. The Italian Cooperative Dialysis Study Group. Effects of different membranes and dialysis technologies on patient treatment tolerance and nutritional parameters. Kidney Int. 1996; 50: 1293-1302.
Maggiore Q, et al. The effects of control of thermal balance on vascular stability in hemodialysis patients: results of the European randomized clinical trial. Aw I Kidney Dis. 2002; 40: 280-290.
Marshall MR, Dunlop JL. Are dialysate sodium levels too high? Semin Dial. 2012; 25: 277.
McCausland FR, et al. Increased dietary sodium is independently associated with greater mortality among prevalent hemodialysis patients. Kidney Int. 2012; 82: 204-211.
McIntyre CW, Odudu A. Hemodialysis-associated cardiomyopathy: a newly defined disease entity. Semin Dial. 2014; Tit 87-97.
Mettang T, Kremer AE. Uremic pruritus. Kidney Int. 2014.
Mowa S, Lynch PG, Wadhwa NK. Interaction of potassium, sodium with higher magnesium dialysate on muscle cramps in chronic hemodialysis patients [abstract]. J Aw Soc Nephrol. 2011; 22: 810A.
Najafabadi MM, et al. Zinc sulfate for relief of pruritus in patients on maintenance hemodialysis. Ther Apher Dial. 2012; 16: 142.
Narita I, et al. Etiology and prognostic significance of severe uremic pruritus in chronic hemodialysis patients. Kidney Int. 2014; 69: 1626-1632.
Odudu A, et al. Rationale and design of a multi-centre randomised controlled trial of individualised cooled dialysate to prevent left ventricular systolic dysfunction in haemodialysis patients. BMC Nephrol. 2012; 13: 45.
Oguma S, et al. Biotin ameliorates muscle cramps of hemodialysis patients: a prospective trial. Tohoku I Exp Med. 2012; 227: 217-223.
Parker TF, et al. Effect of the membrane biocompatibility on nutritional parameters in chronic hemodialysis patients. Kidney Int. 1996; 49: 551-556.
Parnes EL, Shapiro WB. Anaphylactoid reactions in hemodialysis patients treated with the AN69 dialyzer. Kidney Int. 1991; 40: 1148.
Pegues DA, et al. Anaphylactoid reactions associated with reuse of hollow-fiber hemodialyzers and ACE inhibitors. Kidney Int. 1992; 42: 1232.
Poldermans D, et al. Cardiac evaluation in hypotension-prone and hypotension-resistant dialysis patients. Kidney Int. 1999; 56: 1905-1911.
Popov D, et al. Pseudopulmonary embolism: acute respiratory distress in the syndrome of heparin-induced thrombocytopenia. Am I Kidney Dis. 1997; 29: 449-452.
Raimann JG, et al. Metabolic effects of dialyzate glucose in chronic hemodialysis: results from a prospective, randomized crossover trial. Nephrol Dial Transplant. 2012; Tit 1559-1568.
Reddan DN, et al. Intradialytic blood volume monitoring in ambulatory hemodialysis patients: a randomized trial. I Am Soc Nephrol. 2005; 16: 2162-2169.
Ritz E, et al. Cardiac changes in uraemia and their possible relationship to cardiovascular instability on dialysis. Nephrol Dial Transpl. 1990; 5: 93-97.
Roth VR, Jarvis WR. Outbreaks of infection and/or pyrogenic reactions in dialysis patients. Semin Dial. 2000; 13:92-96.
Santos SFF, Peixoto AJ. Sodium balance in maintenance hemodialysis. Semin Dial. 2010; 23: 549.
SavMY, Sav T, Senocak E, et al. Hemodialysis-related headache. Hemodial Int. 2014.
Selby NM, McIntyre CW. A systematic review of the clinical effects of reducing dialysate fluid temperature. Nephrol Dial Transplant. 2006; 21: 1883-1898.
Seukeran D, et al. Sudden deepening of pigmentation during haemodialysis due to severe haemolysis. Br I Dermatol. 1997; 137: 997-999.
Shah A, Davenport A. Does a reduction in dialysate sodium improve blood pressure control in haemodialysis patients? Nephrology (Carlton). 2012; 17: 358-363.
Sherman RA, et al. Effect of variations in dialysis solution temperature on blood pressure during hemodialysis. Am I Kidney Dis. 1984; 4: 66-68.
Sherman RA, et al. The effect of dialysis solution calcium levels on blood pressure during hemodialysis. Am I Kidney Dis. 1986; 8: 244-227.
Sherman RA, et al. The effect of red cell transfusion on hemodialysis-related hypotension. Am I Kidney Dis. 1988; 11: 33-35.
Sherman RA, et al. Postprandial blood pressure changes during hemodialysis. Aw I Kidney Dis. 1988; 12:37-39.
Shimizu K, et al. Vasopressin secretion by hypertonic saline infusion during hemodialysis: effect of cardiopulmonary recirculation. Nephrol Dial Transplant. 2012; Tit 796-803.
Silver SM, et al. Dialysis disequilibrium syndrome (DDS) in the rat: role of the «reverse urea effect». Kidney Int. 1992; 42: 161-166.
Steuer RR, et al. Reducing symptoms during hemodialysis by continuously monitoring the hematocrit. Am I Kidney Dis. 1996; Tit 525-532.
Stiller S, et al. A critical review of sodium profiling for hemodialysis. Semin Dial. 2001; 14: 337-347.
Straumann E, et al. Symmetric and asymmetric left ventricular hypertrophy in patients with end-stage renal failure on long-term hemodialysis. Clin Cardiol. 1998; 21: 672-678.
Sweet SJ. Hemolytic reactions mechanically induced by kinked hemodialysis lines. Am I Kidney Dis. 1996; Tit 262-266.
Tomson CRV. Advising dialysis patients to restrict fluid intake without restricting sodium intake is not based on evidence and is a waste of time. Nephrol Dial Transplant. 2001; 16: 1538-1542.
Trivedi H, et al. Effect of variation of blood flow rate on blood pressure during hemodialysis. ASN Annual Meeting, Philadelphia, PA. J Am Soc Nephrol. 2005; 16: 39A.
Van der Sande FM, et al. Effect of dialysis solution calcium concentration on intradialytic blood pressure course in cardiac-compromised patients. Aw I Kidney Dis. 1998; 32: 125-131.
Van der Zee S, et al. Vasopressin administration facilitates fluid removal during hemodialysis. Kidney Int. 2007; 71: 318-324.
Wikstrijm B, et al. Kappa-opioid system in uremic pruritus: multicenter, randomized, double-blind, placebo-controlled clinical studies. J Aw Soc Nephrol. 2005; 16: 3742-3747.
Yalcin AU, et al. Effect of sertraline hydrochloride on cardiac autonomic dysfunction in patients with hemodialysis-induced hypotension. Nephron Physiol. 2003; 93: P21-P28.
