- Диализному врачу
- 1. Ведение пациентов с ХБП 4-5-й стадии.
- 2. Подготовка к трансплантации, диализу или к консервативной терапии
- 3. Физиологические принципы и моделирование кинетики мочевины
- 4. Оборудование для гемодиализа и расходные материалы
- 5. Вода для диализа и диализирующий раствор
- 6. Артериовенозные фистулы и протезы. Основные положения
- 7. Центральный венозный катетер в качестве доступа: основы
- 8. Мониторинг артериовенозного доступа и осложнений
- 9. Инфекции и другие осложнения центральных венозных катетеров
- 10. Назначение острого гемодиализа
- 11. Назначение хронического гемодиализа
- 12. Осложнения в ходе процедуры гемодиализа
- 13. Повторное использование диализаторов
- 14. Антикоагуляция
- 15. Продленная заместительная почечная терапия
- 16. Гемодиафильтрация
- 17. Терапевтический аферез
- 18. Актуальность сорбционных технологий сегодня
- 19. Руководство по диализу
Центральный венозный катетер в качестве доступа: основы
I. ОБЗОР. Пациенты, получающие диализ через венозные катетеры, в большей степени подвержены различным рискам, чем пациенты на других типах доступов. У них чаще развивается инфекция, они имеют более высокие уровни воспалительных маркеров, таких как ЦРБ, и чаще умирают. Неясно, являются ли эти риски отражением особенностей популяции пациентов, получающих катетеры, некоторых факторов, действующих в ситуации, когда не удается создать другие виды доступа и требуется установка катетера, или полностью относятся собственно к использованию катетеров. Возможно, важны все три фактора. Техническая выживаемость катетеров составляет около 60% через 6 месяцев и 40% - через 1 год, если учитывать восстанавливающие вмешательства. Значимой проблемой остается недостаточный кровоток по катетеру. Номинального потока более 40 мл/мин (фактически 350 мл/мин) редко удается достичь, и обычно кровоток ограничен уровнем ближе к 300 мл/мин. Это ограничивает использование катетеров у крупных пациентов и приводит к меньшему среднему значению снижения мочевины (URR) или фракционному клиренсу мочевины (Kt/V).
В хронических условиях венозные катетеры используются долгосрочно у пациентов, у которых не удается создать другой AV-доступ. Эта группа включает маленьких детей, некоторых пациентов с диабетом и тяжелыми сосудистыми болезнями, пациентов с болезненным ожирением, пациентов, перенесших множественные вмешательства по созданию сосудистого доступа, когда все доступные места исчерпаны. Дополнительные показания включают пациентов с кардиомиопатией, не способных поддерживать адекватное давление и кровоток по доступу. Хотя катетеры первоначально поощрялись при более частом диализе, недавно получены хорошие свидетельства тому, что ночной диализ и короткий дневной диализ успешно проводятся на AV-фистулах и протезах. Возобновлена дискуссия о возможной приемлемости венозных катетеров для хронических пациентов пожилого возраста, особенно если коморбидность ограничивает ожидаемую продолжительность жизни (Drew and Lok, 2014). Частота инфицирования венозных катетеров у пожилых пациентов (старше 75 лет) относительно низка, составляя 1/3 таковой у более молодых пациентов (Murea, 2014). Неукоснительное соблюдение гигиены рук и правил по уходу за катетером привели к значимому снижению частоты инфицирования диализных катетеров (Patel, 2013).
II. ТИПЫ КАТЕТЕРОВ И ДИЗАЙН
А. Катетеры с муфтами и без муфт. Использование временных катетеров без муфт на период в несколько недель приводит к относительно высокой частоте инфицирования и не рекомендуется. Дакроновые муфты, прикрепленные к катетеру, снижают частоту перикатетерного инфицирования и миграции катетера и должны использоваться во всех случаях, где предполагается долгосрочное применение катетера, или если предполагается, что пациент будет выписан на амбулаторное лечение с катетером.
B. Вопросы дизайна. Двухпросветный венозный катетер доступен в конфигурации «двойное D», когда два просвета прилежат друг к другу боковой стороной. Коаксиальные катетеры в настоящее время используются реже. Дизайн «двойное D» порта позволяет разделять интравенозный сегмент катетера на две части ближе к точке окончания. Это обеспечивает более мягкий кончик катетера, лучшее разделение портов входа и выхода, и возможно, более низкую рециркуляцию. Катетерная система TESIO (используемая при хроническом диализе) состоит из двух полностью разделенных катетеров из силикона: один для забора, другой для возврата.
C. Импрегнация антисептиков. Некоторые диализные катетеры или муфты на них импрегнированы антисептиками или покрыты составами на основе серебра в попытке подавить бактериальный рост. В настоящее время не существует крупных исследований, демонстрирующих улучшение исходов при использовании этих катетеров.
III. ОСТРЫЙ ДИАЛИЗ
A. Показания. Венозные катетеры обычно используются для острого сосудистого доступа в следующих случаях: а) при остром почечном повреждении, б) у тех, кто требует гемодиализа или гемоперфузии из-за интоксикации, в) у пациентов с ХБП, нуждающихся в экстренном гемодиализе при отсутствии созревшего сосудистого доступа, г) у пациентов на хроническом гемодиализе, утративших эффективный постоянный доступ и требующих временного доступа до восстановления постоянного, д) у пациентов с потребностью в плазмаферезе, е) у пациентов на перитонеальном диализе на период «отдыха» брюшины до постановки нового перитонеального катетера (обычно после тяжелых перитонитов), ж) у пациентов после трансплантации, нуждающихся во временном гемодиализе на период эпизодов острого отторжения. Возобновившийся интерес к экстренному старту перитонеального диализа (см. обсуждение в главе 24), а также интерес к более раннему направлению пациентов с ХБП на создание доступа, вероятно, понизит потребность в установке центральных катетеров для гемодиализа.
B. Место введения. Доступными местами введения являются правая и левая внутренние яремные вены, бедренная вена, подключичная вена. Порядок предпочтения различных мест установки представлен в табл. 7.1. Оптимальным местом введения является правая внутренняя яремная вена, поскольку венозный путь к правому предсердию относительно короткий и прямой. Следует, как правило, избегать использования подключичных вен, поскольку это связано с высокой частотой осложнений при установке (пневмоторакс, гемоторакс, перфорация подключичной артерии, повреждение плечевого сплетения) и высокой частотой центральных венозных стенозов (до 40%). Использование левой внутренней яремной вены для острого диализа не является оптимальным, поскольку венозный путь к правому предсердию более длинный и извитой. Если существует потребность в последующем хроническом гемодиализе, идеально отказаться от использования вен на верхних конечностях, чтобы ограничить риск развития стенозов в будущем. Бедренные вены в этом отношении имеют слишком строги, с учетом результатов недавних исследований (Dugue, 2012), где медиана времени колонизации кончика катетера составляла 14 дней. Если становится очевидным, что диализ потребуется более продолжительное время, яремный катетер без муфты можно заменить на катетер с муфтой. В случае если продолжительный диализ предполагается исходно, катетер с муфтой можно устанавливать с самого начала, если возможно, в правую внутреннюю яремную вену.
Таблица 7.1. Некоторые факторы, склоняющие к выбору различных мест установки временных (нетуннельных) катетеров

C. Использование катетеров с муфтой и без нее. Риск инфицирования катетеров без муфты значимо возр астает после первой недели, поэтом у рекомендации K D O Q I 2006 года предлагают использовать катетер без муфты, если ожидаемая продолж ительность диализа составит не более одной недели. Они такж е предлагают у лежачих пациентов не оставлять бедренный катетер более чем на 5 дней. Эти рекомендации, особенно в отношении бедренных катетеров, возможно, слишком строги, с учетом результатов недавних исследований (Dugue, 2012), где медиана времени колонизации кончика катетера составляла 14 дней. Если становится очевидным, что диализ потребуется более продолжительное время, яремный катетер без муфты можно заменить на катетер с муфтой. В случае если продолжительный диализ предполагается исходно, катетер с муфтой можно устанавливать с самого начала, если возможно, в правую внутреннюю яремную вену. В недавнем исследовании было продемонстрировано успешное применение бедренного катетера с муфтой (Hingwala, 2014). Преимуществом этой локализации является расположение места выхода вне зоны кожных складок, а также простота удаления после нескольких недель использования. Установка бедренного катетера с муфтой предоставляет время для создания постоянного доступа, будь то гемодиализ или перитонеальный диализ.
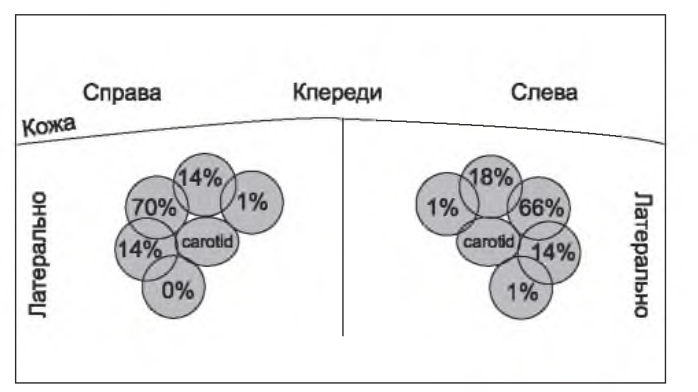
РИСУНОК 7.1. Анатомические вариации расположения яремной вены по отношению к каротидной артерии. Видоизменено из: Caridi JG, et al. Sonographic guidance when using the right internal jugular vein for central vein access. Am J Roentgenol. 1998; 171:1259-1263
D. Анатомические вариации и использование ультразвука в режиме реального времени. Центральные вены шеи демонстрируют значимую вариабельность в расположении (рис. 7.1), а редко одна из них может отсутствовать. Проблему может также составить атипичное расположение яремной артерии. При использовании ультразвукового контроля частота успешного пунктирования внутренней яремной вены с первой попытки значимо возрастает, и частота пункций каротидной артерии и гематом резко снижается (Rabindranath, 2011). На бедре вена часто расположена за артерией, и это соотношение ухудшается, если она погружается дальше от паховой складки (Beaudoin, 2011). Аналогично использование ультразвука снижает частоту осложнений (Clark and Barsuk, 2014).
E. Обучение установке катетера на симуляторе. Установка венозных катетеров для диализа - необходимый навык для нефролога, но многие программы обучения не обладают необходимыми ресурсами для тренировки. Обучение на симуляторе помогает обойти эту трудность и демонстрирует улучшение результатов в отношении исходов установки катетеров (Clark and Barsuk, 2014).
IV. ТЕХНИКА УСТАНОВКИ
А. Подготовка места установки. Катетер устанавливается с использованием техники асептики; оператор надевает стерильный костюм и перчатки для максимальной защиты зоны установки. Перед подготовкой поля полезно провести ультразвуковое исследование, чтобы убедиться, что у пациента имеется подходящая вена в избранном месте. Место введения следует очистить по стандартной методике подготовки операционного поля и отграничить его салфетками (включая плечо и стенку грудной клетки, если устанавливается катетер с муфтой). Ультразвуковой датчик следует обернуть стерильным чехлом.
В. Яремный подход. Ультразвуковой датчик можно расположить параллельно оси сосуда, а вводимую иглу направить к концу или короткой оси датчика. Альтернативно датчик можно расположить перпендикулярно длинной оси сосуда. Этот подход представляет вену в более наглядном виде, как окружность, но ограничивает визуализацию иглы. Вена обычно сдавливается мягким давлением датчика, тогда как артерия - нет. Кроме того, диаметр вены увеличивается в пробе Вальсальвы, что можно легко увидеть при ультразвуковом исследовании. Для внутренней яремной вены ультразвуковой датчик устанавливается параллельно и выше ключицы в углублении между стернальной и ключичной головками грудино-ключично-сосцевидной мышцы. Важно избегать введения катетера сквозь мышцу, поскольку это некомфортно для пациента и может привести к дисфункции катетера при вращении шеей.
1. Введение проводника по игле 21G. Место введения инфильтрируется местной анестезией, под контролем ультразвука игла 21G с присоединенным шприцем вводится в вену. Малый размер иглы ограничивает возможные осложнения в случае непреднамеренной пункции артерии. Под прямым визуальным контролем стенка вены вдавливается внутрь непосредственно перед проникновением иглы в просвет сосуда. Шприц удаляется, и проводник 0,018" вводится через иглу. Проводник продвигается вперед, положение проводника контролируется на флюороскопии.
2. Введение дилататора по проводнику. Затем игла удаляется, и коаксиальный дила-татор продвигается по проводнику. Проводник и внутренний дилататор 3F удаляется, а внешний дилататор 5F остается. К дилататору присоединяется проводник для предотвращения воздушной эмболии.
3. Введение катетера без муфты. Дальнейшие шаги зависят от наличия муфты на катетере. Для временного катетера стандартный проводник 0,035" проводится в вену, и дилататор 5F удаляется. Поэтапно дилататоры возрастающих размеров проводятся по проводнику, расширяя тракт в мягких тканях и стенки вены. Дилататор должен двигаться свободно по проводнику. Если имеются какие-либо сомнения в расположении дилататора, следует проверить их при флюороскопии. Последний дилататор заменяется временным катетером, который также проводится по проводнику. После фиксации катетера следует выполнить рентгенографию для подтверждения правильности расположения катетера, если флюороскопия не была доступна во время введения. Если пациенту в последующем потребуется долгосрочный диализ, временный катетер без муфты, расположенный во внутренней яремной вене, можно безопасно заменить на туннелированный катетер с муфтой при отсутствии признаков инфекции места выхода.
4. Установка катетера с муфтой
а) Создание места выхода и тоннеля. При установке катетера с муфтой проводится маленький разрез в месте вывода дилататора 5F латеральнее места прокола. Подкожные ткани затем проходятся тупым методом, так чтобы катетер в последующем не мог перегибаться и чтобы убедиться, что ди-лататор 5F свободно располагается в мягких тканях. Затем определяется место выхода катетера. Это можно сделать при помощи техники разметки четвертого межреберного интервала, или длину катетера можно определить точнее, используя проводник для того, чтобы измерить расстояние между местом его введения до правого предсердия. Используя это измерение, длину туннеля можно определить таким образом, чтобы муфта располагалась внутри туннеля на 1-2 см от места выхода.
5. Введение катетера через кожу в месте выхода. После того как определено будущее место выхода катетера, в зону вокруг него вводится местная анестезия; проводится прокол кожи скальпелем (11-го размера). Скальпель вводится до самой широкой точки лезвия, что соответствует размеру большинства двухпросветных катетеров. Длинная игла используется для инфильтрирования местным анестетиком туннельного тракта, идущего от места выхода к точке венотомии. Катетер прикрепляется к концу туннелирующего устройства, которое протягивается от места выхода катетера к месту прокола вены. Муфта катетера втягивается в туннель, после чего туннелирующее устройство отсоединяется.
6. Расширение венозного тракта. Проводник к этому этапу проведен через дилата-тор в нижнюю полую вену. Расположение проводника в нижней полой вене снижает вероятность сердечных аритмий. Может использоваться проводник из комплекта катетера. Дилататор 5 F затем удаляется, и по проводнику последовательно проводятся дилататоры возрастающего размера для расширения венозного тракта в мягких тканях. Дилататор должен двигаться по проводнику свободно. Дилататор может сместиться с оси и перфорировать вену и/или средостение. Учитывая это обстоятельство, не следует продвигать дилататор на всю длину, ограничившись длиной, соответствующей расстоянию от кожи до вены. Если существуют какие-либо сомнения в расположении дилататора, следует использовать флюороскопию для подтверждения его правильной позиции.
7. Завершение введения катетера. После окончания расширения дилататор вводится с удаляемым футляром. При продвижении футляра ощущается сопротивление мягких тканей, а затем финальное сопротивление при проникновении в вену. Дилататор и футляр затем удаляются, и катетер продвигается по проводнику без использования футляра в конечное положение (бесфутлярное введение). Иногда требуется некоторое усилие при продвижении катетера через тракт. Эта процедура снижает вероятность воздушной эмболии и приводит к меньшему размеру венотомии и меньшему кровотечению при проведении.
Альтернативно, если используется удаляемый футляр, его слегка продвигают по дилататору, который затем удаляется с оставлением проводника на месте, на случай возможных сложностей. Футляр следует сжимать между пальцами, чтобы перекрыть его просвет. Это предотвращает кровотечение и/или аспирацию, если оставлять достаточную длину футляра для введения катетера. Когда дилататор и проводник удаляются, катетер вводится в просвет футляра так, чтобы предотвратить перекручивание. При проведении катетера по футляру он смещается назад к коже. Когда катетер заведен на максимальную глубину, футляр удаляется. Методика предотвращает создание венозного тракта избыточного размера.
8. Фиксация муфты катетера. После удаления футляра катетер подтягивается назад по туннелю так, чтобы муфта расположилась на глубине 1-2 см от места выхода. Проверяется правильное функционирование катетера. Шприц объемом 10 мл должен быстро наполняться кровью без перерыва в кровотоке, для того чтобы он был способен обеспечить кровоток в 300 мл/мин.
Разрез в месте венопункции ушивается после подтверждения адекватного кровотока. Швы не должны накладываться в месте выхода, поскольку являются путем проникновения инфекции. Дополнительный шов требуется для поддержания положения катетера. Использование «воздушного узла» для фиксации катетера повышает комфорт пациента и снижает вероятность развития некроза кожи. Подкожная муфта в конце концов будет удерживать катетер в заданной позиции, фиксируя его к подкожным тканям. Может использоваться местное применение антибиотиков в виде мази на место разреза и место пункции вены. Рана содержится под повязкой.
С. Бедренный доступ. При бедренном доступе используются, как правило, катетеры без муфты, хотя могут устанавливаться и катетеры с муфтой. Пациент укладывается горизонтально на спину со слегка согнутыми коленями и отведенной и повернутой наружу ногой. Поверхность кожи бедра бреется, очищается, обрабатывается и операционное поле отграничивается салфетками. Проводится анестезия по ходу бедренной иглы на 24 см ниже паховой связки, с использованием иглы 21G со шприцем, заполненным гепарином и местным анестетиком. Как отмечено ранее, для успеха процедуры очень важно использование УЗИ в реальном времени. Небольшое количество анестетика вводится вокруг иглы для предотвращения венозного спазма. Проводник вводится в вену через иглу 18G. Важно, чтобы проводник свободно перемещался вперед и назад. Если проводник перемещается с трудом, возможно, он попал в боковую ветвь бедренной вены. В этих условиях катетер не следует устанавливать. Напротив, проводник следует полностью удалить, угол введения иглы изменить (иногда порт иглы приходится опускать до уровня кожи, почти параллельно с веной), после чего ввести проводник повторно. После достижения свободного перемещения проводника игла 18G удаляется, и канюля вводится снова. Оставшаяся часть процедуры аналогична установке катетера в яремную вену, описанной выше.
V. ОСЛОЖНЕНИЯ, СВЯЗАННЫЕ С УСТАНОВКОЙ. Эти осложнения перечислены в табл. 7.2. При пункции артерии иглой малого размера следует приложить местное давление на 15-20 минут. Катетер ни в коем случае не должен быть введен в артерию. В случае непреднамеренной установки катетера в артерию диализ следует отложить и рассмотреть хирургическое вмешательство для предотвращения образования большой гематомы и сдавления трахеи. В случае установки в бедренную артерию (равно как и при непреднамеренной пункции задней стенки вены) может развиться тяжелое ретроперитонеальное жизнеугрожающее кровоизлияние. Крупный пневмоторакс или гемоторакс обычно требует установки дренажа в плевральную полость. Перфорация верхней полой вены или камер сердца является жизнеугрожающим осложнением. На такую возможность указывает неожиданная боль в груди, одышка и гипотония сразу после начала диализа. Иногда требуется хирургическое вмешательство. Инфекционные осложнения можно минимизировать, обеспечивая при установке катетера гигиену рук, использование стерильных перчаток, масок и хирургической одежды, а также отграничивая операционное поле стерильной тканью большого размера и применяя хлоргексидин в качестве антисептика до начала процедуры (O’Grady, 2011).
Таблица 7.2 Осложнения катетеризации центральной вены

VI. УХОД ЗА ВЕНОЗНЫМ КАТЕТЕРОМ
A. Перевязки. Во время подсоединения и отсоединения катетера диализный персонал и пациент должны быть в хирургических масках. Не следует использовать щиток на лицо без хирургической маски, поскольку щиток направляет дыхание непосредственно на катетер. Просвет и кончики катетера не должны оставаться открытыми на воздухе. Колпачки или шприц всегда должны закрывать просвет катетера, создавая чистую зону места соединения. Просвет сосуда следует держать стерильным: инфузии через катетер в ходе диализа запрещены.
После каждого диализа разъемы катетера следует замачивать в антисептике на 3-5 минут, а затем высушивать перед рассоединением. Антисептики на растворе хлоргексидина (больше 0,5%) дают лучшие результаты, чем повидон-йод (Mimoz, 2007; Onder, 2009). После отсоединения каждой магистрали от катетера разъемы катетера следует обработать раствором хлоргексидина (табл. 7.3). Катетер покрывают стерильной сухой салфеткой. Воздухонепроницаемые прозрачные пленки не следует использовать для укрывания места выхода катетера, поскольку они в большей мере содействуют колонизации, чем сухие салфетки. Наилучший тип укрывания катетера перевязочным материалом не определен. В США центр инфекционного контроля рекомендует «использовать или стерильные салфетки, или стерильные прозрачные полупроницаемые пленки для укрывания катетера» (O’Grady, 2011). Центр предоставляет материалы для обучения, включая видеоматериалы, демонстрирующие наилучшую технику для смены повязок на катетере (CDC, 2014).
B. Риск воздушной эмболии при удалении катетера из области шеи.Сообщалось о летальных исходах из-за воздушной эмболии после удаления яремных венозных катетерев (Boer and Hene, 1999). Из-за наличия такого риска удаление катетеров требуется проводить по протоколу. Подобный протокол (Boer and Hene, 1999) включает следующее.
Таблица 7.3 Ключевые мероприятия, рекомендованные Centers for Disease Control (CDC) США для предотвращения бактериемии
1. Наблюдение и обратная связь.
Ежемесячно оценивайте частоту бактериемии и других событий, используя рекомендации CDC. Рассчитывайте частоту инфекции, сравнивайте ее с таковой в других центрах. Активно делитесь результатами оценок с персоналом.
2. Наблюдение за гигиеной рук.
Проводите наблюдение за гигиеной рук ежемесячно и делитесь результатами с клиническим персоналом.
3. Наблюдение за состоянием катетера/сосудистого доступа.
Ежеквартально проводите наблюдение за практикой ухода за сосудистым доступом и оценкой состояния катетера. Оценивайте приверженность персонала технике асептики при соединении и отсоединении катетера, а также при перевязках. Делитесь результатами с клиническим персоналом.
4. Обучение персонала и его компетентность.
Проводите повторное обучение по теме инфекционного контроля, включая практику ухода за сосудистым доступом и техникой асептики. Проводите оценку компетентности и навыков в этой области каждые 6-12 месяцев и для нового персонала.
5. Обучение/привлечение пациентов.
Проводите стандартизованное обучение для всех пациентов по теме инфекционного контроля, включая вопросы ухода за сосудистым доступом, гигиены рук, рисков, связанных с использованием катетера, выявления признаков инфекции, а также проводите инструктаж по уходу за доступом вне диализного отделения.
6. Уменьшение использования катетеров.
Соединяйте усилия (например, через обучение пациентов, работу координаторов по сосудистому доступу) для уменьшения частоты использования катетеров путем выявления и снятия барьеров к созданию перманентного сосудистого доступа и удаления катетера.
7. Хлоргексидин как кожный антисептик.
Используйте хлоргексидин на основе спирта (больше 0,5%) в качестве антисептика первой линии при установке центральных венозных катетеров и при смене повязки.
8. Дезинфекция порта катетера.
Обрабатывайте порт катетера подходящим антисептиком после снятия колпачков перед использованием. Делайте это каждый раз при рассоединении катетера.
9. Антимикробная мазь.
Накладывайте антимикробную мазь или мазь с повидон-йодом на место выхода катетера при смене повязки.
Воспроизведено из: National Center for Emerging and Zoonotic Infectious Diseases, Center for Disease Control and Prevention. http://www. cdc.gov/dialysis/PDFs/Dialysis-Core-lnterventions-5_10_13.pdf.
1. В день удаления гепарин не используется. Вводится протамин, если гепарин был применен. Пациент располагается в положении с опущенной головой во время удаления катетера. Пациента просят не кашлять и не делать глубоких вдохов во время удаления. Используется воздухонепроницаемая повязка и достаточное количество нейтральной мази, чтобы обеспечить надежную преграду для воздуха. Пациент находится под наблюдением в течение 30 минут, прежде чем покинуть центр. Воздухонепроницаемая повязка остается на 24 часа.
C. Методика смены катетера по проводнику. Основания для смены катетера по проводнику (дисфункция, инфекция) детально обсуждены в главе 9. Техника смены яремного катетера следующая. Стенка грудной клетки и старый катетер укрываются стерильной салфеткой. Оператор надевает двойные перчатки. Проводится инфильтрационная анестезия старого места выхода и вокруг муфты существующего катетера. Из обоих портов катетера необходимо аспирировать содержимое, чтобы освободить их от гепарина. Используя гемостаз, проводится тупое выделение муфты катетера. На этом этапе проводник проводится в венозный просвет катетера и направляется в нижнюю полую вену. Катетер мягко вытягивается до уровня плечеголовной вены. Через артериальный порт проводится инъекция контраста, чтобы проверить наличие фибринового футляра. При его наличии следует рассмотреть баллонную ангиопластику и повторить инъекцию контраста, чтобы оценить результаты удаления фибринового футляра. Старый катетер удаляется, проводник остается на месте.
На этом этапе оператор снимает наружную пару перчаток, перед тем как начать работать с новым катетером. Эта процедура позволяет минимизировать передачу инфекции со старого катетера на новый. Новый катетер затем проводится по проводнику в правое предсердие. Функция катетера оценивается по описанной выше методике.
D. Купание и принятие душа. Место выхода никогда не следует погружать в воду в ванной. Использования душа следует избегать. В любом случае пациент должен принимать его до прихода в диализное отделение, где будет проведена смена повязки и наложение антибактериальной мази. Принимать душ можно только после того, как сформируется синусовый тракт места выхода. В недавних исследованиях у избранных пациентов использование душа в комбинации с введением туннелированных центральных катетеров без повязки не увеличивало риск инфекции (Lawrence, 2014). Купание с погружением, в том числе в хлорированную воду, не следует поощрять из-за опасения инфекции.
E. Замки катетера
1. Гепарин. После каждого сеанса мертвое пространство каждого просвета заполняется гепарином через инъекционный порт, доза 1000-5000 ЕД/мл. Любой раствор замка будет вытекать до уровня наиболее проксимального отверстия в катетере. Поэтому использование более высоких доз гепарина (5000 vs 1000 ЕД/мл) может привести к значимой системной антикоагуляции; в одном из исследований более высокая концентрация гепарина была связана с меньшей потребностью в тканевом активаторе плазминогена (Мауа, 2010). Мертвое пространство каждого просвета катетера варьирует у разных производителей и в зависимости от длины катетера. Необходимый объем гепарина обычно указывается на разъеме катетера. Важно отметить этот объем в карте пациента, чтобы эта информация всегда была доступна для диализного персонала. Введения гепарина в большем объеме следует избегать, поскольку в результате повышение системной антикоагуляции может нести в себе риски кровотечения. Перед каждым сеансом диализа раствор гепарина из каждого просвета аспирируется, и катетер промывается гепаринизированным физраствором (100 ЕД/мл), после чего начинается гемодиализ.
2. Цитрат 4%. Раствор цитрата можно использовать в качестве антикоагулянта, поскольку он связывает кальций - критичный компонент для свертывания крови. По данным метаанализа, проведенного в 2014 году, растворы на основе цитрата, содержащие антибиотики или антисептики, показали лучшие результаты в снижении частоты катетер-ассоциированной бактериемии, чем гепарин-содержащие аналоги. Цитрат без добавок был более эффективен, чем гепарин, но использовался в более высокой концентрации (30%). Более низкие концентрации не имели преимуществ перед гепарином (Zhao, 2014). Показано, что цитрат быстро вытекает из замков катетера в циркуляцию, что снижает его концентрацию до уровней меньше тех, что подавляют рост бактерий (Schilcher, 2014). В США в 2000 году использование цитрата очень высокой концентрации связали с сердечной аритмией и смертью пациента предположительно в результате непреднамеренной инъекции концентрированного цитрата в левое предсердие, что резко понизило уровень ионизированного кальция (Polaschegg and Sodemann, 2003). Разумно использовать низкие концентрации цитрата (4%), понимая, однако, что эффективность цитрата в этих концентрациях не выше таковой для гепарина. Использование цитрата в любых концентрациях проблематично в странах (таких, как США), где малые объемы таких растворов недоступны.
3. Другие замки. Другие варианты замков содержат в себе гепарин, цитрат, этанол или EDTA плюс один или более антибиотиков или антисептиков. В настоящее время использование антибиотик-содержащих замков не является обычной практикой в результате ряда факторов: дополнительной стоимости, практических вопросов касательно смешивания компонентов и опасений в отношении формирования устойчивых микроорганизмов. Использование ванкомицина и гентамицина в качестве замков увеличило распространенность Staphylococcus и резистентного Enterobacter (Dixon, 2012). В настоящее время в США не рекомендуется рутинное использование замков, содержащих антибиотики (Camins, 2013), в то время как в соответствии с Европейскими рекомендациями по наилучшей практике приемлемы оба варианта (Vanholder, 2010).
Поиск растворов для замка для предотвращения инфицирования катетеров является зоной активных исследований. Задачей является не только стерилизация внутреннего объема катетера, но и предотвращение образования биопленок. Растворы для замка, содержащие этанол, цитрат или EDTA, имеют теоретическое преимущество, более активно предотвращая образование биопленок. Растворы, содержащие глицерил-тринитрат, цитрат и этанол, продемонстрировали определенную эффективность против бактерий, которые обычно находят в биопленках (Rosenblatt, 2013). Разработаны и другие растворы для замков, которые находятся на различных стадиях тестирования. Показано, что смесь цитрата, метиленового голубого, метил-парабена и пролил-парабена снижает частоту связанной с катетерами бактериемии (Maki, 2011). Существует определенный энтузиазм в отношении замков, содержащих комбинацию тауролидина и цитрата. Возможно, что использование тауролидина, который является дезинфектантом и ингибирует образование биопленок, может оказаться не связанным с формированием резистентности бактерий (Liu, 2014).
F. Профилактическое использование антибиотиков. Системные антибиотики обычно не назначаются перед установкой туннельного катетера.
1. Мази на место выхода. Показано, что использование мази с мупироцином в месте выхода катетера для уменьшения колонизации стафилококками снижает частоту катетерной инфекции и повышает выживаемость (McCann and Moore, 2010; O’Grady, 2011); этот метод, однако, не используется широко из опасений формирования мупироцин-резистентных микроорганизмов. В США рекомендуется использование мази в месте выхода (табл. 7.3), но обеспокоенность в отношении формирования резистентных организмов сохраняется. В Европейских рекомендациях по наилучшей практике мазь рекомендуется только на период заживления места выхода катетера (Vanholder, 2010). Как промежуточную стратегию накладывание мази на место выхода можно ограничить только у пациентов с частыми эпизодами инфекции. Перед использованием любой мази следует убедиться, что ее основа не взаимодействует с пластиком катетера.
2. Деколонизация пололи носа. Показано, что у пациентов с носительством стафилококка мероприятия по деколонизации снижают частоту связанной с катетером бактериемии (Abad, 2013), но остается спектр мупироцин-резистентных микроорганизмов (Тео, 2011). Это лечение остается более привлекательной опцией для избранных пациентов, чем для всех пациентов в целом, хотя деколонизация (например, мультирезистентного S. aureus) была применена у всех пациентов диализного центра с обнадеживающим краткосрочным результатом (Kang, 2012).
Ссылки и рекомендуемая литература
Abad CL, et al. Does the nose know? An update on MRSE decolonization strategies. Curr Infect Dis Rep. 2013; 15:455-464.
Allon M. Dialysis catheter-related bacteremia: treatment and prophylaxis. Aw J Kidney Dis. 2004; 44:779-791. Beathard GA. Management of bacteremia associated with tunneled-cuffed hemodialysis catheters. J Am Soc Nephrol. 1999; 10: 1045-1049.
Beaudoin FL, et al. Bedside ultrasonography detects significant femoral vessel overlap: implications for central venous cannulation. Can JEmergMed. 2011; 13: 245-250.
Bevilacqua JL, et al. Comparison of trisodium citrate and heparin as catheter-locking solution in hemodialysis patients. I Bras Nefrol. 2011; 33: 68-73.
Boer WH, Hene RJ. Lethal air embolism following removal of a double lumen jugular catheter. Nephrol Dial Transplant. 1999; 14: 1850-1852.
Camins BC. Preventions and treatment of hemodialysis-related bloodstream infections. Semin Dial. 2013; 26: 476-481.
Centers for Disease Control. Guidelines of the prevention of intravascular catheter-related infections. 2011. http://www.cdc.gov/hicpac/pdf/guidelines/bsi-guidelines-2011.pdf.
Centers for Disease Control. Training video and print resources for preventing bloodstream and other infections in outpatient hemodialysis patients. Best practices for dialysis staff. 2014.
http://www.cdc.gov/dialysis/ prevention-tools/training-vi deo.html.
Clark EG, Barsuk JH. Temporary hemodialysis catheters: recent advances. Kidney Int. 2014. doi: 10.1038/ ki.2014.162.
Clase CM, et al. Thrombolysis for restoration of patency to hemodialysis central venous catheters: a systematic review. I Thrornb Thrombolysis. 2001; 11 (2): 127-136.
Dixon J J, Steele M, Makanjuola AD. Anti-microbial locks increase the prevalence of Staphylococcus aureusand antibiotic-resistant Enterobacter: observational retrospective cohort study. Nephrol Dial Transplant. 2012; Tit 3575-3581.
Drew DA, Lok CE. Strategies for planning the optimal dialysis access for an individual patient. Curr Opin Nephrol Hypertens. 2014; 23: 314-320.
Dugue AE, et al; for the Cathedia Study Group. Vascular access sites for acute renal replacement in intensive care units. Clin I Am Soc Nephrol. 2012; 7:70-77.
Frankel A. Temporary access and central venous catheters. Eur I Vase Endovasc Surg. 2006; 31: 417-422. Haymond J, et al. Efficacy of low-dose alteplase for treatment of hemodialysis catheter occlusions. I Vase Access. 2005; 6:76-82.
Hebert C, Robicsek A. Decolonization therapy in infection control. Curr Opin Infect Dis. 2010; 23: 340-345.
Hingwala J, Bhola С, Lok СЕ. Using tunneled femoral vein catheters for «urgent start» dialysis patients: a preliminary report. J Vase Access. 2014; 15 (suppl 7): 101-108.
Johnson DW, et al. A randomized controlled trial of topical exit site mupirocin application in patients with tunnelled, cuffed haemodialysis catheters. Nephrol Dial Transplant. 2002; 17: 1802-1807.
Kang YC, et al. Methicillin-resistant Staphylococcus aureusnasal carriage among patients receiving hemodialysis in Taiwan: prevalence rate, molecular characterization and de-colonization. BMC Infect Dis. 2012; 12:284.
Lawrence JA, et al. Shower and no-dressing technique for tunneled central venous hemodialysis catheters: a quality improvement initiative. Nephrol Nurs J. 2014; 41: 67-72.
Lee T, Barker J, Allon M. Tunneled catheters in hemodialysis patients: reasons and subsequent outcomes. Am J Kidney Dis. 2005M6: 501-508.
Little MA, Walshe JJ. A longitudinal study of the repeated use of alteplase as therapy for tunneled hemodialysis dysfunction. Aw I Kidney Dis. 2002; 39: 86-91.
Liu H, et al. Preventing catheter-related bacteremia with taurolidine-citrate catheter locks. A systemic review and meta-analysis. Blood Purtf. 2014; 37: 179-187.
Lok CE, et al. A patient-focused approach to thrombolytic use in the management of catheter malfunction. Semin Dial. 2006-, 19: 381-390.
Maki DG, et al. A novel antimicrobial and antithrombotic lock solution for hemodialysis catheters: A multicenter, controlled, randomized trial. Crit Care Med. 2011; 39: 613-620.
Maya ID, Allon M. Outcomes of tunneled femoral hemodialysis catheters: comparison with internal jugular vein catheters. Kidney Int. 2005; 68: 2886-2889.
Maya ID, et al. Does the heparin lock concentration affect hemodialysis catheter patency? Clin I Am Soc Nephrol. 2010; 5:1458-1462.
McCann M, Moore ZE. Interventions for preventing infectious complications in haemodialysis patients with central venous catheters. Cochrane Database Syst Rev. 2010; (1): CD006894.
Mermel LA, et al. Guidelines for the management of intravascular catheter-related infections. Clin Infect Dis. 2001; 32: 1249-1272.
Mimoz O, et al. Chlorhexi dine-based antiseptic solution vs alcohol-based povidone-iodine for central venous catheter care. Arch Intern Med. 2007; 167: 2066-2067.
Mokrzycki MH, et al. A randomized trial of minidose warfarin for the prevention of late malfunction in tunneled, cuffed hemodialysis catheters. Kidney Int. 2001; 59: 1935-1942.
Murea M, et al. Risk of catheter-related bloodstream infection in elderly patients on hemodialysis. Clin I Am Soc Nephrol. 2014; 9: 764-770.
O’Grady NP, et al. Guidelines for the prevention of intravascular catheter-related infections. Aw I Infect Control. 2011; 39 (suppl): S1-S34.
Oliver MJ, et al. Risk of bacteremia from temporary hemodialysis catheters by site of insertion and duration of use: a prospective study. Kidney Int. 2000; 58: 2543-2545.
Onder AM, et al. Chlorhexi dine-based antiseptic solutions effectively reduce catheter related bacteremia. Pedi-atr Nephrol. 2009; 224: 1741-1747.
Patel PR, et al. Bloodstream infection rates in outpatient hemodialysis facilities participating in a collaborative prevention effort: a quality improvement report. Aw I Kidney Dis. 2013; 62: 322-330.
Polaschegg HD, Sodemann K. Risks related to catheter locking solutions containing concentrated citrate. Nephrol Dial Transplant. 2003; 18: 2688-2690.
Rabindranath KS, et al. Ultrasound use for the placement of haemodialysis catheters. Cochrane Database Syst Rev. 2011; (11): CD005279.
Rosenblatt J, et al. Glyceryl trinitrate complements citrate and ethanol in a novel antimicrobial catheter lock solution to eradicate biofilm organisms. Antimicrob Agents Chemother. 2013; 57: 3555-3560.
Schilcher G, et al. Loss of antimicrobial effect of trisodium citrate due to ‘lock’ spillage from haemodialysis catheters. Nephrol Dial Transplant. 2014; 29: 914-919.
Silva TNV, et al. Approach to prophylactic measures for central venous catheterrelated infections in hemodialysis. A critical review. Hemodial Int. 2014; 18: 15-23.
Teo BW, et al. High prevalence of mupirocin-resistant staphylococci in a dialysis unit where mupirocin and chlorhexidine are routinely used for prevention of catheterrelated infections. I Med Microbiol. 2011; 60 (pt 6): 865-867.
Vanholder RM, et al. Diagnosis, prevention, and treatment of haemodialysis catheterrelated bloodstreams infections (CRBSI): a position statement of European Renal Best Practice (ERBP). Nephrol Dial Transplant. 2010;3:234-246.
Zhao Y, et al. Citrate versus heparin lock for hemodialysis catheters: a systematic review and meta-analysis of randomized controlled trials. Aw I Kidney Dis. 2014; 63: 479-490.
Интернет-ссылки
American Society of Diagnostic and Interventional Nephrology, http://www.asdin.org/.
CDC guidelines for prevention of intravascular catheter-related infections, http://www.cdc.gov/dialysis.
HDCN vascular access channel, http://www.hdcn.com/ch/access/.
KDOQI 2006 access guidelines, http://www.kidney.org/professionals/kdoqi/ guideline_upHD PD _VA/index. htm.
Vascular Access Society guidelines, http://www.vascularaccesssociety.com/guidelines.html. YouTube link (11 min). https://www.youtube.com/watch?v=_OzhYOJMGCA&feature=youtu.be.
