- Диализному врачу
- 1. Ведение пациентов с ХБП 4-5-й стадии.
- 2. Подготовка к трансплантации, диализу или к консервативной терапии
- 3. Физиологические принципы и моделирование кинетики мочевины
- 4. Оборудование для гемодиализа и расходные материалы
- 5. Вода для диализа и диализирующий раствор
- 6. Артериовенозные фистулы и протезы. Основные положения
- 7. Центральный венозный катетер в качестве доступа: основы
- 8. Мониторинг артериовенозного доступа и осложнений
- 9. Инфекции и другие осложнения центральных венозных катетеров
- 10. Назначение острого гемодиализа
- 11. Назначение хронического гемодиализа
- 12. Осложнения в ходе процедуры гемодиализа
- 13. Повторное использование диализаторов
- 14. Антикоагуляция
- 15. Продленная заместительная почечная терапия
- 16. Гемодиафильтрация
- 17. Терапевтический аферез
- 18. Актуальность сорбционных технологий сегодня
- 19. Руководство по диализу
Инфекции и другие осложнения центральных венозных катетеров
Главными проблемами, связанными с центральными венозными катетерами (ЦВК), являются инфекции, плохой кровоток, тромбоз и стеноз центральных вен.
I. ИНФЕКЦИИ. Несмотря на проведение оптимальных мероприятий, детализированных в главе 7, табл. 7.3, при использовании ЦВК часто встречаются инфекционные осложнения, и их частота существенно выше, чем при АВФ. Инфекции - это главная причина потери катетеров и увеличения заболеваемости и смертности. Чаще всего к инфекциям приводят загрязнение коннектора катетера или его просвета в ходе диализа или от инфузионных растворов. Инфекция может также мигрировать с кожи пациента через место пункции и по внешней поверхности катетера. Иногда катетеры могут инфицироваться из удаленных мест при развитии бактериемии.
A. Инфекции места выхода диагностируются по эритеме, отделяемому и уплотнению кожи вокруг места выхода; при этом нет уплотнения или гнойного выделения по ходу туннеля. Местного лечения антибактериальным кремом или пероральными антибиотиками может оказаться достаточно. Эти инфекции можно предотвратить тщательным уходом за местом выхода катетера. Следует обследовать пациента на носительство стафилококка и в случае его обнаружения лечить интраназальным мупироцином в течение пяти дней для предотвращения развития инфекции. При развитии инфекции места выхода катетер подлежит удалению в случае развития системных признаков инфекции (лейкоцитоз или температура выше 38°), а также если можно получить гной из тракта катетера или если инфекция персистирует или повторяется после начального курса антибиотиков. В случае положительного посева крови катетер также следует удалить.
B. Туннельная инфекция. Туннельной инфекцией называют распространение инфекции вдоль подкожного туннеля по направлению к муфте и месту введения катетера. Как правило, присутствует значимое уплотнение, отек и эритема вдоль тракта катетера, в сочетании с гнойным отделяемым из места выхода. Это может привести к системной бактериемии. В этом случае катетер следует немедленно удалить и начать антибактериальную терапию.
C. Связанная с катетером бактериемия. Пациент демонстрирует симптомы и признаки системной инфекции в диапазоне от минимальных до тяжелых. Легкие случаи сопровождаются лихорадкой и ознобом, тогда как более тяжелые могут привести к гемодинамической нестабильности. После начала диализа у пациента могут развиться симптомы сепсиса, что указывает на освобождение бактерий и/или эндотоксинов с катетера в системную циркуляцию. Возможно появление метастатической инфекции, включая эндокардит, остеомиелит, эпидуральный абсцесс или септический артрит. В большинстве случаев причиной являются грамположительные микробы. Детали лечения таких пациентов хорошо описаны в диализной секции материалов сайта U.S. Centers of Disease Control (CDC) (http://www.cdc.gov/dialysis), Рекомендациях NKF KDOQI 2006 по сосудистому доступу (NKF, 2006), в Европейских рекомендациях по наилучшей клинической практике (ERBP) по сосудистому доступу (Tordoir, 2007), Рекомендациях Infectious Disease Society of North America (IDSA) по лечению катетерной бактериемии (Mermel, 2009) и в комментариях ERBP к Рекомендациям IDSA (Vanholder, 2010). Алгоритмы представлены на рис. 9.1 и в табл. 9.1 и 9.2. Ключевые европейские рекомендации показаны на рис. 9.2. Принципы лечения бактериемии у диализных пациентов отличаются от таковых при инфицировании устанавливаемых на короткое время инфузионных венозных катетеров. У пациентов на диализе венозный катетер является жизненно необходимым, и заменить его можно иногда с большим трудом. Поэтому рекомендации включают в себя разнообразные меры по сохранению катетера: содержащие антибиотики катетерные замки, замена инфицированного катетера новым в том же месте по проводнику. Использование этих мер, однако, следует ограничивать определенными обстоятельствами. Если состояние пациента ухудшается, в короткий период после этих процедур катетер следует удалить, чтобы минимизировать риски распространения инфекции.
1. Посевы крови и частей катетера. При подозрении на инфекцию посевы можно получить с разъемов катетера, из периферической вены или из диализных магистралей. Рекомендации IDSA предлагают брать посевы с разъема катетера и из периферической вены, а после удаления катетера - с дистальных пяти сантиметров его окончания. Мы ищем совпадение результатов для подтверждения того, что оба посева выявляют один и тот же микроорганизм. При заборе посевов с кожи или разъема катетера Рекомендации IDSA предлагают очищать и дезинфицировать зону спиртовым раствором хлоргекси-дина, но не повидон-йодом, и давать возможность антисептику высыхать перед взятием проб. Это предотвращает контаминацию материалов посевов. Рекомендации признают кровь из магистрали приемлемой заменой периферической крови в отношении проведения посевов.
Европейские рекомендации схожи с Рекомендациями IDSA. В них также отмечается трудность взятия посевов из периферической вены у гемодиализных пациентов; практической альтернативой признается взятие крови из диализного контура. Кровь из контура, возможно, лучше представляет периферическую кровь, чем кровь, расположенная в катетере; таким образом, положительный посев крови, полученной из магистрали, может отражать иной источник бактериемии, чем катетер. Европейские рекомендации предлагают учитывать эту возможность, проводя параллельно оценку анамнеза, результатов обследования, визуализации и результатов других лабораторных тестов, включая по возможности посев мочи.
2. Показания для немедленного удаления катетера. При наличии признаков септического тромбоза, эндокардита, остеомиелита или тяжелого сепсиса с гипотонией катетер следует удалять немедленно. Такие же рекомендации распространяются на туннельную инфекцию с лихорадкой. Диализ следует проводить на временном катетере, установленном в другом месте.
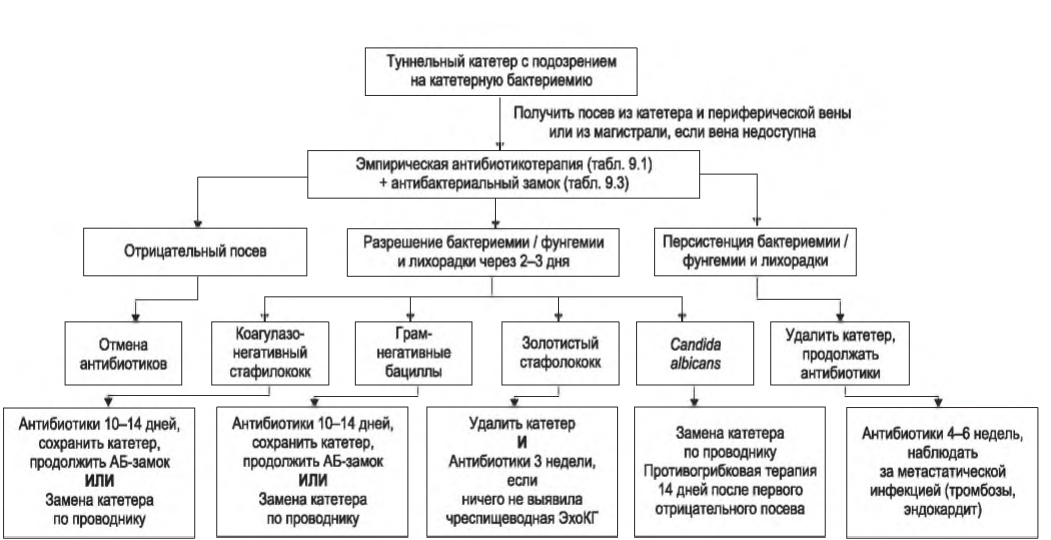
РИСУНОК 9.1. Алгоритм лечения туннельных катетеров для гемодиализа по рекомендациям Infectious Disease Society of America. Обновление 2009 года. Воспроизведено с разрешения из: Mermel LA, et al. Clinical practice guidelines for the diagnosis and management of intravascular catheter-related infection: 2009 update by the Infectious Diseases Society of America. Clin Infect Dis. 2009; 49:1-45
Таблица 9.1 Дозы антибиотиков для пациентов на гемодиализе

3. Выбор антибиотика. Наиболее типичными микроорганизмами являются стафилококки, хотя грамотрицательные микроорганизмы выявляются с частотой до 40% случаев. Терапию антибиотиками широкого спектра следует начинать немедленно после забора крови на посев. Диализный центр должен поддерживать базу данных всех случаев бактериемии, связанных с катетером, включая выявленные микроорганизмы, их чувствительность, ответ на терапию, поскольку эта информация исключительно ценна для выбора антибактериальной терапии в новых случаях. Если в местной диализной популяции распространены метициллин-резистентные стафилококки, в начальную терапию должен быть включен ванкомицин, а не цефалоспорины первого поколения. Адекватное покрытие грамнегативного спектра можно обеспечить аминогликозидами или цефалоспоринами третьего поколения. Аминогликозиды, однако, могут вызвать ототоксичность у 20% диализных пациентов. Если начата терапия, рассчитанная на метициллин-резистент-ный стафилококк, а посев выявил метициллин-чувствительный микроорганизм, следует сменить терапию на цефазолин или похожий антибиотик.
4. Доза антибиотиков. С практической точки зрения удобно пользоваться антибиотиками, уровень которых поддерживается во время междиализного интервала, благодаря чему их можно вводить в конце каждого сеанса диализа. Е1екоторые начальные дозы представлены в табл. 9.1 и 9.2 (из IDSA, Mermel, 2009). Однако эти дозы, возм ож но, потребуется увеличить у пациентов со значимой остаточной функцией почек и у тех, кто получает интенсивный диализ (часты й диализ), вы сокообъемную гемодиафильтрацию или продленные методы заместительной почечной терапии. По возм ож ности следует мониторировать преддиализный уровень антибиотика, но практически это доступно только в условиях стационара. Тактика дозирования антибиотиков у пациентов на гемодиализе и на продленных методах заместительной почечной терапии обсуж дена в деталях в главах 15 и 35. С реж имами дозирования можно такж е познакомиться в M erm el (2009).
Таблица 9.2 Особые аспекты ведения пациентов, получающих гемодиализ через катетеры, у которых подозревается или доказана связанная с катетером инфекция
Посевы крови и катетера Получать пробы крови для посевов следует из сосудов, которые не планируется использовать в дальнейшем для создания фистулы.
Если нельзя получить образец крови из периферической вены, его можно взять во время диализа из магистралей, соединенных с катетером.
У пациентов с подозрением на катетерную бактериемию, у которых были взяты посевы и начата антибактериальная терапия, антибиотики можно отменить, если все посевы оказались негативными и не выявлены другие источники инфекции.
Когда образец периферической крови получить нельзя, отсутствуют другие катетеры для взятия образца, отсутствуют отделяемое из места выхода катетера и клинические признаки альтернативного источника инфекции, тогда положительные результаты посева крови, полученной из катетера, требуют продолжения антибактериальной терапии из-за возможной катетерной бактериемии у пациентов с соответствующей симптоматикой.
Удаление катетера, замена его или сохранение (антибактериальными замками Инфицированный катетер у пациентов с катетерной бактериемией вследствие золотистого стафилококка, синегнойной палочки или грибов, должен быть удален, а временный (не туннельный) катетер установлен в другом анатомическом месте.
При абсолютном отсутствии иных мест для установки катетера можно провести замену катетера по проводнику.
Когда гемодиализный катетер удаляется из-за катетерной бактериемии, новый долговременный катетер можно устанавливать после получения отрицательных посевов крови.
При катетерной бактериемии из-за других микробов (например, грамотрицательных бацилл, кроме синегнойной палочки, или коагулазонегативных стафилококков) можно начинать стартовую эмпирическую внутривенную терапию антибиотиками без немедленного удаления катетера. Если симптомы персистируют и при наличии признаков метастатической инфекции, катетер следует удалить. Если симптомы (лихорадка, озноб, гемодинамическая нестабильность, нарушение ментального статуса) разрешаются через 2-3 дня экстренно начатой терапии антибиотиками и отсутствует метастатическая инфекция, инфицированный катетер можно заменить по проводнику на новый туннельный катетер. Альтернативно у пациентов без показаний к удалению катетера катетер можно сохранить, используя в качестве дополнительной терапии антибактериальный замок после каждого сеанса в течение 10-14 дней.
Антибактериальная терапия Эмпирическую антибактериальную терапию следует начинать с ванкомицина и препаратов, покрывающих грамотрицательные палочки с учетом местной чувствительности к антибиотикам (например, цефалоспорины 3-го поколения, карбапенем или комбинация бета-лактамных антибиотиков с защитой от лактамазы).
Пациентов, которые начали лечение с ванкомицина, после подтверждения у них катетерной бактериемии метициллинчувствительным золотистым стафилококком следует перевести на цефазолин. Для цефазолина используйте после сеанса дозу 20 мг/кг, округляя до ближайших 500 мг.
Курс антибиотиков увеличивается до 4-6 недель в случае резистентной бактериемии или фунгемии (72 часа после удаления катетера или у пациентов с эндокардитом или тромбофлебитом); 6-8-недельный курс следует применять у пациентов с остеомиелитом.
Диализные пациенты с катетерной инфекцией ванкомицин-резистентнымиэнтерококками могут лечиться или даптомицином 6 мг/кг после каждого сеанса или пероральным линезолидом 600 мл 2 раза в день.
Таблица 9.2 Особые аспекты ведения пациентов, получающих гемодиализ через катетеры, у которых подозревается или доказана связанная с катетером инфекция (окончание)
Антибактериальные замки
Антибактериальные замки показаны у пациентов с катетерной бактериемией, связанной с туннельными катетерами, при отсутствии признаков инфекции места выхода или туннельной, у которых ставится цель сохранить катетер.
Для этой цели антибактериальные замки не должны использоваться как единственный метод, а сочетаться с системной антибактериальной терапией с применением обоих режимов в течение 7-14 дней. Время установки раствора антибактериального замка не должно превышать 48 часов до следующей замены; для пациентов с бедренными катетерами предпочтительно инсталлировать новый раствор каждые 12 часов. Для пациентов на гемодиализе замки могут обновляться после каждой диализной сессии.
При катетерной бактериемии вследствие золотистого стафилококка или Candidasp. вместо антибактериальных замков рекомендуется удаление катетера, если не существует каких-либо чрезвычайных обстоятельств (например, отсутствие альтернативного места для введения катетера).
Для пациентов с положительными посевами из катетера с ростом коагулазонегативного стафилококка или грамнегативных бацилл при отрицательных посевах крови антибактериальные замки можно использовать без системной терапии.
Для ванкомицина концентрация в замке должна быть по меньшей мере в 1000 раз выше, чем подавляющая концентрация для данного микроорганизма.
В настоящее время недостаточно данных, чтобы рекомендовать спиртовые замки при катетерной бактериемии.
Последующие посевы
Нет необходимости подтверждать отрицательные результаты посева перед сменой катетера по проводнику у диализных пациентов с катетерной бактериемией, если отсутствует симптоматика.
Контрольные посевы следует выполнить через неделю после завершения курса антибиотиков, в случае если катетер сохранен. Если посевы окажутся положительными, катетер следует удалить, а новый перманентный катетер можно устанавливать после дополнительных посевов с отрицательными результатами.
Видоизменено из: Mermel LA, et al. Clinical practice guidelines for the diagnosis and management of intravascular catheter-related infection: 2009 update by the Infectious Diseases Society of America. Clin Infect Dis. 2009; 49:1-45.
5. Длительность курса. Курс антибиотиков следует остановить сразу, как только в посевах зафиксировано прекращение роста, а симптомы и признаки пациента указывают на отсутствие инфекции. В случае положительных посевов изначально выбранный режим следует скорректировать по получении анализа результатов чувствительности. В неосложненных случаях курс в 2-3 недели системного применения антибиотиков адекватен при связанной с катетером бактериемией. Более продолжительные курсы (4-8 недель) показаны при метастатической инфекции, такой как эндокардит и остеомиелит (рис. 9.1 или табл. 9.2).
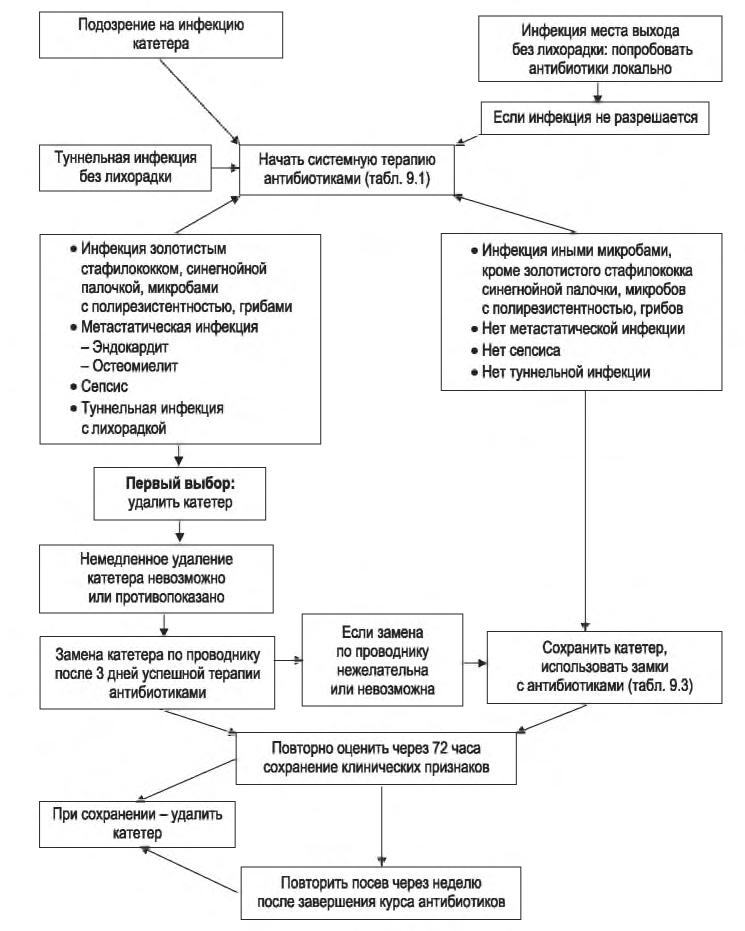
РИСУНОК 9.2. Алгоритм лечения туннельных катетеров для гемодиализа по Европейским рекомендациям по наилучшей клинической практике. Обновление 2010 года. Видоизменено с разрешения из: Vanholder R, et al. Catheter-related blood stream infections (CRBSI): a European view. Nephrol Dial Transplant. 2010; 25:1753-1756
6. Удаление катетера и замена по проводнику. С точки зрения лечения инфекции катетер лучше всего удалять независимо от вызвавшего инфекцию микроорганизма. Однако, поскольку пациент продолжает нуждаться в диализе, становится необходимой установка временного катетера. Таким образом, решение об удалении катетера следует индивидуализировать на основе тяжести сепсиса и доступности альтернативных мест для сосудистого доступа. Если у пациента клинически выражен сепсис, несмотря на системное применение антибиотиков, катетер следует удалять как можно быстрее. Попытки сохранять тот же катетер путем лечения инфекции были успешными менее чем в 30% случаев при наличии риска метастатической инфекции. Некоторые исследования, однако, поддерживают смену катетера по проводнику при разрешении симптоматики через 2-3 дня от начала антибактериальной терапии; сообщается о 70-80% случаев сохранения катетера. Таким образом, удаление инфицированного катетера (и предположительно биопленки, в которой могут сохраняться бактерии) и замена его новым катетером через то же самое место венотомии сохраняет венозный доступ с излечением от инфекции. Замену катетера по проводнику можно проводить только если симптомы быстро разрешаются за 2-3 дня начальной антибактериальной терапии и нет признаков метастатической инфекции.
а) Инфекция катетеров золотистым стафилококком, синегнойной палочкой или Candidasp.
В этих случаях предлагают удалять катетер, как только выявлена такая инфекция. Замена катетера по проводнику не рекомендуется, если нет непреодолимых обстоятельств.
7. Антибактериальные замки влечении инфекции катетера. Другим подходом в лечении пациентов с бактериемией, связанной с катетером, является введение замков с концентрированными антибиотиками в просвет катетера после каждого сеанса диализа в дополнение к системному применению антибиотиков (табл. 9.3). Антибактериальные замки используются только на протяжении системной антибиотикотерапии, которая затем меняется на стандартные гепариновые или цитратные замки. В 2/3 случаев антибактериальные замки успешно обеспечивают стерильность биопленки в катетере, тем самым позволяя успешно лечить бактериемию с сохранением инфицированного катетера. В оставшейся трети случаев сохраняется лихорадка и положительные посевы, что требует неотложной замены катетера. Протокол с антибактериальным замком наиболее успешен при катетерной бактериемии вследствие Staphylococcus epidermidis (75%) и грамотрицательных инфекциях (87%), и менее успешен при инфекции S. aureus (40%) (Allon, 2004; Poole, 2004), при которой он не рекомендуется. Значительное количество раствора, введенного в катетер, за 24 часа изливается (Sungur, 2007; Schilcher, 2014), поэтому концентрация антибиотика в замке должна быть существенно выше, чем минимально подавляющая рост концентрация. Обычно замки содержат также гепарин в количестве от 2500 до 5000 МЕ/мл или смешаны с 4% цитратом натрия. Состав некоторых часто используемых замков представлен в табл. 9.3.
8. Последующие посевы. Повторные посевы обычно проводятся через 72 часа лечения, в зависимости от состояния пациента. Важно также провести повторный п осев через одну неделю после заверш ения запланированного курса, чтобы убедиться в отсутствии возвратной инфекции.
Таблица 9.3 Некоторые принятые концентрации антибиотиков для замков

D. осложнения катетерной бактериемии. Отсрочка в терапии или продолжительные попытки сохранить инфицированный катетер могут привести к серьезным осложнениям: эндокардит, остеомиелит, гнойный тромбоф лебит и спинальный эпидуральный абсцесс. Последний является редким, но серьезным неврологическим осложнением у ГД-пациентов. В одной серии наблюдений 50% случаев эпидуральных абсцессов были связаны с попытками сохранить инфицированный перманентный катетер (Kovalik, 1996). Симптомами его являю тся лихорадка, боль в спине, локальное напряжение мыш ц, боль и слабость в ногах, нарушение функции сфинктеров, парезы или параличи. Для диагностики М ТР менее чувствительно, чем КТ-миелография. О бычное КТ-сканирование без миелографии низкочувствительно и м ож ет дать искаженные результаты (например, протрузия диска). Обычно рекомендуется раннее (немедленное) декомпрессионное хирургическое вмеш ательство, хотя редкие пациенты могут лечиться только антибиотиками.
Эндокардит следует подозревать у пациентов, у которых лихорадка и бактериемия сохраняются, несмотря на адекватную антибактериальную терапию и удаление катетера. Это осложнение наблюдается чаще всего при бактериемии Saureus. Признаками являются: развитие симптоматической сердечной недостаточности и новых шумов в сердце. Трансторакальная и/или чреспищеводная эхо-кардиография подтверждает наличие вегетации на клапанах и недостаточности клапанов.
E. Аспирин. Терапия аспирином связана с уменьшением частоты S. aureus-катетерной бактериемии (Sedlacek, 2007). Предшествующая терапия аспирином также связана с уменьшением симптом ов инфекции и размера вегетации на имплантируемых сердечно-сосудистых устройствах (Habib, 2013). Эти данные требуют подтверждения, и действующие рекомендации такую практику не поддерживают.
II. ДИСФУНКЦИЯ КАТЕТЕРА. Дисфункция катетера определяется как невозможность получить кровоток в 300 мл/мин при давлении перед насосом ниже чем -250 мм рт. ст. Проблемой является невозможность свободно получить кровь из просвета катетера и частые тревоги по давлению, которые не разрешаются при перемене пациентом положения или при промывании катетера.
А. Начальная дисфункция. Недавно установленные катетеры могут давать плохой кровоток из-за перегиба, сдавления катетера внутри туннеля отеком, неправильного положения катетера (в непарной или полунепарной вене) или неправильного расположения кончика катетера (рис. 9.3). Для диагностики полезна рентгенография. Отек в туннеле обычно разрешается за 24 часа. Наличие перегиба или неправильного расположения кончика катетера требует его перестановки с созданием другого туннеля или использования другой длины катетера. Важно также устанавливать катетер в нижней части шеи близко к ключице; высокое расположение катетера на шее может сделать катетер «позиционным», с кровотоком, зависящим от положения шеи. Фактически кончик катетера поднимается при наклоне шеи, приводя к плохому кровотоку. Место выхода близко к молочной железе может также тянуть кончик катетера вверх, в верхнюю полую вену. Экструзия муфты в результате перемещения катетера или эрозия тканей повышают риски дисфункции и инфекции. Такие катетеры требуют замены.
РИСУНОК 9.3. Перегиб: катетер в левой яремной вене с перегибом
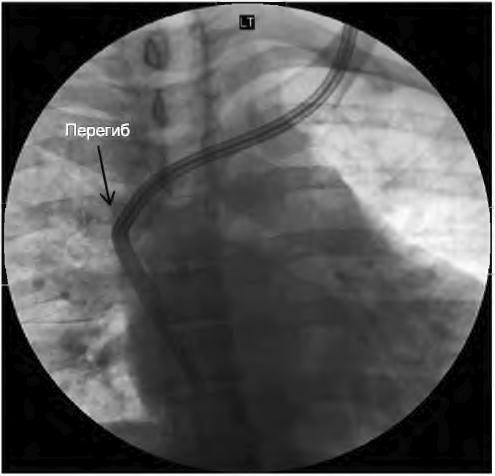
Если в туннеле есть эрозия или он инфицирован, требуется создание нового туннеля или новое место установки. Катетеры в левой яремной вене характеризуются большей частотой дисфункции, чем в правой (Engstrom, 2013), по не вполне понятным причинам, возможно, из-за извилистого пути до входа в правое предсердие.
1. Протокол с альтеплазой. Иногда ранняя дисфункция может быть обусловлена внутрикатетерным тромбозом. Введение на короткий (на 1 час) или продолжительный (на ночь) срок тканевого активатора плазминогена (tPA) обычно эффективно в лечении тромбоза просвета в краткосрочной перспективе, хотя долгосрочная выживаемость катетера не очень хороша. Описано несколько протоколов (Savader, 2001; Clase, 2001) (табл. 9.4). Короткие протоколы не обязательно работают лучше, чем протоколы с задержкой (Vercaigne, 2012). Для детального описания протоколов с альтеплазой см. ВС Renal Agency (2011).
В. Поздняя дисфункция. Поздние дисфункции обычно связаны с образованием фибринового футляра (рис. 9.4) или пристеночного тромба. Почти на всех катетерах, установленных в центральную вену, через 1-2 недели образуются фибриновые футляры. Вначале они клинически незначимы, пока не вызывают обструкцию на дистальном конце катетера. Обычно раствор легко вводится в порт, но забор затруднен, демонстрируя эффект клапана. Эти футляры могут служить очагом инфекции. Использование варфарина и других антикоагулянтов на постоянной основе не снижает вероятности образования футляров или формирования тромба в катетере (Mokrzycki, 2001).
Таблица 9.4 Дозирование тканевого активатора плазминогена (tPA) для окклюдированных катетеров

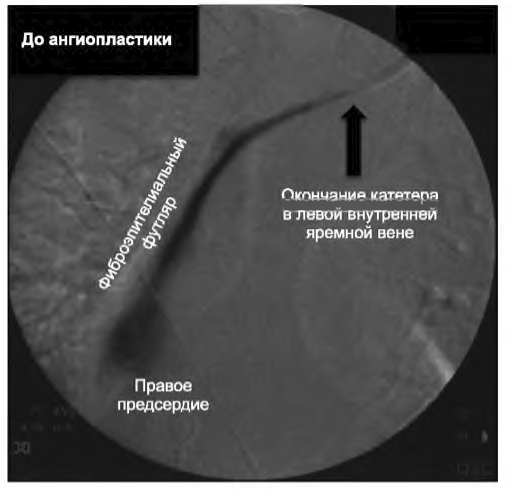
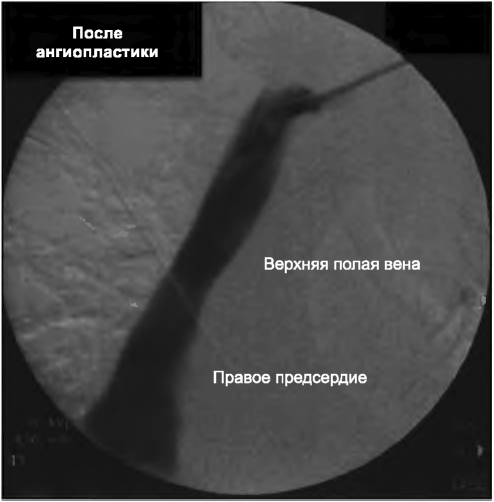
РИСУНОК 9.4. Фибриновый футляр: центральный венозный катетер в яремной вене с фибриновым футляром, распространяющимся за окончание катетера. На нижней ангиограмме катетер освобожден от футляра
1. Лечение. Наличие фибринового футляра обычно выявляется во время замены катетера при введении радиоконтраста через венозный порт старого катетера (рис. 9.4). Это состояние обычно исправляется при помощи введения катетера с баллоном для ангиопластики по проводнику через просвет катетера. Баллон вводится в просвет фибриновой оболочки и затем раздувается, чтобы разорвать ее. Диаметр баллона в 8 мм обычно достаточен, чтобы решить эту задачу. Разрыв оболочки подтверждается повторным введением радиоконтраста после установки нового катетера. Эта методика приводит к восстановлению кровотока по катетеру, достаточного для проведения диализа, в абсолютном большинстве случаев (Rasmussen, 2010; Shanaah, 2013).
С. Возвратная дисфункция катетера. Небольшая доля пациентов с дисфункцией катетера после проведения замены катетера и баллонной ангиопластики может продемонстрировать развитие повторной дисфункции катетера. Такие пациенты требуют неоднократной замены катетера (Rasmussen, 2010). Не существует идеального решения для этих пациентов. Использование антикоагулянтов в этих случаях не помогает, и лучшим решением является смена типа доступа, если это возможно.
III. ТРОМБОЗЫ
A. Тромбозы внутри просвета. Тромбозы катетеров обычно лечатся введением 1РА на 1 час или более. Некоторые часто используемые протоколы представлены в табл. 9.4. Механическое удаление тромба предложено, но не является популярным. Профилактическая терапия пероральными антикоагулянтами (вар-фарином) не улучшает проходимость катетера, если не достигаются высокие показатели МНО, а это может быть связано с кровотечениями. Более того, риск кальцифилаксии с кожными некрозами на терапии варфарином ограничивает его использование у диализных пациентов.
B. Тромбоз центральных вен или внутрисердечный тромбоз связаны с наличием больших длительно стоящих катетеров и в редких случаях могут привести к эмболическим осложнениям. Внутрипредсердный тромб требует продолжительной системной антикоагуляции (6 месяцев или более) с регулярной оценкой его состояния.
C. Эмболические осложнения. Большие тромбы, прикрепленные к кончику катетера или к стенке сосуда, могут клинически не проявляться до возникновения эмболических осложнений. Большие пристеночные тромбы могут привести к развитию стеноза и тромбоза центральных вен. Возможные варианты лечения при крупном тромбе или тромбе правого предсердия включают в себя только удаление катетера, системную или направленную на катетер фибринолитическую терапию и редко - торакотомию с тромбэктомией.
IV. ЦЕНТРАЛЬНЫЙ ВЕНОЗНЫЙ СТЕНОЗ
А. Причины. Центральный венозный стеноз происходит от повреждения эндотелия в месте контакта катетера с эндотелием путем освобождения большого количества факторов роста. Частота стенозов возрастает при использовании жестких несиликоновых катетеров, при использовании подключичных катетеров (предположительно из-за высокого углового стресса на катетере в подключичном положении) и у пациентов с предшествующими инфекциями, связанными с катетером. Факторы риска включают множественные установки катетеров в анамнезе (не исключая малые и большие венозные катетеры и периферически установленные центральные катетеры), а также длительное время их использования. Обычно развиваются коллатеральные сосуды, но они не обеспечивают адекватного оттока, чтобы уменьшить отек конечности.
В. Проявления и диагноз. Стеноз или окклюзия подключичной, плечеголовной или верхней полой вены обычно проявляется венозной гипертензией (отеком груди, плеча, шеи и лица) или дисфункцией сосудистого доступа (высокое венозное давление на диализе, неадекватный диализ, продолжительное кровотечение). Стеноз может быть бессимптомным, пока не раскрывается созданием AV-фистулы. В результате может произойти тромбоз доступа. Окклюзия нескольких центральных вен в грудной клетке может привести к развитию синдрома верхней полой вены. Тщательный сбор анамнеза и обследование часто выявляют рубцы от множественных установок центрального венозного катетера. Кроме того, может присутствовать имплантированный водитель ритма. Множественные коллатеральные вены видны при обследовании.
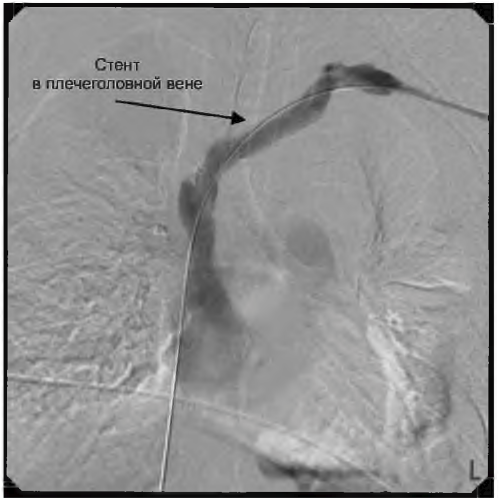
РИСУНОК 9.5. Стент в центральной вене: окклюзия плечеголовной вены, скорректированная ангиопластикой со стентированием
С. Лечение. Перевязка сосудистого доступа обеспечивает наиболее быстрое улучшение, но жертвует сосудистым доступом. Терапия антикоагулянтами (гепарин с переходом на варфарин) и возвышенное положение руки на вовлеченной стороне облегчают симптомы и признаки, если присутствует тромбоз. Обычно требуется более энергичное вмешательство; при стенозе использовалась баллонная ангиопластика, но патология имеет тенденцию к рецидиву. Установка стента в комбинации с ангиопластикой (рис. 9.5) показана при эластичных центральных венах (легко растяжимых) или если произведенная дилатация стеноза рецидивировала в течение трех месяцев. Однако установка стента редко разрешает проблему в долгосрочной перспективе, поскольку стеноз развивается повторно вокруг стента. Стеноз подключичной вены иногда можно разрешить созданием анастомоза из аксилярной вены во внутреннюю яремную.
V. АДГЕЗИЯ КАТЕТЕРА. При долговременном существовании катетер может прикрепиться спайками к эндотелию вены или предсердия. Адгезию можно заподозрить, когда попытки удалить катетер вызывают сильную боль или требуют значительных усилий. Сердце или средостение могут смещаться при визуализации флюороскопией. Удаление такого катетера сложное и может потребовать инвазивных вмешательств, включая рассечение лазером или открытую хирургию. Недавно были предложены новые закрытые методики (Hong, 2011).
VI. ПОВРЕЖДЕНИЕ ПОРТА И ЗАЖИМА. Можно нередко видеть поврежденный порт или зажимы на туннельном катетере. Это приводит к подсасыванию воздуха или невозможности надежно закрыть катетер с риском кровотечения (Amin, 2011). Нередко эти части катетера можно заменить, используя специальные наборы для конкретного катетера, что не требует замены всего катетера. При наличии излома на порте с подсасыванием воздуха возрастает риск инфекции, и при ремонте катетера следует использовать профилактически антибиотики после получения результатов посевов.
Ссылки и рекомендуемая литература
Abad CL, Pulia MS, Safdar N. Does the nose know? An update on MRSA decolonization strategies. Curr Infect Dis Rep. 2013; 15:455-464.
Allon M. Dialysis catheter-related bacteremia: Treatment and prophylaxis. Am/Kidney Dis. 2004; 44:779-791. Amin P, et al. Broken clamp on a cuffed tunneled catheter - are all catheters equal? Semin Dial. 2011; 24: 104-106.
Asif A, et al. Transvenous cardiac implantable electronic devices and hemodialysis catheters: recommendations to curtail a potentially lethal combination. Semin Dial. 2012; 25: 582-586.
BC Renal Agency. Alteplase use for occluded hemodialysis catheters. Vascular Access Guideline. Approved July 24, 2006; Updated March 4, 2011. http://www.bcrenalagency.ca/sites/default/files/documents/files/Use-of-Alteplase-FINALMarch-4-2011.pdf. Accessed May 26, 2014.
Clase CM, et al. Thrombolysis for restoration of patency to haemodialysis central venous catheters: a systematic review. J Thrornb Thrombolysis. 2001; 11: 127-136.
Dotson B, et al. Physical compatibility of 4% sodium citrate with selected antimicrobial agents. Aw /Health Syst Pharm. 2010; 67: 1195-1198.
Engstrom BI, et al. Tunneled internal jugular hemodialysis catheters: impact of laterality and tip position on catheter dysfunction and infection rates. J Vase Interv Radiol. 2013; 24: 1295-1302.
Habib A, et al; for the Mayo Cardiovascular Infections Study Group. Impact of prior aspirin therapy on clinical manifestations of cardiovascular implantable electronic device infections. Europace. 2013; 15: 227-235.
Hickson LJ, et al. Clinical presentation and outcomes of cardiovascular implantable electronic device infections in hemodialysis patients. Aw /Kidney Dis. 2014; 64: 104-110.
Hong JH. A breakthrough technique for the removal of a hemodialysis catheter stuck in the central vein: endoluminal balloon dilatation of the stuck catheter. J Vase Access. 2011; 12: 381-384.
Hwang HS, et al. Comparison of the palindrome vs. step-tip tunneled hemodialysis catheter: a prospective randomized trial. Semin Dial. 2012; 25: 587-591.
Joshi AJ, Hart PD. Antibiotic catheter locks in the treatment of tunneled hemodialysis catheter-related blood stream infection. Semin Dial. 2013; 26: 223-226.
Kovalik EC, et al. A clustering of epidural abscesses in chronic hemodialysis patients: risks of salvaging access catheters in cases of infection. J Am Soc Nephrol. 1996; 7: 2264-2267.
LokCE, et al. Trisodium citrate 4% - an alternative to heparin capping of haemodialysis catheters. Nephrol Dial Transplant. 2007; 22: 477-483.
Mandolfo S, et al. Hemodialysis tunneled central venous catheters: five-year outcome analysis. J Vase Access. 2014 Apr 25. doi: 10.530l/jva.5000236.
Maya ID, et al. Does the heparin lock concentration affect hemodialysis catheter patency? Clin J Am Soc Nephrol. 2010; 5: 1458-1462.
Mermel LA, et al. Clinical practice guidelines for the diagnosis and management of intravascular catheter-related infection: 2009 update by the Infectious Diseases Society of America. Clin Infect Dis. 2009; 49:1-45.
Mokrzycki MH, et al. A randomized trial of minidose warfarin for the prevention of late malfunction in tunneled, cuffed hemodialysis catheters. Kidney Int. 2001; 59: 1935-1942.
Poole CV, et al. Treatment of catheter-related bacteremia with an antibiotic lock protocol: effect of bacterial pathogen. Nephrol Dial Transplant. 2004; 19: 1237-1244.
Quaretti P, et al. A refinement of Hongs technique for the removal of stuck dialysis catheters: an easy solution to a complex problem. I Vase Access. 2014; 15: 183-188.
Rasmussen RL. The catheter-challenged patient and the need to recognize the recurrently dysfunctional tunneled dialysis catheter. Semin Dial. 2010; 23: 648-652.
Sabry AA, et al. The level of C-reactive protein in chronic hemodialysis patients: a comparative study between patients with noninfected catheters and arteriovenous fistula in two large Gulf hemodialysis centers. Hemodial Int. 2014; 18: 674-679.
Savader SJ, et al. Treatment of hemodialysis catheter-associated fibrin sheaths by rt-PA infusion: critical analysis of 124 procedures. J Vase Interv Radiol. 2001; 12:711-715.
Schiller B, et al. Spurious hyperphosphatemia in patients on hemodialysis with catheters. Am I Kidney Dis. 2008;52:617-620.
Schilcher G, et al. Loss of antimicrobial effect of trisodium citrate due to ‘lock’ spillage from haemodialysis catheters. Nephrol Dial Transplant. 2014; 29: 914-919.
Sedlacek M, et al. Aspirin treatment is associated with a significantly decreased risk of Staphylococcus aureus bacteremia in hemodialysis patients with tunneled catheters. Aw I Kidney Dis. 2007; 49: 401-408.
Shanaah A, Brier M, Dwyer A. Fibrin sheath and its relation to subsequent events after tunneled dialysis catheter exchange. Semin Dial. 2013; 26: 733-737.
Sungur M, et al. Exit of catheter lock solutions from double lumen acute haemodialysis catheters - an in vitro study. Nephrol Dial Transplant. 2007; 22: 3533-3537.
Tordoir J, et al. EBPG on Vascular Access. Nephrol Dial Transplant. 2007; 22 Suppl 2: ii88—117.
Vanholder R, et al. Catheter-related blood stream infections (CRBSI): a European view. Nephrol Dial Transplant. 2010; 25:1753-1756.
Vercaigne LM, et al. Alteplase for blood flow restoration in hemodialysis catheters: a multicenter, randomized, prospective study comparing «dwell» versus «push» administration. Clin Nephrol. 2012; 78: 287-296.
Wang AY, et al. Anticoagulant therapies for the prevention of intravascular catheters malfunction in patients undergoing haemodialysis: systematic review and meta-analysis of randomized, controlled trials. Nephrol Dial Transplant. 2013; 28: 2875-2888.
Yaseen O, et al. Comparison of alteplase (tissue plasminogen activator) high-dose vs. low-dose protocol in restoring hemodialysis catheter function: the ALTE-DOSE study. Hemodial Int. 2013; 17: 434-440.
