- Диализному врачу
- 1. Ведение пациентов с ХБП 4-5-й стадии.
- 2. Подготовка к трансплантации, диализу или к консервативной терапии
- 3. Физиологические принципы и моделирование кинетики мочевины
- 4. Оборудование для гемодиализа и расходные материалы
- 5. Вода для диализа и диализирующий раствор
- 6. Артериовенозные фистулы и протезы. Основные положения
- 7. Центральный венозный катетер в качестве доступа: основы
- 8. Мониторинг артериовенозного доступа и осложнений
- 9. Инфекции и другие осложнения центральных венозных катетеров
- 10. Назначение острого гемодиализа
- 11. Назначение хронического гемодиализа
- 12. Осложнения в ходе процедуры гемодиализа
- 13. Повторное использование диализаторов
- 14. Антикоагуляция
- 15. Продленная заместительная почечная терапия
- 16. Гемодиафильтрация
- 17. Терапевтический аферез
- 18. Актуальность сорбционных технологий сегодня
- 19. Руководство по диализу
Продленная заместительная почечная терапия
Чаще всего из продленных1 процедур ЗПТ (CRRT20 21) у пациентов в критических состояниях применяются продленный гемодиализ и продленная гемодиафильтрация. Кроме них популярны еще два метода пролонгированной интермиттирующей ЗПТ (PIRRT22): длительный низкоэффективный гемодиализ и длительная низкоэффективная гемодиафильтрация. Продленная гемофильтрация и медленная продленная ультрафильтрация также применяются, но гораздо реже.
I. НОМЕНКЛАТУРА И ТЕРМИНОЛОГИЯ. В данной книге для продленного гемодиализа применяется сокращение С-HD, какой бы тип сосудистого доступа (артериовенозный -AV или вено-венозный - VV) ни использовался; продленная гемофильтрация обозначается С-HF; а комбинация этих двух процедур - продленная гемодиафильтрация - обозначается C-HDF. Раньше после этих аббревиатур ставились еще буквы AV или VV, обозначающие тип сосудистого доступа, так что для гемодиализа они выглядели как CAVHD или CVVHD, для гемофильтрации - как CAVH или CVVH, и для гемодиафильтрации - как CAVHDF или CVVHDF. Но сегодня в большинстве процедур используется доступ на основе центральных венозных катетеров, поэтому добавление букв VV в аббревиатуры стало излишним. Медленная продленная ультрафильтрация обозначается как SCUF23, а длительный низкоэффективный гемодиализ и длительная низкоэффективная гемодиафильтрация -SLED24 и SLED-F соответственно. SLED и SLED-F относятся к пролонгированной интермиттирующей ЗПТ (PIRRT). Стандартный интермиттирующий гемодиализ обозначается аббревиатурой IHD или более общим понятием - IRRT25 (интермиттирующая заместительная почечная терапия), поскольку такая терапия не всегда является только гемодиализом.
А. Различия между С-HD, С-HF и GHDF. В каждой из этих процедур используется медленная постоянная перфузия крови из артериального или венозного доступа через фильтр. В табл. 15.1 приводится сравнение данных техник.
Таблица 15.1 Сравнение техник CRRT
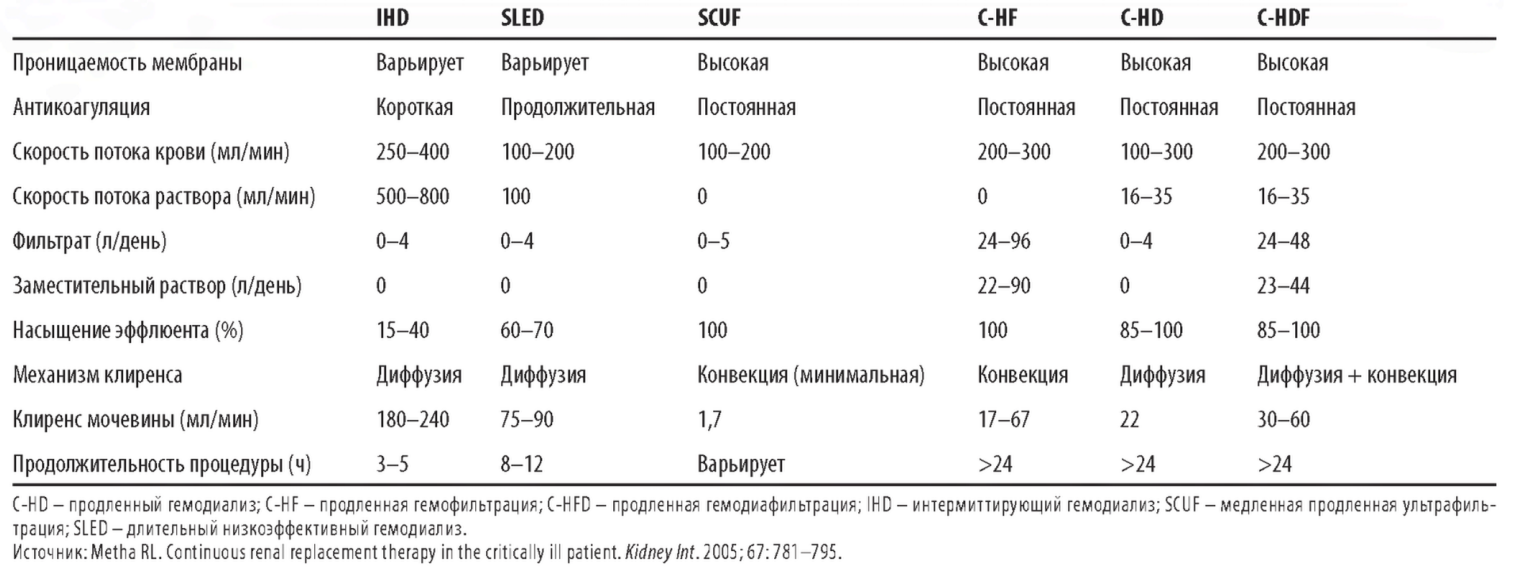
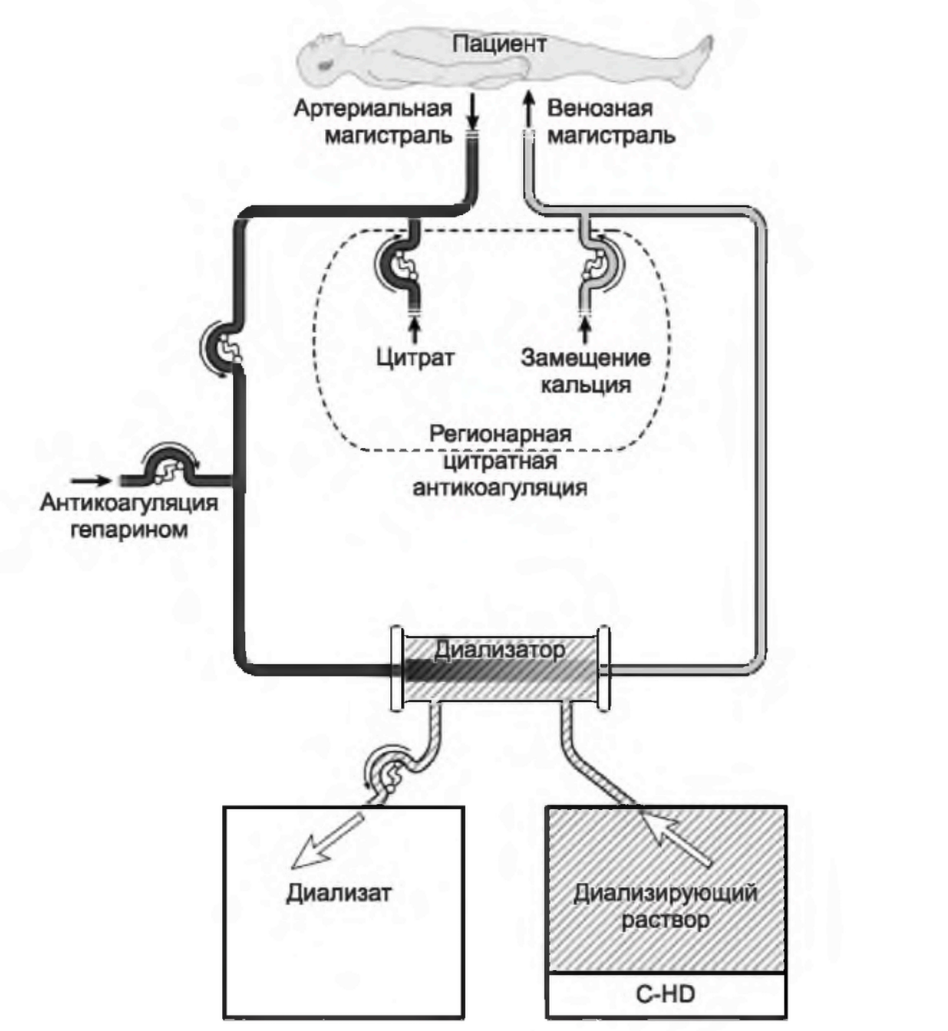
1. Продленный (непрерывный) гемодиализ (С-HD). При использовании данного метода (рис. 15.1) диализирующий раствор непрерывно, с малой скоростью проходит через соответствующий отсек диализатора. При С-HD растворенные в плазме вещества выводятся из нее преимущественно за счет диффузии. Объем ультрафильтрации, как правило, небольшой (3-6 л в день) и обычно ограничивается излишком жидкости в организме, подлежащим выведению.
2. Продленная гемофильтрация (С-НF). В данной технике (рис. 15.2) диализирующий раствор не используется. Вместо этого на входе или выходе гемофильтра производится инфузия большого объема (25-50 л в день) замещающего раствора (режимы предилюции и постдилюции соответственно). При С-HF объем ультрафильтрации равен сумме объемов замещающего раствора и излишков удаляемой из организма жидкости, поэтому он гораздо больше, чем при C-HD.
РИСУНОК 15.1. Типичный контур для проведения продленного гемодиализа. Проиллюстрировано применение гепаринизации либо регионарной цитратной антикоагуляции. При медленной продленной ультрафильтрации контур тот же, но диализирующий раствор не используется
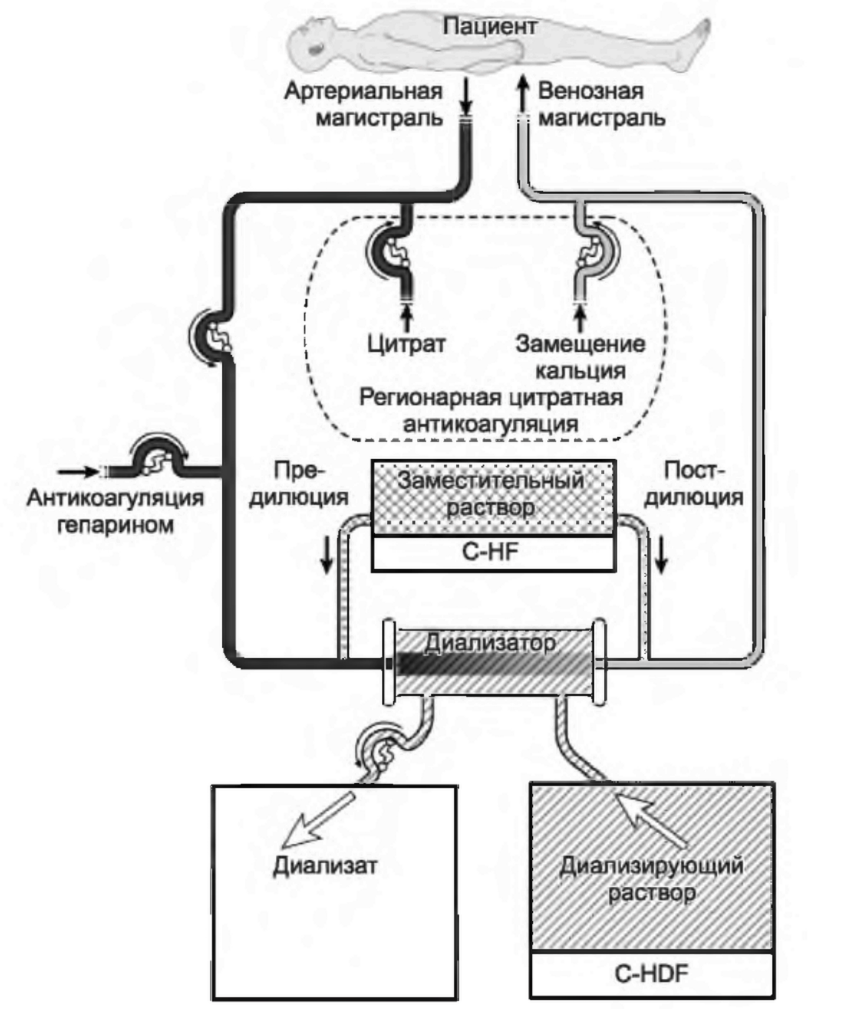
3. Продленная гемодиафильтрация (С-HDF). По сути, это комбинация С-HD и C-HF (рис. 15.2). Диализирующий раствор используется, но замещающий раствор также подается либо в артериальную, либо в венозную часть экстракорпорального контура. Дневной объем ультрафильтрации равен сумме использованного замещающего раствора и удаленной из организма жидкости. Обычно объем замещающего раствора при С-HDF примерно равен половине объема, используемого при С-HF, однако совокупный объем диализата («отработанной» жидкости) при C-HDF, то есть суммы замещающего и диализирующего растворов плюс удаленной из организма жидкости, близок к объему ультрафильтрата при С-HF, который складывается только из замещающего раствора и удаленной из организма жидкости.
РИСУНОК 15.2. Типичный контур для проведения продленной гемофильтрации (CHF) и продленной гемодиафильтрации (С-HDF), где заместительный раствор может подаваться в режиме предилюции или постдилюции, либо с использованием обоих режимов одновременно. При С-HDF гемодиализ применяется одновременно с С-HF. Проиллюстрировано применение гепаринизации либо регионарной цитратной анти коагуляции
4. Медленная продленная ультрафильтрация (SCUF). Контур для SCUF похож на те, что применяются при C-FFD и C-FFF, однако не используется ни замещающий, ни диализирующий раствор. Дневной объем ультрафильтрации небольшой -примерно, как при C-FFD, то есть 3-6 л.
В. Длительный низкоэффективный гемодиализ и длительная низкоэффективная гемодиафильтрация (SLED и SLED-F). SLED - это разновидность IHD с длительной (6-10 часов) процедурой и малыми скоростями потоков крови и диализирующего раствора. Обычно скорость потока крови (BFR) около 200 мл/мин, а диализирующего раствора - 100-300 мл/мин. Для данной техники могут применяться стандартные аппараты для гемодиализа, если они способны обеспечивать малые скорости потоков крови и диализирующего раствора, для этого в некоторых машинах потребуется обновление программного обеспечения. Один и тот же диализный аппарат, используемый днем для стандартного гемодиализа, ночью можно использовать для SLED, и диализных медсестер несложно обучить методике SLED, что дает экономию на тренингах. SLED позволяет предоставлять диализ с преимуществами CRRT в тех учреждениях, где есть хронический гемодиализ, но при этом нет оборудования и персонала для проведения CRRT. При SLED-F потребуется дополнительная инфузия замещающего раствора, если в диализном аппарате не предусмотрена функция ГДФ-онлайн (Marshall, 2004).
II. ПОКАЗАНИЯ ДЛЯ CRRT В СРАВНЕНИИ С IRRT. Потенциальные преимущества различных методов CRRT, а также SLED приведены в табл. 15.2. Среди них более низкая скорость удаления жидкости, а также лучший контроль азотемии по сравнению со стандартным IHD. Несмотря на, казалось бы, очевидные преимущества продленных процедур, несколько рандомизированных исследований не предоставили никаких доказательств, что применение CRRT при острой почечной недостаточности улучшает выживаемость по сравнению с IHD (Rabindranath, 2007). Однако в большинстве исследований пациенты в критическом состоянии не подвергались обычному IHD. Рекомендации KDIGO 2012 г., касающиеся лечения острого повреждения почек (AKI7), предлагают (с уровнем доказательности 2В) использовать CRRT вместо стандартной IRRT для гемодинамически не стабильных пациентов, а также предлагают применять CRRT для лечения AKI у пациентов с острым повреждением мозга или других причин повышения внутричерепного давления или генерализованного отека мозга (KDIGO АКТ 2012). Впрочем, в данных рекомендациях оговаривается, что использование пролонгированных IRRT процедур, таких как SLED или SLED-F, может быть не менее эффективным при лечении гемодинамически не стабильных пациентов, чем CRRT, однако указывается на недостаточное количество исследований, сравнивающих CRRT с продолжительными IRRT процедурами. В некоторых из ранних сравнительных исследований (Van Berendoncks, 2010; Marshall 2011) авторы полагают, что результаты пролонгированных IRRT процедур схожи с результатами CRRT, и при этом достигается существенная экономия затрат.
III. ЗАТРАТЫ НА ОБОРУДОВАНИЕ И ОБУЧЕНИЕ ПЕРСОНАЛА. Применение продленных процедур требует от медицинских сестер в отделениях интенсивной терапии знания техники их проведения. В отделениях, где высока текучесть кадров и где продленные процедуры проводятся нечасто, более подходящим может быть применение интермиттирующих методов, таких как SLED. Однако в тех медучреждениях, где помощь оказывается в больших объемах и продленная терапия входит в стандартный перечень диализных процедур, их проведение может помочь в решении задач по контролю жидкости, удалению токсинов и обеспечению питания у наиболее тяжелых пациентов.
Таблица 15.2 Потенциальные преимущества продленных процедур

IV. РАЗЛИЧИЯ В КЛИРЕНСЕ МОЛЕКУЛ С МАЛОЙ И БОЛЬШОЙ МОЛЕКУЛЯРНОЙ МАССОЙ МЕЖДУ C-HD, С НГ И C-HDF
А. Клиренс растворенных в крови веществ при С-HD. При С-HD, когда скорость кровотока (QB) 50-200 мл/мин или больше, а скорость потока диализирующего раствора (QD) обычно 25-30 мл/мин, клиренс мочевины и других молекул с малой молекулярной массой определяется главным образом QD. Как правило, QB при С-HD должна быть, как минимум, в три раза больше QD. При такой малой QB и таком высоком соотношении QB к QD диализат на выходе из диализатора оказывается почти на 100% насыщенным мочевиной и другими веществами с малой молекулярной массой. Клиренс мочевины, таким образом, определяется объемом ультрафильтрата, складывающимся из объема диализирующего раствора и объема выводимой из организма жидкости.
Стандартный QD на входе в диализатор равен 20-25 мл/кг в час, что соответствует 23-29 мл/мин для человека весом 70 кг. Если для примера взять QD в 26 мл/мин, то при его стопроцентном насыщении это будет соответствовать клиренсу мочевины в 26 мл/мин и расходу раствора около 37 л в день. Если прибавить к этому объему 3 л выводимых за день излишков жидкости, мы получим дневной объем УФ и клиренс мочевины 37 + 3 = 40 л. В терминах кинетики мочевины эти 40 л соответствуют уже знакомому нам параметру К х 1. Для пациента с объемом распределения мочевины 40 л приведенное выше назначение будет соответствовать Kt/V = 40/40 = 1,0, или около 7,0 в неделю. Это значительно больше эквивалентного недельного Kt/V по мочевине, равного примерно 2,7
AKI-acute kidney injury при стандартном трехразовом интермиттирующем гемодиализе - IHD (расчет эквивалентного недельного Kt/V по мочевине приведен в главе 3).
В. Клиренс растворенных веществ приС-HF. Принцип очищения крови при С-HF базируется исключительно на конвекции. При прохождении крови через гемофильтр градиент трансмембранного давления между пространством крови и ультрафильтратом заставляет воду из плазмы крови фильтроваться через высокопроницаемую мембрану. Проходя через мембрану, вода вымывает и увлекает с собой малые (не связанные с белками) и большие (если позволяет размер пор мембраны) молекулы, тем самым обеспечивая их удаление из крови. Удаленный ультрафильтрат замещается сбалансированным раствором электролитов, который подается либо во входящую магистраль гемофильтра (предилюция), либо в отводящую (постдилюция). Обычно инфузия замещающего раствора производится со скоростью примерно 20-25 мл/кг в час. Если используется постдилюция, «дренирующая жидкость» из гемофильтра почти на 100% насыщена мочевиной.
1. Фильтруемая фракция плазмы. Это часть удаленной плазмы, прошедшей через гемофильтр. Она может быть вычислена делением скорости ультрафильтрации на скорость потока плазмы, которая равна скорости кровотока (QB) х (1 - Het), где Het - гематокрит. Например, если QB = 150 мл/мин, a Het = 33%, то скорость потока плазмы будет 0,67 х 150 = 100 мл/мин. Если скорость ультрафильтрации 25 мл/мин, то фильтруемая фракция равна 25/97, то есть 25%. По эмпирическим правилам, фильтруемую фракцию плазмы следует поддерживать на уровне 25% или ниже, во избежание гемоконцентрации, скопления эритроцитов и белков плазмы в гемофильтре. Из-за такой чрезмерной концентрации засоряются поры мембраны, что, в свою очередь, может повлиять на эффективность УФ, снизить коэффициент просеивания, а также спровоцировать тромбообразование. Если в режиме постдилюции требуется высокая скорость подачи замещающего раствора, во избежание гемоконцентрации и поддержания фильтруемой фракции на уровне ниже 25%, необходимо увеличить скорость кровотока (QB) выше обычных 150 мл/мин.
2. Режим предилюции. Другой способ поддержания низкого уровня фильтруемой фракции плазмы - использование режима предилюции. В этом режиме концентрация мочевины в ультрафильтрате несколько меньше (обычно 80-90% от ее уровня в плазме), однако он позволяет повысить скорость потока замещающего раствора, увеличивая общий клиренс молекул со средней молекулярной массой. Рекомендуется использовать предилюцию в случаях, когда запланированный объем УФ составляет более 25 л в день. Предилюция также проводится, если исходная вязкость крови несколько повышена (например, при гематокрите >35%). Некоторые специалисты рекомендуют комбинацию пре- и постдилюции.
3. Расчет дилюционного эффекта в режиме предилюции. В качестве примера предположим, что скорость потока замещающего раствора 25 мл/мин, a QB - 150 мл/ мин. Доля растворенных в крови веществ, подлежащих удалению, на входе в гемофильтр будет равна 25/(150 + 25) = 14%. Если предположить также, что в день расходуется 35 л замещающего раствора и выводится 5 л излишков жидкости, то дневной объем УФ будет около 40 л. В режиме постдилюции (К х t) будет 40 л. А в режиме предилюции (К х t) будет примерно на 15% меньше, то есть 34 л, и поэтому, предположив, что V = 40 л, ежедневный индекс Kt/V при С-HF будет примерно 40/40 = 1,0 (при постдилюции) или 34/40 = 0,85 (при предилюции).
С Клиренс мочевины при C-HDF. При C-HDF сумма скорости потока диализирующего раствора, скорости инфузии замещающего раствора, а также скорости удаления излишков жидкости, как правило, устанавливается на уровне скорости потока диализата на выходе из фильтра при С-HD или при C-HDF в режиме постдилюции. Расчеты клиренса аналогичны приведенным выше. Клиренс малых молекул при C-HDF примерно тот же, что и при С-HD и С-HF, если дневные объемы УФ имеют сравнимые значения.
D. Сравнение клиренса молекул с малой и средней молекулярной массой при С-HF и С-HD. При С-HD оттекающий диализат не сильно насыщен веществами с большей молекулярной массой, поскольку они имеют меньшую скорость диффузии в растворе и меньшую скорость переноса через диализную мембрану. При С-HF, напротив, ультрафильтрат плазмы почти полностью насыщен веществами как с низкой, так и со средней молекулярной массой, поскольку скорость выведения данных веществ конвекцией из плазмы примерно одинаковая. Таким образом, С-HF более эффективна, чем С-HD, в плане выведения токсинов с большей молекулярной массой, включая пептиды, некоторые антибиотики и витамин В12. Использование теоретических преимуществ С-HF является довольно сложно технически реализовать на практике, поскольку требует объема ультрафильтрации >25 л у пациентов, которым невозможно обеспечить высокий QB для предотвращения гемоконцентрации. Также при высоких скоростях потока замещающего раствора очень сложно поддерживать водный баланс. При больших объемах С-HF любое уменьшение QB приводит к временному повышению гемоконцентрации в фильтре, увеличивающей риск тромбообразования. С другой стороны, С-HD легко осуществим при расходе диализирующего раствора 50 л в день. По этой причине С-HD становится более популярной терапией в рутинной практике, ну а если требуется увеличить выведение средних молекул, дополнительно используется замещающий раствор (C-HDF).
1. Площадь поверхности мембраны и клиренс веществ с молекулярной массой выше средней:
В одном исследовании in vitro клиренса таких молекул при С-HF по сравнению с С-HD на двух мембранах разной площади (0,4 и 2 м2) были получены парадоксальные результаты: при большей площади мембраны данный клиренс был схожим для С-HD и С-HF, а при меньшей площади мембраны он был хуже для С-HF, чем для C-HD (Messer, 2009). Было высказано предположение, что в режиме С-HF загрязнение компонентами белка сильнее повлияло на производительность мембраны меньшей площади. Данные результаты демонстрируют, что высокие скорости подачи замещающего раствора при небольшом размере гемофильтра могут быть малоэффективны для увеличения клиренса молекул с массой выше средних.
V. СОСУДИСТЫЙ ДОСТУП
А. Вено-венозный сосудистый доступ. Доступ получают установкой двухпросветного катетера в крупную (внутреннюю яремную или бедренную) центральную вену. Подключичная вена также может быть использована, но в качестве запасного варианта - см. главу 7. Клинические рекомендации KDIGO AKI 2012 г. рекомендуют для CRRT применение венозных катетеров без манжеты (5.4.1), при очень слабом уровне доказательности (2D). Рекомендации основаны на относительной простоте установки временного катетера без манжеты и на том, что технически более сложная установка манжеточного катетера может задержать начало лечения, а средняя продолжительность терапии CRRT составляет всего 12-13 дней (KDIGO, 2012). В одном из исследований (Morgan, 2012) сравнивалось применение при CRRT длинных (20-24 см) временных мягких силиконовых катетеров, кончик которых располагался вблизи правого предсердия, и коротких (15-20 см) катетеров с расположением кончика в верхней полой вене. Использование длинных катетеров приводило к увеличению срока функционирования гемофильтра и достижению большей дозы лечения. В другом исследовании оценивали успешность проведения CRRT с использованием бедренного сосудистого доступа, при этом средний срок службы фильтра составил 15 часов, если катетер устанавливался справа, и 10 часов при установке в левую бедренную вену (Kim, 2011). Механизм более успешной правосторонней установки катетера остается неясным.
B. Артериовенозный сосудистый доступ. При установке катетера в крупную артерию, обычно в бедренную, появляется возможность перфузии крови через экстракорпоральный контур за счет собственного артериального давления пациента вместо насоса. Возврат крови производится через любую крупную вену. Использование AV-доступа для CRRT больше широко не практикуется. Существует риск повреждения бедренной артерии с возможной дистальной ишемией конечности; к тому же AV-доступ зачастую не может обеспечить достаточный кровоток, необходимый для проведения практикуемых сегодня интенсивных CRRT-процедур. Однако CRRT с использованием AV-доступа может быть жизнеспасающим методом при массовых стихийных бедствиях (например, при землетрясениях, с развитием повреждения почек вследствие травматического рабдомиолиза), когда источники электроснабжения не надежны, поскольку кровоток обеспечивается за счет артериального давления пациента, а ультрафильтрация происходит благодаря гравитации (либо с помощью зажимов) и регулируется высотой расположения емкости для сбора фильтрата. Детальное описание CRRT с использованием AV-доступа можно найти в третьем издании нашего руководства.
C. Замена катетеров: плановая или диктуемая клиническими показаниям. CRRT-катетеры следует заменять только при наличии клинических показаний; не следует менять катетеры в соответствии с неким заранее предопределенным графиком в надежде минимизировать частоту катетерного сепсиса. Практика рутинной, плановой замены катетеров, бывшая когда-то популярной, теперь не рекомендуется центрами по контролю за распространением и профилактикой заболеваний (CDC), и ее целесообразность не подтверждается исследованиями.
VI. ВЫБОР ФИЛЬТРОВ ДЛЯ CRRT. В данной главе термины «гемофильтр» и «диализатор» используются взаимозаменяемо. Гемофильтры имеют только один вход на корпусе, что делает невозможным использование диализирующего раствора. У диализаторов есть второй порт. Диализаторы, применяемые для CRRT, должны иметь хорошую гидравлическую проницаемость для воды, поэтому они, скорее всего, будут из категории high-flux. Некоторые из ранних фильтров, разработанных главным образом для С-HF, имели отличную гидравлическую проницаемость и конвекционный клиренс, но плохой диффузионный клиренс при С-HD, к тому же в этих фильтрах был плохо оптимизирован контакт диализирующего раствора и всех волокон мембраны. В настоящее время фильтры для CRRT обеспечивают быстрое выравнивание концентраций мочевины между пространствами крови и диализирующего раствора, что делает их подходящими как для С-HF, так и для C-HD.
А. Размер фильтра и площадь поверхности. Размер гемофильтра должен учитывать используемую скорость кровотока (QB). Когда большой фильтр применяется при малой QB, повышается риск тромбообразования, поскольку такие фильтры рассчитаны на гораздо больший кровоток. Скорость потока крови через единичный капилляр (полое волокно) фильтра будет медленной. Кроме того, для больших диализаторов, рассчитанных на высокие скорости потока диализата, диализирующий раствор может неоптимально распределяться внутри пучка полых волокон. С другой стороны, большие диализаторы могут использоваться с большими QB, как, например, в протоколах высокоэффективного SLED - с целью достижения максимального клиренса средних молекул. Исследование Messer и соавт. (2009), упомянутое ранее, также предлагает использование больших диализаторов, если требуется выведение токсинов, крупнее, чем средние молекулы, и применяется высокая скорость подачи замещающего раствора.
VII. ВЫБОР ДИАЛИЗИРУЮЩИХ И ЗАМЕЩАЮЩИХ РАСТВОРОВ. Растворы для CRRT поставляются приготовленными в заводских условиях и стерильными. Обычно они разлиты в пластиковые мешки объемом 2,5 или 5 л. В ряде случаев емкости имеют два отделения, содержимое которых необходимо смешать непосредственно перед применением раствора.
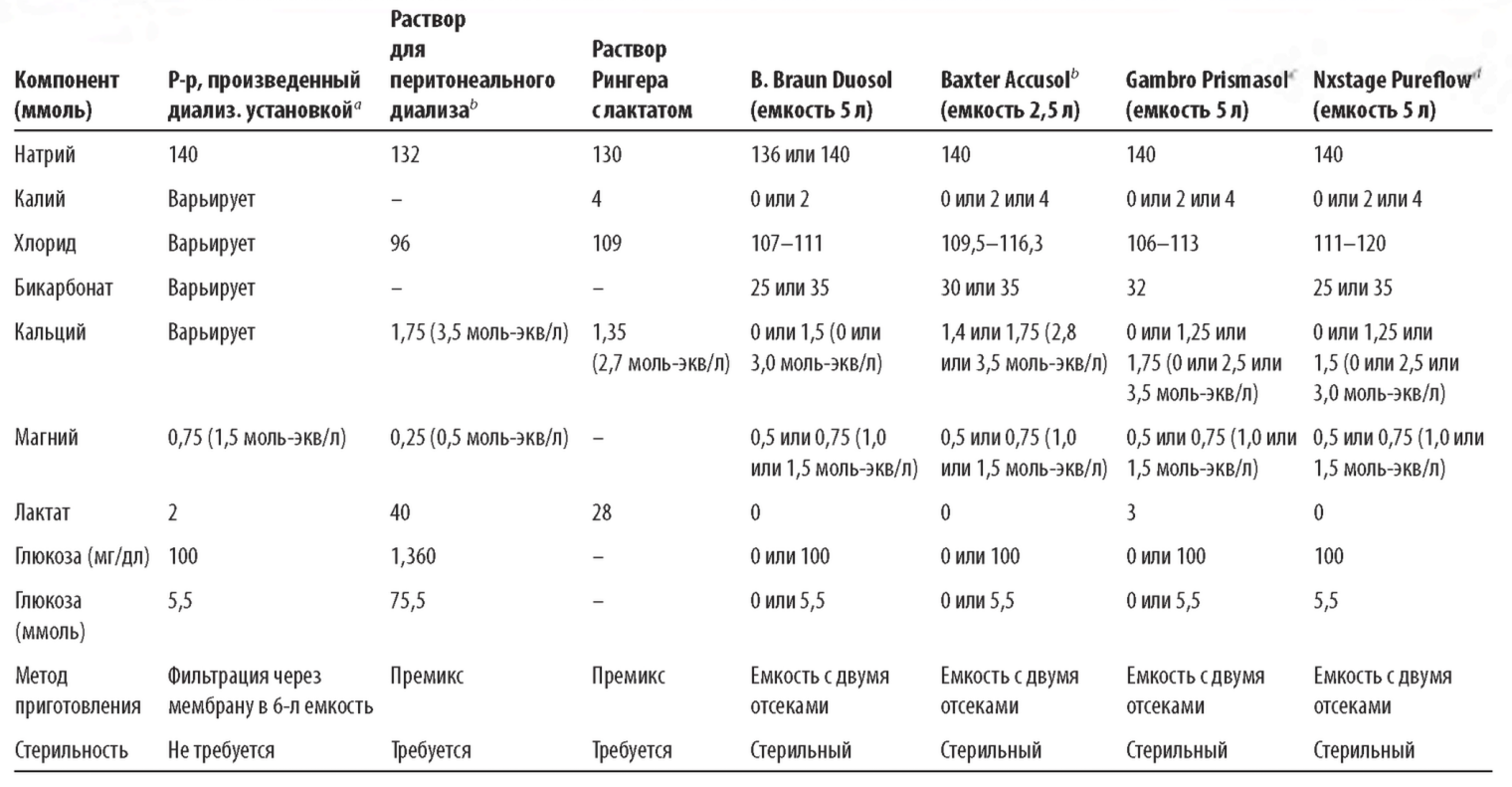
А. Состав растворов (табл. 15.3).
1. Буферные растворы. Готовятся на основе лактата или бикарбоната.
a. Лактатные растворы. Замещающие лактатные растворы обычно содержат 40-46 ммоль лактата. Лактатные растворы эффективно корректируют метаболический ацидоз у большинства пациентов. В молярном выражении метаболизм лактата в бикарбонат составляет 1:1, но на практике для коррекции одной и той же степени ацидоза концентрация лактата в диализирующем растворе должна быть выше, чем бикарбоната.
b. Бикарбонатные растворы. Данные растворы поставляются в емкостях, разделенных на два отсека, наподобие тех, в которых продается бикарбонатный диализирующий раствор для перитонеального диализа. Бикарбонатные буферные растворы более предпочтительны, и общая концентрация оснований в них - 25-35 ммоль. Некоторые растворы содержат небольшое количество лактата (3 ммоль), остающегося после подкисления готового раствора молочной кислотой. Данных, что это небольшое количество лактата вносит вклад в гиперлактатемию, нет.
Если назначаются высокие скорости потока диализирующего или замещающего раствора (например, >30 мл/кг/ч), применение растворов с пониженным содержанием бикарбоната может предотвратить метаболический алкалоз. Растворы с низкой концентрацией бикарбоната или совсем без него также назначаются при регионарной цитратной антикоагуляции, поскольку цитрат метаболизируется в бикарбонат в печени.
с Условия, при которых растворы с большой концентрацией лактата должны применяться с осторожностью. Применение лактатных растворов, генерирующих бикарбонат, как выяснилось, усугубляет гиперлактатемию у пациентов с тяжелой нестабильностью кровообращения, сопровождающейся гипоперфузией тканей, а также у пациентов с тяжелым поражением печени. В KDIGO AKI 2012 г. использование бикарбонатных растворов рекомендуется для всех пациентов с острым почечным повреждением с низким уровнем доказательности (2С), но более аргументировано - для пациентов с печеночной недостаточностью и/или с лактатным ацидозом (уровень доказательности 2В) и для пациентов с циркуляторным шоком (уровень доказательности 1В).
Таблица 15.3 Сравнение некоторы х растворов для CRRT
d. Цитратные растворы. Цитратные растворы появились в результате попыток совмещения буферных и антикоагулирующих свойств цитрата, а также для упрощения сложных протоколов регионарной цитратной антикоагуляции (РЦА8). Основной объем цитратных растворов должен подаваться в контур до гемофильтра - для обеспечения адекватной антикоагуляции. От 40 до 60% цитрата, подаваемого в контур в режиме предилюции, удаляется с диализатом, а остальное преимущественно метаболизируется печенью в бикарбонат (из 1 ммоль цитрата получается 3 ммоль бикарбоната). Поэтому такие растворы не подходят для С-HD, где поток диализирующего раствора и кровоток направлены в противоположные стороны, или для C-HF/HDF с преимущественным замещением после фильтра. Растворы с концентрацией цитрата 11-12 ммоль могут не обладать достаточной буферной емкостью (Naka, 2005). Растворы с повышенной концентрацией цитрата (14 ммоль) обеспечивают лучшую коррекцию ацидоза, а также продлевают время жизни фильтра (Egi, 2005, 2008). Растворы с концентрацией цитрата 18 ммоль также доступны, однако их влияние на кислотно-щелочной баланс пока мало изучено. Инфузию заместительных цитратных растворов лучше производить в режиме предилюции - для обеспечения оптимального соотношения концентраций цитрата и крови на входе в гемофильтр, а дополнительное выведение токсинов может достигаться применением бикарбонатных растворов либо в составе диализата, либо в замещающей жидкости в режиме постдилюции. Дополнительные методы цитратной антикоагуляции, а также потенциальные преимущества данного подхода рассматриваются далее в этой главе.
2. Натрий. Имеющиеся в продаже готовые растворы для CRRT, как правило, содержат физиологические концентрации натрия, около 140 ммоль. При лечении пациентов с тяжелой, и в особенности продолжительной гипонатриемией, когда стоит задача медленного повышения уровня натрия в плазме не более чем на 6-8 ммоль/л в день, замещающий или диализирующий раствор должен быть разбавлен водой до концентрации, лишь ненамного большей, чем преддиализный уровень натрия. Подробности можно найти в работе Yessayan et al. (2014). В некоторых методах антикоагуляции, требующих инфузии тринатрия цитрата в магистрали, применяются специально приготовленные диализирующие/замещающие растворы с пониженным содержанием натрия (100 ммоль) для предотвращения гипернатриемии.
3. Калий. Растворы для CRRT, не содержащие калия, доступны для стартовой терапии пациентов с острым почечным повреждением (ОПП) и тяжелой гиперкалиемией. После того как уровень калия в плазме снижен до безопасных значений, применяются растворы с концентрацией калия 4 ммоль - для минимизации риска развития аритмии и истощения запасов калия в организме. Доступные потребителям готовые растворы содержат 0, 2 или 4 ммоль калия. Для пациентов с высоким уровнем катаболизма и устойчивой гиперкалиемией также могут потребоваться растворы с пониженным содержанием калия.
4. Фосфор. Гипофосфатемия при продолжительной CRRT - нередкое явление, и может вызвать слабость дыхательных мышц и длительную дыхательную недостаточность у пациентов в критическом состоянии (Demirjian, 2011). Применение фосфатных замещающих растворов при гипофосфатемии -обычная практика, требующая, однако, частого мониторинга уровня фосфата в крови. Хорошая клиническая эффективность была получена путем непредусмотренного инструкцией добавления фосфата к раствору для CRRT с целью получения его концентрации в 1,2 ммоль (Troyanov, 2004). В продаже имеется замещающий раствор с содержанием фосфата 1,2 ммоль и бикарбоната 30 ммоль, и его применение ассоциируется с развитием легкого метаболического ацидоза и гиперфосфатемии по сравнению с обычными растворами для CRRT (Chua, 2012). Идеальная концентрация фосфора, вероятно, должна быть более низкой, но нужны дальнейшие исследования.
Сообщается о развитии ОПП после фосфатных клизм или внутривенного введения фосфатов. В одном из отчетов сообщается, что внутривенная инфузия 20 ммоль раствора фосфата натрия/калия в среднем около 5 часов не приводила к повышению уровня креатинина у пациентов с остаточной функцией почек, но ассоциировалась с некоторым снижением концентрации ионизированного кальция (Agarwal, 2014).
5. Кальций и магний. Большинство замещающих и диализирующих растворов содержат 1,5-1,75 ммоль кальция и 0,5-0,6 ммоль магния, и их применение обычно позволяет поддерживать целевые уровни в системной циркуляции. При регионарной цитратной антикоагуляции (РЦА) цитрат связывается с кальцием и магнием, из-за чего их концентрация в плазме понижается. Растворы для CRRT, применяемые при РЦА, зачастую не содержат кальция - для более эффективного снижения цитратом концентрации ионизированного кальция в фильтре и обеспечения адекватной антикоагуляции в экстракорпоральном контуре. Поэтому при РЦА необходимы дополнительные системные инфузии кальция и иногда магния - со строгим протоколом мониторинга их концентраций.
6. Глюкоза. В современных растворах для CRRT глюкоза либо не используется вообще, либо применяется в физиологических концентрациях, обычно 5,5 ммоль (100 мг/дл). Применение безглюкозных растворов при CRRT ассоциируется с гипогликемией, поэтому растворы, содержащие глюкозу, предпочтительнее; для предотвращения гипергликемии и достижения целевого уровня глюкозы в плазме в 6-8 ммоль (ассоциируемого с лучшими результатами терапии) требуется его регулярный мониторинг и при необходимости применение инсулина. Другим аргументом против безглюкозных растворов для CRRT является повышенное выведение глюкозы из организма на процедуре, что может привести к нарушению нутриционного баланса (Stevenson, 2013).
В. Способы приготовления бикарбонатных растворов для CRRT, если готовые растворы недоступны. Индивидуальные ультрачистые растворы с требуемой концентрацией бикарбоната могут быть приготовлены в аптеке либо в самом диализном аппарате. Второй способ применим только в странах, где онлайн-гемофильтрация официально разрешена. Можно приготовить стерильный диализирующий или замещающий раствор с концентрацией бикарбоната 30-35 ммоль. Ионы бикарбоната присутствуют в растворе только при наличии уравновешивающей их свободной углекислоты, которая неустойчива и распадается на углекислый газ и воду, поэтому бикарбонатные растворы нестабильны. Бикарбонат-ионы также образуют нерастворимые соли с кальцием и магнием. Поэтому замещающие и диализирующие бикарбонатные растворы следует готовить непосредственно перед их использованием.
1. Метод с одним контейнером. Замещающий или диализирующий бикарбонатный безлактатный раствор готовят следующим образом (обычно в условиях больничной аптеки): NaHCO3 и некоторое количество NaCl добавляют к 0,45% раствору NaCl, имеющемуся в продаже. Также добавляется небольшое количество СаС12 • 2Н2О, а магний вводится парентерально, по необходимости.
Состав раствора: 1,0 л раствора 0,45% NaCl + 35 мл раствора 8,4% NaHCO3 (32 ммоль) + 10 мл раствора 23% NaCl (40 ммоль) + 2,1 мл раствора 10% СаС12 • 2Н2О (1,45 ммоль или 2,9 мЭкв/л). Общий объем готового раствора -1,047 л.
Итоговые концентрации в растворе, в ммоль: Na - 145; Cl - 114; НСО3 - 33; Са- 1,35 (2,7 мЭкв/л).
2. Метод с двумя контейнерами. Емкости 0,9% физраствора с добавлением кальция чередуются с емкостями 0,45% физраствора с добавлением бикарбоната. Состав раствора А: 1,0 л 0,9% физраствора + 4,1 мл раствора 10% СаС12 • 2Н2О (2,8 ммоль или 5,6 мЭкв/л).
Состав раствора В: 1,0 л 0,45% физраствора + 75 мл раствора 8,4% NaHCO3 (75 ммоль). Общий объем готового раствора - 2,079 л.
Итоговые общие концентрации в обоих растворах, в ммоль: Na - 147; Cl -114; НСО3 - 36; Са - 1,35 (2,7 мЭкв/л).
3. Аппаратный метод (только для С-HD). Можно приготовить бикарбонатный диализирующий раствор для С-HD путем ультрафильтрации стандартного диализирующего раствора, приготовленного диализным аппаратом, через диализатор (для удаления бактерий), с последующим хранением полученного раствора в стерильной 15-литровой дренажной емкости от циклера для перитонеального диализа. Такие растворы должны быть использованы сразу же после приготовления. В настоящее время растворы хранят в более удобных 6-литровых стерильных пластиковых мешках (пакетах). В приготовленных таким образом растворах не наблюдается роста бактерий, по крайней мере, в течение 72 часов и даже при хранении до одного месяца (как показывают наблюдения). Однако на практике такие растворы не используются, если они хранились более 72 часов. За 10 лет применения данного метода не сообщалось о каких-либо негативных последствиях его использования, и при проведении LAL-теста таких растворов эндотоксин не обнаруживается (Тео, 2006).
C. Стерильность. Для С-HD и C-HDF применяются стерильные диализирующие растворы. Медленный поток диализата, а также длительное время использования одного и того же набора магистралей и фильтра способствуют росту бактерий. Все замещающие растворы, подаваемые непосредственно в магистрали крови, должны быть стерильными.
D. Температура диализирующего/замещающего раствора. Процедура CRRT может устанавливать введение растворов при комнатной температуре. Это отличается от традиционного протокола диализа, когда диализирующий раствор подогревается. Применение растворов с комнатной температурой приводит к потере тепла организмом, и не исключено, что гемодинамические преимущества CRRT во многом могут быть следствием такого охлаждения крови. Однако когда терапия проводится в течение продолжительного времени, индуцируемая CRRT потеря тепла может маскировать наличие лихорадки, уменьшая, таким образом, роль показателя температуры тела как признака наличия инфекции и воспаления. Насколько такая потеря тепла влияет на способность организма противостоять инфекциям, пока не изучено. В одном исследовании на овечьей модели септического шока продемонстрировано повышение выживаемости при подогреве крови в экстракорпоральном контуре (Rogiers, 2006). Современные установки для CRRT имеют системы подогрева растворов. Подогрев иногда приводит к появлению пузырьков в замещающем или диализирующем растворах, особенно бикарбонатных, однако клиническая значимость такого эффекта пока не ясна.
VIII. НАЗНАЧЕНИЕ И ОБЕСПЕЧЕНИЕ CRRT
A. Доза и ее связь с исходами. При остром почечном повреждении рекомендуется доза CRRT, соответствующая объему ультрафильтрата 20-25 мл/кг в час (KDIGO АКТ 2012). Эта рекомендация, однако, приведена без градации по степени доказательности, и нет данных, что меньшие дозы дают худший результат лечения. Есть единичные рандомизированные, контролируемые исследования, указывающие, что заметное повышение объема замещения приводит к лучшим исходам, однако эти результаты пока не подтверждены. В одном механистичном анализе было показано, что увеличение фильтрационного объема приводит к небольшому улучшению клиренса средних молекул (Hofmann, 2010) и что лучший способ повышения эффективности выведения таких молекул заключается в увеличении скорости кровотока и площади поверхности мембраны. Не существует доказательств, что конвекционные методы терапии (С-Н или C-HDF) приводят к лучшим результатам, чем методы, основанные на диффузии (С-HD). Выбор адекватной дозы CRRT остается областью, в которой необходимо больше исследований.
Для обеспечения объема УФ на уровне 20-25 мл/кг в час следует назначить пониженную скорость замещения, поскольку общий объем фильтрата будет включать от 2 до 5 л удаляемых из организма излишков жидкости в день. Однако это зачастую сопряжено с техническими сложностями, приводящими к прерыванию процедуры, или снижению ее эффективности из-за частичного тромбирования диализатора, поэтому следует назначать несколько большую скорость замещения, чем ее целевое значение. Как уже указано ранее, в режиме предилюции скорость инфузии замещающего раствора должна быть увеличена на 15-20%, в зависимости от соотношения скорости инфузии в режиме предилюции и кровотока. Эффект разведения будет более выраженным для соединений, выводимых исключительно из плазмы, поскольку в этом случае он будет пропорционален отношению скорости инфузии замещающей жидкости к скорости плазмотока, чем к соотношению скорости инфузии раствора и кровотока.
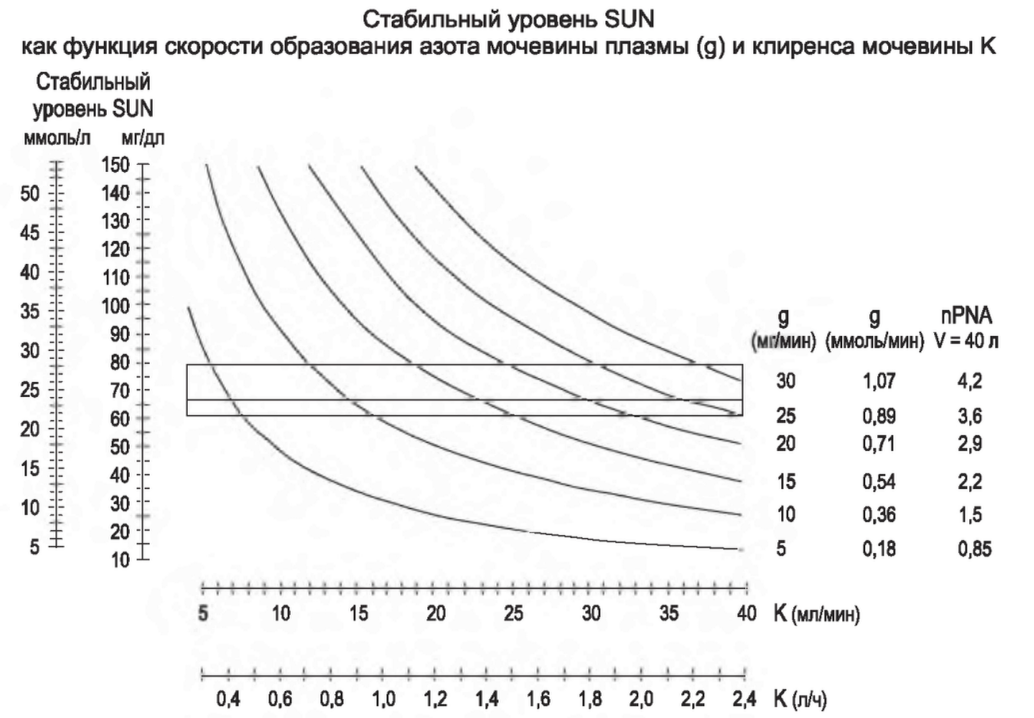
B. Эмпирическое определение дозы CRRT. Интенсивность лечения должна подбираться на основании клинических признаков. Интенсивность CRRT может быть увеличена у пациентов с высоким уровнем катаболизма, с целью нутритивной поддержки, при синдроме лизиса опухоли или при интоксикации лекарственными препаратами, если пациент не переносит интермиттирующие методы заместительной терапии. Для определения адекватных доз CRRT может быть полезным ежедневное измерение сывороточного уровня азота мочевины в период проведения терапии. Основываясь на данных исследований RENAL и ATN, следует придерживаться целевого уровня азота мочевины плазмы в 45 мг/дл (16 ммоль/л). Способы дозировки CRRT исходя из целевого уровня азота мочевины крови, приведены в табл. 15.4. Упрощенная номограмма достижения целевого уровня азота мочевины крови показана на рис. 15.3.
Таблица 15.4 Выбор дозы CRRT исходя из целевого значения уровня азота мочевины крови


С. Определение дозы SLED и SLED-F. Учитывая почти полное отсутствие исследований, посвященных выбору дозы при SLED и SLED-F, не существует каких-либо специальных рекомендаций на этот счет. При применении интермиттирующей терапии IRRT рекомендации KDIGO AKI предписывают достижение минимального недельного Kt/V, равного 3,9, рассчитываемого как сумма значений всех процедур, проведенных за неделю. Обычно процедура SLED длится 6-12 часов, с кратностью от 4 до 7 раз в неделю, с QB = 200-300 мл/мин и при скорости потока диализирующего раствора (QD) 300-400 мл/мин (Kumar, 2000). При таком режиме недельный Kt/V намного превышает рекомендованное KDIGO значение 3,9.
РИСУНОК 153. Оценка общего экстракорпорального клиренса мочевины, необходимого, чтобы поддержать различные стабильные уровни азота мочевины в сыворотке. Клиренс - по горизонтальной шкале - считывается по точке пересечения скорости генерации азота мочевины (д) и избранного целевого стабильного уровня азота мочевины сыворотки. (Из Garred LJ. Syllabus of the Second International Conference on CRRT, San Diego, CA, Feb 9,1997, p. 7). [При использовании единицы мг/дл традиционно говорят об уровне азота мочевины, при использовании единицы системы СИ ммоль/л чаще говорят об уровне мочевины, хотя имеется в виду одно соединение; для пересчета уровня азота мочевины в мг/дл в уровень мочевины в ммоль/л требуется разделить первую величину на 2,8 (Прим, переводчика)]
IX. ОБОРУДОВАНИЕ ДЛЯ CRRT. Для проведения различных форм CRRT существует немало специально разработанных аппаратов. На некоторых из них можно проводить процедуры плазмафереза, что остается вне рамок данной главы. Очень сложно сделать обзор всех устройств, а выбор некоторых машин, описанных ниже, не следует рассматривать как их преимущество над конкурентами.
А. Система Prismaflex® компании Гамбро (США)10. Данная система имеет в своем составе пять насосов - крови, диализирующего раствора, эффлюента (ультрафильтрата), насос замещающего раствора для пре- и постдилюции, насос перед насосом крови (НПНК) и четыре выдвигаемых взвешивающих устройства со съемными ручками для емкостей с ультрафильтратом, диализирующим и замещающим растворами, а также для НПНК, что позволяет контролировать объемы жидкостей при разных вариантах CRRT. Наличие НПНК делает возможной инфузию замещающего раствора в режиме предилюции или непрерывную подачу антикоагулянта в контур перед насосом крови. Возможна также одновременная пре- и постдилюция, благодаря наличию интегрированных в контур пережим-ных клапанов, контролирующих подачу замещающего раствора. Могут использоваться различные источники для подачи диализирующего и замещающего растворов. Контроль ультрафильтрации и точного объема выводимой из организма жидкости осуществляется с помощью встроенной контрольной панели с сенсорным экраном, которая регулирует скорость помпы диализирующего раствора, насоса эффлюента, пренасоса крови и скорость насоса замещающего раствора. Другие особенности включают заранее собранные сеты-картриджи, содержащие магистрали, гемофильтр и программируемый блок-шприц для подачи антикоагулянта, а также опционально подогреватель крови.
B. Использование модифицированных диализных аппаратов 2008К и 2008Т компании Фрезениус (США)”. Для С-HD можно использовать стандартные диализные аппараты, но некоторые из них должны быть модифицированы для обеспечения скорости подачи диализирующего раствора 100 мл/мин. Магистрали крови и диализаторы заменяются каждые 24 часа.
C. Использование усовершенствованных аппаратов 2008 Н/К компании Фрезениус (США). Дальнейшее усовершенствование оборудования для диализа позволило добавить штатную функцию проведения С-HD, без необходимости какого-либо дополнительного апгрейда аппарата. Скорость потока диализирующего раствора может быть установлена на уровне 100-200 мл/мин, однако данная опция должна быть выбрана в сервисном режиме, плюс потребуется дополнительная калибровка. Профилирование ультрафильтрации или содержания натрия в растворе не предусмотрено; также нельзя установить продолжительность ультрафильтрации или ее целевое значение. Экстракорпоральный контур, включая диализатор, необходимо заменять каждые 48 часов, согласно рекомендациям производителя. Эти установки также популярны для проведения процедур SLED, когда скорости потоков крови и раствора близки к обычным.
D. Система NxStage System One (США)27 28. Это модульная система, имеющая сенсорный дисплей, циклер с цифровым управлением, стенд со стойкой для инфузии растворов, а также опциональный нагреватель раствора. Данная система может применяться как портативный диализный аппарат или машина для процедур CRRT. Поскольку используются одноразовые картриджи, как с фильтром, так и без него, система позволяет проводить разные типы процедур, при этом необходимость обслуживания циклера и требования к дезинфекции минимальные. В картридже имеются волюметрические балансировочные камеры, что позволяет обойтись без встроенных весов; ультрафильтрат направляется напрямую в дренаж. Особенностью картриджа является отсутствие контакта крови с воздухом - для оптимизации потока крови и снижения тромбообразования.
E. Система «Диапакт» компании Б. Браун (США)29. Простая и компактная система для CRRT, первоначально предназначенная для чрезвычайных ситуаций, когда очищенная вода недоступна. Имеет в своем составе три насоса - крови, диализирующего и замещающего растворов, ультрафильтрации, а также электронные весы. Снабжена упрощенным пользовательским интерфейсом, интегрированным нагревателем раствора, а также дает возможность выбора диализатора. Помимо CRRT позволяет производить IHD и гемофильтрацию.
X. АНТИКОАГУЛЯЦИЯ. Для большинства пациентов с низким риском кровотечений обычно системно применяется гепарин, так как он недорог и прост в использовании. Пациентам, уже получающим системные антикоагулянты по другим показаниям (например, при внутриаортальной баллонной контрпульсации), не требуется дополнительная антикоагуляция. Для пациентов с тяжелой тромбоцитопенией или нарушениями свертываемости крови следует применить пробную процедуру CRRT без антикоагуляции. Для пациентов после операций или с высоким риском кровотечений можно использовать безгепариновую CRRT либо регионарную цитратную антикоагуляцию (РЦА). Для пациентов с неиммунной гепарин-индуциро-ванной тромбоцитопенией (ГИТ, тип I) может быть применена РЦА. Системная антикоагуляция часто необходима пациентам с иммунной гепарин-индуцирован-ной тромбоцитопенией (ГИТ, тип II), обычно сопровождающейся венозным или артериальным тромбозом. Для таких пациентов, которым требуется CRRT, предлагается системная антикоагуляция лепирудином и аргатробаном.
A. Гепарин. Если базовые значения тромбинового времени не повышены, то после подключения и заполнения гемофильтра или диализатора пациенту вводится 2000-2500 ед. гепарина предпочтительно через венозную магистраль. После этого нужно подождать 2-3 минуты, чтобы гепарин перемешался в системном кровотоке. Затем с помощью гепариновой помпы начинают непрерывную инфузию гепарина со скоростью 500-1000 ед/ч в артериальную магистраль, после чего начинают циркуляцию в экстракорпоральном контуре. Проведение и мониторинг гепаринизации описаны в табл. 15.5.
B. Безгепариновый метод. У пациентов с болезнями печени, после операций, с активным или недавним кровотечением, а также у пациентов с ГИТ CRRT может проводиться без гепарина. Фильтр будет периодически тромбироваться, что потребует более частой его замены. Если острое кровотечение произошло при проведении CRRT с гепарином, процедура может быть продолжена даже после прекращения введения гепарина. Если гепарин не используется, требуется предпринять ряд мер для уменьшения вероятности тромбоза.

Таблица 15.5 Протокол гепаринизации для продленных процедур
1. При С-HD скорость потока диализирующего раствора увеличивается на 2040%. Повышенная скорость потока диализирующего раствора компенсирует ожидаемые потери клиренса по мере медленного тромбирования диализатора без гепарина. При применении безгепаринового С-HD мы обычно не проводим периодические промывки системы физраствором через артериальную магистраль, в противоположность тому, как это обычно практикуется при безгепариновом IHD из-за опасений появления микропузырьков воздуха в фильтре, повышающих вероятность тромбоза.
2. Если С-HF производится без гепарина, предпочтительнее использовать режим предилюции, поскольку подача замещающего раствора в контур перед фильтром уменьшает гемоконцентрацию в процессе удаления воды из плазмы. Поддержание скорости кровотока на уровне 200 мл/мин или выше также помогает предотвратить раннее или чрезмерное тромбирование.
Если гепарин не используется у пациентов без коагуляционных расстройств, тромбоз диализатора обычно наступает через 8 часов. Ранним признаком начала тромбообразования является снижение соотношения уровней азота мочевины в диализате и в плазме до <0,8. Когда это соотношение опускается <0,6, тромбоз становится неизбежен.
С. Регионарная цитратная антикоагуляция (РЦА). Цитрат образует хелатные комплексы с кальцием (и магнием), что останавливает коагуляционный каскад. Комплексы кальция с цитратом удаляются с фильтратом, а те из них, которые попадают в организм, подвергаются метаболизму в печени и скелетных мышцах. РЦА может уменьшать риск кровотечений по сравнению с гепаринизацией при CRRT (Wu, 2012), со сравнимой или лучшей эффективностью сохранения работоспособности контура, в зависимости от используемой дозы цитрата (Monchi, 2004). Цитратная антикоагуляция, уменьшающая локальную концентрацию ионизированного кальция, способна также снижать активацию нейтрофилов и системы комплемента в экстракорпоральном контуре (Schilder, 2014). Для пациентов с отсутствием противопоказаний к введению цитрата рекомендации KDIGO 2012 AKI предписывают применение РЦА при CRRT.
Как правило, для уменьшения концентрации ионизированного кальция на выходе из фильтра до уровня 0,3-0,4 ммоль/л требуется содержание цитрата в крови 3 ммоль/л. Потери организмом кальция и магния восполняются системными инфузиями по точным протоколам. Токсичность определяется общей цитратной нагрузкой и усугубляется у пациентов с печеночной и полиорганной недостаточностью - у таких пациентов количество вводимого цитрата может превзойти способность пациента его метаболизировать, вызывая аккумуляцию кальцийцитратных комплексов и неадекватную регенерацию свободного кальция. В свою очередь, это может привести к метаболическому ацидозу (цитратному) с высокой анионной разницей и к повышению (>2,5) соотношения между общим и ионизированным кальцием (Meier-Kriesche, 2001) - состояния, требующего прекращения РЦА и коррекции гипокальциемии.
Для рутинной РЦА вместо цитрата натрия предпочтительнее использование раствора ACD-A30 - цитратно-глюкозного раствора А для антикоагуляции производства компании Бакстер31, США, содержащего 3% цитрата натрия (2,2 г на 100 мл), лимонную кислоту (0,73 г на 100 мл) и глюкозу (2,45 г на 100 мл), так как данный раствор менее гипертонический, изготовлен в заводских условиях, поэтому помогает избежать ошибок, связанных с приготовлением растворов для антикоагуляции, а также опасности для организма в результате передозировки. На сегодняшний день для CRRT было предложено множество протоколов РЦА. Главными осложнениями РЦА являются симптоматическое уменьшение концентрации ионизированного кальция и метаболический алкалоз, вызванный цитратом.
Мы предпочитаем такие протоколы РЦА, при которых инфузия цитрата минимальная - при них обычно применяются бескальциевые диализирующие или замещающие растворы, поскольку в таком случае инфузия цитрата нужна лишь для связывания кальция в крови пациента. Однако сообщается о протоколах РЦА, при которых используются кальцийсодержащие растворы (Mitchell, 2003). Такой метод имеет преимущество, так как позволяет избежать возврата пациенту крови с низким уровнем ионизированного кальция вблизи области сердца в случае отказа насоса, осуществляющего инфузию замещающего раствора кальция.
1. Протокол Шварца (рис. 15.4). В качестве примера приводим протокол РЦА при С-HD, предложенный Шварцем (2004).
а. К инфузионному насосу артериальной магистрали подсоединяется емкость с 1000 мл ACD-A, как можно ближе к сосудистому доступу пациента. В данной магистрали имеется клапан отрицательного давления, поэтому в случае остановки насоса крови инфузия продолжается в сторону насоса, а не прямо в больного. Скорость инфузии цитрата в мл/ч обычно в 1,5 раза больше, чем скорость потока крови в мл/мин. Например, при BFR = 200 мл/мин скорость инфузии цитрата будет 300 мл/ч.
РИСУНОК 15.4. Схема контура для продленного цитратного гемодиализа. Уровень WlgSO, был модифицирован до значения 1,1 ммоль (по сравнению с 1,3 ммоль в оригинальном протоколе Шварца). (Источник: Swartz R, et al. Improving thedelivery of continuous renal replacement therapy using regional citrate anticoagulation. Clin Nephrol. 2004; 61:134-143.)
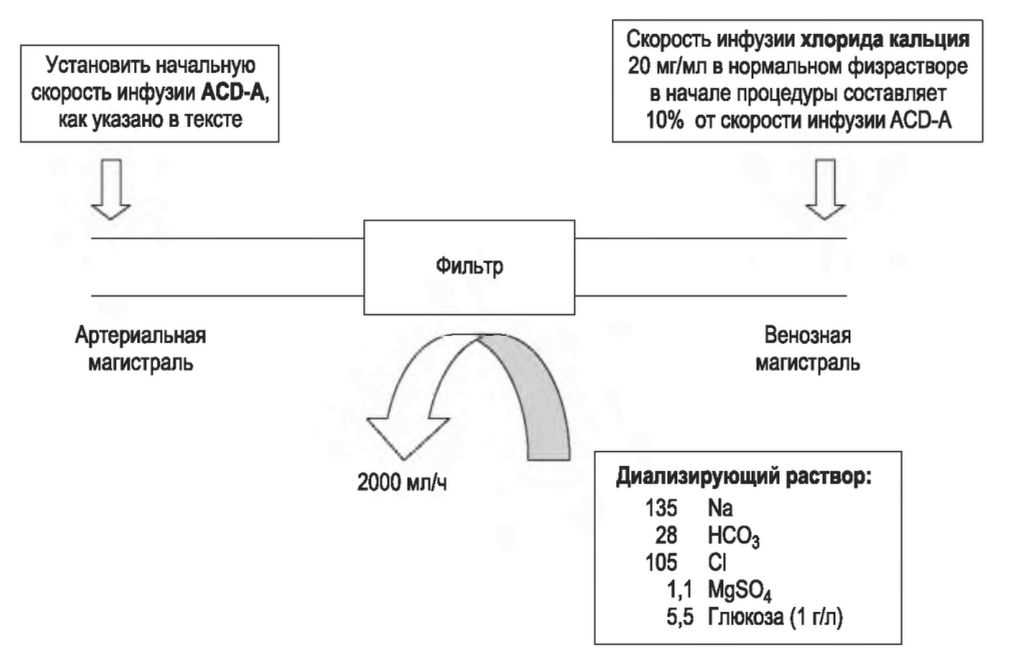
b. Инфузия хлорида кальция (20 мг/мл в изотоническом 0,9% растворе NaCl) производится через порт-тройник на венозном конце диализного катетера. Одновременно можно производить инфузию глюконата кальция через периферический венозный катетер, однако это будет приводить к дополнительной нагрузке жидкостью. Первоначальная скорость инфузии кальция должна быть на уровне 10% от скорости инфузии цитрата. Например, если скорость инфузии ACD-A 300 мл/ч, то скорость инфузии кальция - 30 мл/ч.
c. Пробы содержания ионизированного кальция в крови берутся каждые 2 часа х 4, затем каждые 4 часа х 4 первые сутки, после этого каждые 6-8 часов. Данный уровень должен быть проверен в течение 1-2 часов после смены сета или места инфузии, если что-либо производилось. Пробы должны браться из двух точек и маркироваться соответствующим образом: одна - «после фильтра» через порт из венозной магистрали; другая - взятая у пациента из артериальной или венозной магистрали. Базовые биохимические показатели и общий кальций должны проверяться каждые 6-8 часов. Титрование цитрата и хлорида кальция в растворе ACD-A производится в соответствии с табл. 15.6.
d. В данном методе используется диализирующий раствор без кальция и с содержанием 135 ммоль натрия, 1,1 ммоль (2,2 мЭкв/л) магния (в форме сульфата магния), 28 ммоль бикарбоната, 105 ммоль хлорида, 1,1 ммоль сульфата и 5,5 ммоль (1 г/л) глюкозы. Пониженные концентрации натрия и бикарбоната помогают скомпенсировать тоничность раствора и поступление бикарбоната с ACD-A. Скорость диализирующего раствора - 2,0 л/ч. Примечание: концентрация магния в растворе (1,1 ммоль) при данном методе выше, чем в большинстве доступных диализирующих растворов (0,5-0,75 ммоль, табл. 15.3).
Таблица 15.6 Титрование доз цитрата, поступающего с раствором ACD-A, и инфузий кальция при протоколе RCA по Шварцу

D. Протоколы регионарной цитратной антикоагуляции для SLED. Существует целый ряд таких протоколов, например протокол Fiaccadori (2013) или автоматизированная система Szamosfalvi (2010) - группа протоколов, которая, кроме прочего, работает с сенсорами измерения уровней цитрата и ионизированного кальция (Yang, 2011).
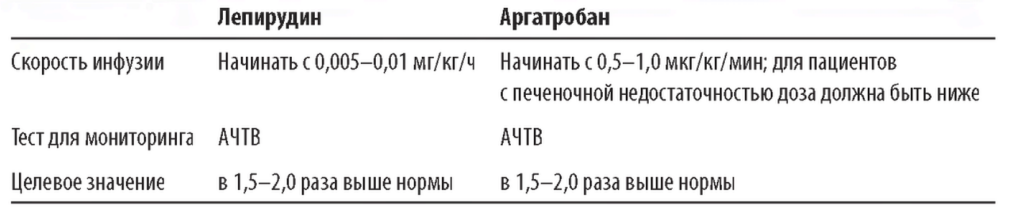
E. Антикоагуляция лепирудином и аргатробаном. Параметры доз приведены в табл. 15.7. Лепирудин (рекомбинантный гирудин) и аргатробан - прямые ингибиторы тромбина. Лепирудин выводится в основном почками. Поэтому его доза должна учитывать остаточную функцию почек и его клиренс при диализе. Препарат может вводиться методом постоянной инфузии либо болюсно. Типичная доза - 0,005-0,025 мг/кг массы тела в час. Эффект антикоагуляции контролируется измерением АЧТВ, поддерживаемого на уровне в 1,5-2 раза большем нормального, чтобы избежать возможного кровотечения. После 5 дней использования лепирудина в организме могут появиться антитела к нему. Эти антитела улучшают эффект антикоагуляции лепирудина, поэтому может потребоваться уменьшение его дозы для минимизации риска кровотечений. При длительном применении лепирудина АЧТВ должно измеряться ежедневно. Метаболизм аргатробана происходит главным образом в печени, препарат выводится с желчью, по этой причине он более предпочтителен для пациентов с почечной недостаточностью. Инфузии аргатробана начинают с 0,5-1,0 мкг/кг/мин, для пациентов с печеночной недостаточностью применяют меньшие дозы. Эффект антикоагуляции также контролируется измерением АЧТВ. При возникновении кровотечения из-за передозировки лепирудина или аргатробана необходимо введение свежезамороженной плазмы. Гемофильтрация с использованием высокопоточных диализаторов может снижать концентрацию гирудина в плазме.
F. Другие антикоагулянты
1. Низкомолекулярные гепарины (НМГ). Sagedal и Hartmann (2004) сделали обзор применения НМГ при CRRT. Мониторинг антикоагуляции требует определения активности анти-Ха-фактора, однако применимость таких измерений для дозирования НМГ при CRRT еще не доказана. НМГ нельзя инактивировать протамином. При С-HDF можно применять далтепарин в виде болюса с дозой 20 ед./кг с последующей инфузией дозы 10 ед./кг в час для адекватной антикоагуляции без риска развития кровотечений. В исследовании С-HD доза далтепарина в 35 ед./кг болюсно с последующей инфузией 13 ед./ кг в час приводила к увеличению времени работы фильтра, однако наблюдались эпизоды кровотечений. При более низкой дозе далтепарина, 8 ед./ч болюсно с последующей инфузией 5 ед./кг в час, срок работы контура был неудовлетворительным, так что оптимальная доза препарата должна быть, видимо, чем-то средним. Можно использовать эноксапарин и надропарин, однако данных об их применении недостаточно. Надропарин сравнивался с РЦА при С-HF: пациентам с массой тела >100 кг надропарин вводился в виде болюса 3800 ME с последующей продолжительной инфузией со скоростью 456 МЕ/ч; пациентам с массой тела <100 кг надропарин давался в дозе 2850 ME болюсно с последующей инфузией со скоростью 380 МЕ/ч. Мониторинг анти-Ха-активности не проводился. У пациентов в группе надропарина кровотечения наблюдались чаще, чем в группе РЦА (Oudemansvan Straaten, 2009). /p>
Таблица 15.7 Дозировка лепирудина и аргатробана при CRRT
2. Нафамостат мезилат. Синтетический ингибитор сериновых протеаз и аналог простациклина с минимальной гипотензивной активностью. Его применение при CRRT связывают с лучшими показателями срока жизни контура и относительно низким риском кровотечений. Начальная доза раствора (200 мг нафамостата, смешанного с 20 мл 5% раствора глюкозы) вводится методом постоянной инфузии со скоростью 10 мг/ч. Для мониторинга антикоагуляции в контуре используется АВС-тест (активное время свертывания крови) на месте, после чего скорость инфузии антикоагулянта может быть скорректирована (Baek, 2012).
G. Микропузырьки воздуха. Микропузырьки воздуха могут оказаться в экстракорпоральном контуре на этапе его подготовки или в любой момент, когда производятся манипуляции с магистралями, ведущими к гемофильтру. Микропузырьки могут попасть в полые волокна мембраны, что приводит к тромбообразо-ванию в них. Следует соблюдать осторожность при подготовке контура и при проведении инфузий.
H. Признаки тромбоза фильтра. Признаки заметного снижения скорости потока крови включают ее потемнение в экстракорпоральном контуре, понижение температуры крови в венозной магистрали, а также сепарацию плазмы и эритроцитов в контуре. Инфузия физраствора помогает определить момент начала тромбообразования в системе: физраствор позволяет визуализировать сгустки крови в прозрачных элементах гемофильтра.
При С-HD можно проверить отношение уровней азота мочевины в фильтрате (FUN : SUN). Если оно <0,6, тромбоз неизбежен. Для измерения общего объема пучка волокон мембраны (FBV32) во время использования диализатора можно использовать ультразвуковые приборы, однако онлайн измерение FBV не позволяет предсказать срок его адекватного функционирования. Одной из проблем является то, что тромбообразование в основном происходит в венозной воздушной ловушке, а не в самом диализаторе (Liangos, 2002).
XI. БАЛАНС ВИТАМИНОВ И МИНЕРАЛОВ. Общее количество аминокислот, выводимых из организма за сутки, при скорости УФ 1,0 л/ч и при инфузии стандартных растворов парентерального питания со скоростью 60-100 мл/ч составляет 12 г. При CRRT водорастворимые витамины и микроэлементы легко вымываются. Если ожидается длительная терапия, рекомендуется назначение витаминов и минералов: активных витаминов D, Е и С, цинка, селена, меди, магния, хрома и тиамина.
XII. ПРИНЦИПЫ ВЫВЕДЕНИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ ПРИ CRRT. Выведение лекарственных препаратов из организма при CRRT зависит: а) от свойств препарата, таких как молекулярная масса, способность связываться с белками крови, объем распределения в организме и доля, выводимая почками; б) особенностей пациента, таких как остаточная функция почек, избыточный объем жидкости, концентрация альбумина в крови, а также степень поражения других органов и систем, участвующих в метаболизме и экскреции лекарственного препарата (например, печени); в) параметров CRRT, таких как скорость крови, диализирующего раствора, ультрафильтрации и диализата, а также объем гемофильтра. Как С-HD, так и C-HF эффективно выводят вещества с малой молекулярной массой, однако при C-HF лучше выводятся препараты со средними и большими молекулами - из-за конвекции. В целом считается, что при С-HF клиренс препаратов выше, чем при C-HD, при одной и той же скорости оттока эффлюента, то есть CVVH > CVVHDF > CVVHD (Churchwell, 2009).
Различная интенсивность CRRT и уровень остаточной функции почек у пациента могут приводить к заметной вариабельности в способности к удалению лекарственных средств. Доступную литературу по дозированию лекарств у пациентов, получающих CRRT, следует использовать только как общее руководство, понимая, что они могут быть неприменимы к конкретным особенностям назначения и применения CRRT у данного пациента. Один из способов определения доз препаратов при проведении CRRT - оценка общего клиренса креатинина (СгС1) исходя из остаточной функции почек пациента и ожидаемого клиренса при CRRT (Matzke, 2011). Процедуру CRRT следует рассматривать как работу виртуальной почки со скоростью клубочковой фильтрации (СКФ), зависящей от общего объема ультрафильтрата. Каждые 10 л суточного объема диализата эквивалентны примерно 7 мл/мин СКФ (7,0 мл/мин х 1440 мин в день = 10,08 л в день). Таким образом, при назначении препаратов пациентам с анурией, получающим CRRT, следует ориентироваться на назначения, обычно даваемые пациентам с остаточной GFR в 7 мл/мин, в расчете на каждые 10 л удаляемого фильтрата (эффлюента).
В табл. 15.8 приведена примерная дозировка антибиотиков для пациентов с почечной недостаточностью, получающих С-HD и C-HDF. В тех случаях, когда это возможно, следует проводить терапевтический лекарственный мониторинг (TDM33) для таких антибиотиков, как ванкомицин, аминогликозиды, а также для других препаратов с узким терапевтическим индексом. Любые изменения в назначении CRRT или в клиническом статусе (например, ухудшение или улучшение функции почек) могут потребовать дополнительного мониторинга и пересмотра дозы.
Объем препаратов для повышения АД, выводимых при CRRT, обычно не особенно критичен, поскольку может корректироваться титрованием доз таких препаратов для обеспечения требуемого гемодинамического ответа. В табл. 15.9 приведена дозировка дополнительных препаратов, обычно назначаемых пациентам в отделениях интенсивной терапии, с указаниями относительно корректировки доз при CRRT.
XIII. ИЗОЛИРОВАННАЯ УЛЬТРАФИЛЬТРАЦИЯ И МЕДЛЕННАЯ ПРОДЛЕННАЯ УЛЬТРАФИЛЬТРАЦИЯ (SCUF). Изолированная ультрафильтрация (ИУФ) производится посредством стандартного диализного оборудования путем байпаса диализирующего раствора (без диализа / использования диализирующего раствора) и может проводиться перед диализом, после него или независимо от диализа. У пациентов с почечной недостаточностью ИУФ в большинстве случаев проводится до процедуры гемодиализа. SCUF производится с помощью того же контура, что и для С-HD (рис. 15.1), но без диализирующего раствора.
А. Изолированная ультрафильтрация. ИУФ обычно проводится при IHD. Она полезна для выведения излишков жидкости с минимизацией риска развития дизэквилибриум-синдрома при проведении первых одной-двух процедур диализа у пациентов с острой уремией. Также она используется амбулаторно - для пациентов с излишками жидкости, трудно поддающимися выведению. Принципиальное преимущество ИУФ в том, что она лучше переносится по сравнению с обычным гемодиализом. В настоящее время изолированная ультрафильтрация уже не рассматривается в качестве лучшего метода выведения жидкости из организма. Исторически плохая переносимость выведения излишков жидкости при IHD была следствием применения ацетат-содержащего или перегретого диализирующего раствора, а также раствора со слишком низким содержанием
Таблица 15.8 Дозировка антимикробных препаратов при CRRT
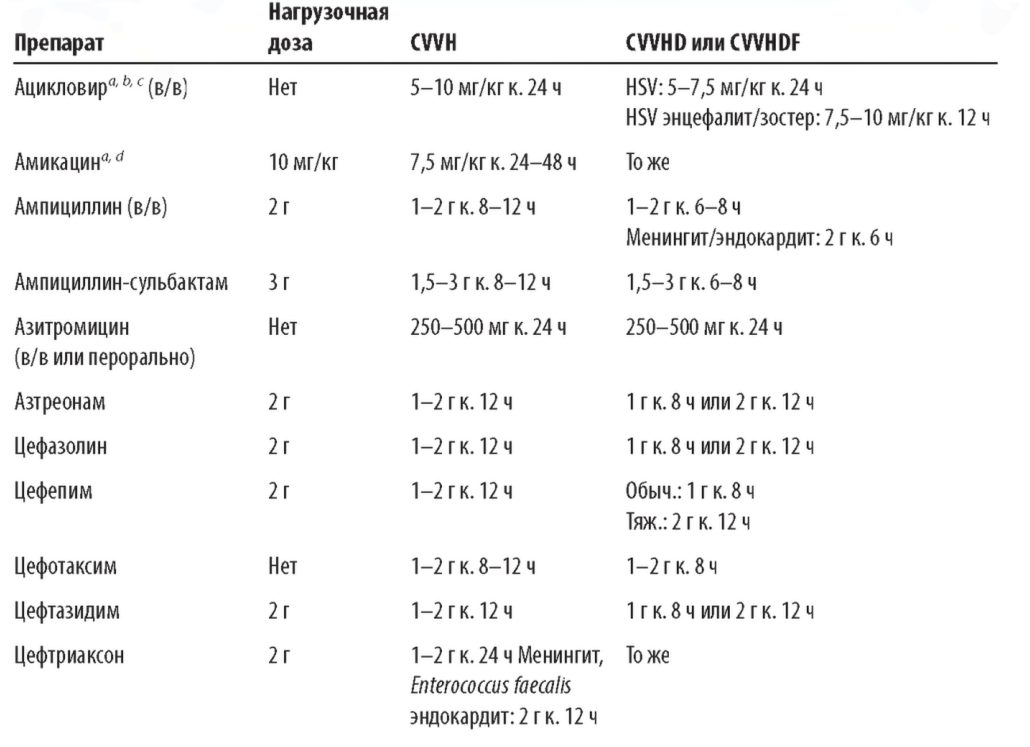
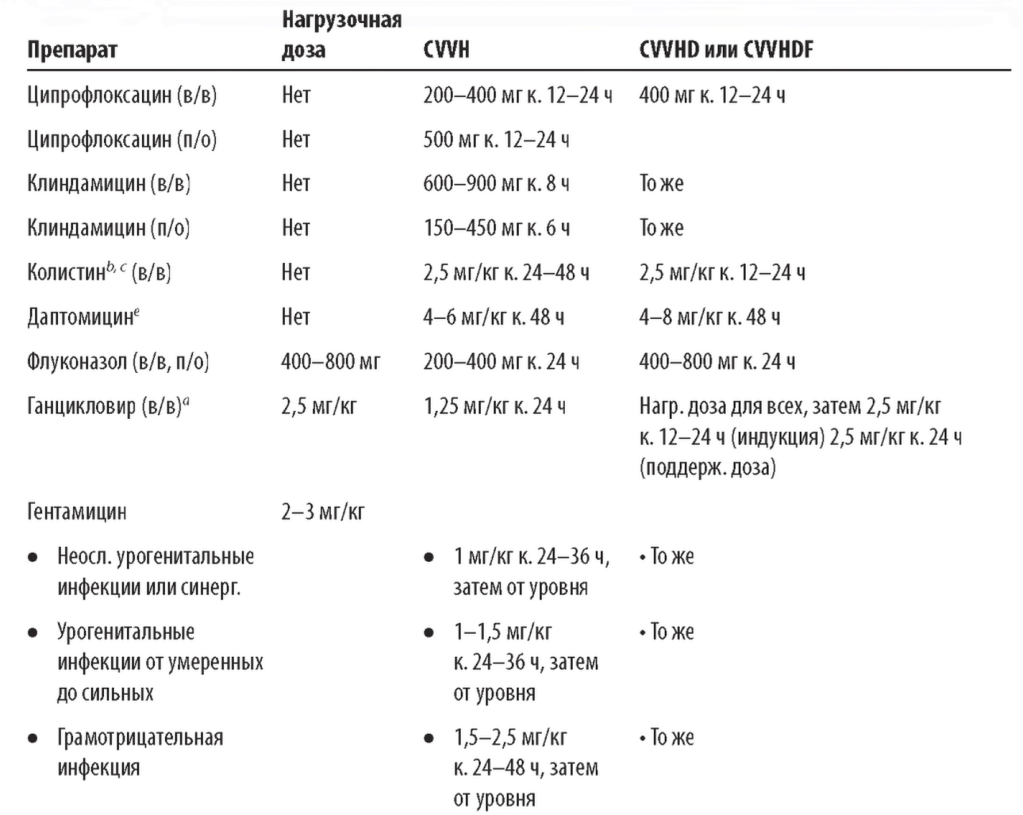

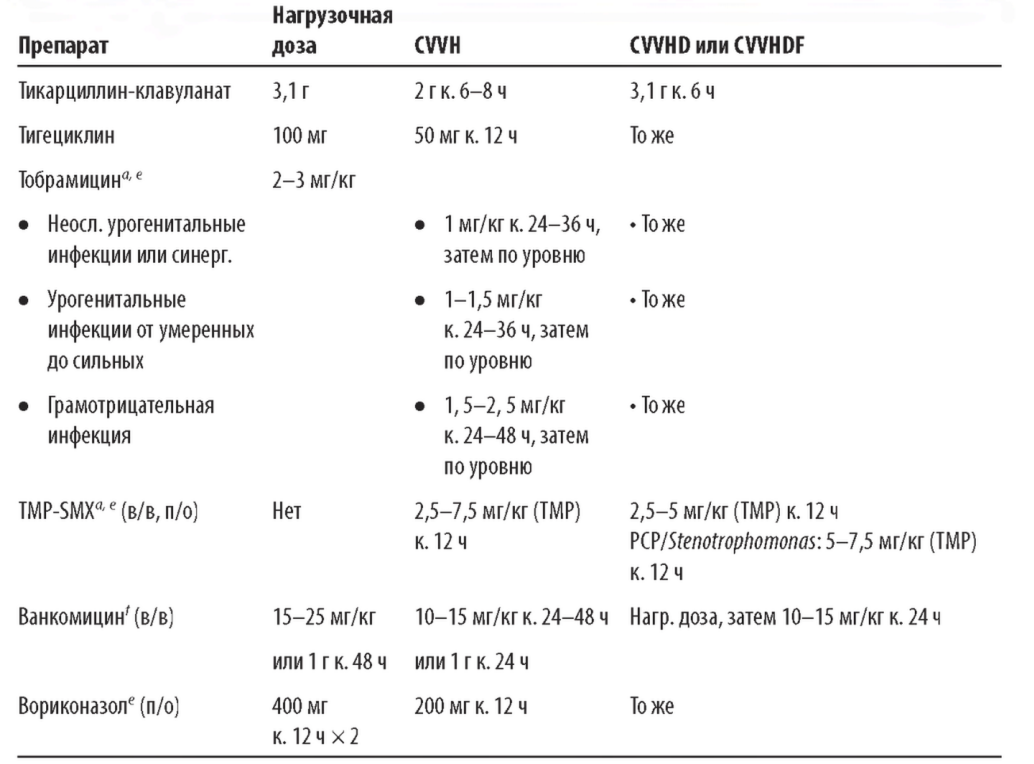

Таблица 15.9 Рекомендованные дозы некоторых препаратов, используемых в отделениях интенсивной терапии (для взрослых пациентов)


После исключения этих факторов (например, при использовании бикарбонатных растворов, с достаточным содержанием натрия и несколько охлажденных) превосходство ИУФ в плане обеспечения гемодинамической стабильности перестает наблюдаться. При ИУФ выведение уремических токсинов минимальное. Поэтому продолжительность следующей за ИУФ процедуры гемодиализа не должна сокращаться, и это влияет на общую длительность терапии.
Несмотря на относительно хорошую переносимость пациентами выведения излишков жидкости методом ИУФ, при превышении некоторого порога скорости ультрафильтрации может возникать гипотензия. Если наблюдается явная отечность пациента, гипотензия при скорости ультрафильтрации 1,5 л/ч проявляется редко, однако не следует превышать этот порог, если не используется мониторинг объема крови на основе датчика гематокрита. Сообщается о рикошете гиперкалиемии до опасных значений после интенсивной ИУФ - возможно, из-за перехода внутриклеточного калия во внеклеточное пространство. Хотя данное осложнение наблюдается далеко на всегда, любое возможное развитие гиперкалиемии при ИУФ должно купироваться путем обязательного проведения гемодиализа.
В. Медленная длительная ультрафильтрация (SCUF). SCUF применяется прежде всего в отделениях интенсивной терапии - для выведения излишков жидкости у пациентов со значительной остаточной функцией почек и у тех, для кого дисбаланс электролитов и нарушение кислотно-щелочного состояния не являются серьезной проблемой. SCUF также используется для стационарного лечения пациентов с рефрактерной сердечной недостаточностью и умеренным нарушением функции почек, как описано ниже. Недостатком SCUF является необходимость коррекции имеющихся у пациентов нарушений баланса электролитов и КОС недиализными методами.
1. SCUF при рефрактерной сердечной недостаточности. У пациентов с рефрактерной сердечной недостаточностью может развиваться сопутствующая почечная недостаточность, приводящая к появлению гипергидратации. У таких пациентов может наблюдаться анурия, олигурия либо недостаточное выделение мочи (<1 л в сутки), несмотря на оптимальную терапию и максимально возможные дозы внутривенных диуретиков, инотропов и натрийуретических пептидов. В таких случаях может помочь проведение ультрафильтрации. Несмотря на то что существуют протоколы интермиттирующей изолированной ультрафильтрации при застойной сердечной недостаточности для стационарных и амбулаторных пациентов, ряд преимуществ SCUF должны приниматься во внимание. Медленное выведение жидкости минимизирует гемодинамические проблемы, такие как симптоматическая гипотензия. Вместе с тем немало таких пациентов сильно перегружены жидкостью, иногда на 10-15 кг выше массы тела, при которой пациент чувствует себя «в норме»; протоколы длительной CRRT позволяют выводить значительные объемы жидкости, избегая гемодинамических проблем. Техника ультрафильтрации может быть улучшена путем использования катетера Свана-Ганца для мониторинга центральной гемодинамики, и таким образом, точного определения конечной точки лечения, а также онлайн монитора объема крови - для предотвращения избыточной ультрафильтрации. Стали доступны компактные установки, специально разработанные для проведения SCUF. Однако большое рандомизированное исследование сравнения пошаговой фармакотерапии с ультрафильтрацией у пациентов с декомпенсаций сердечной недостаточности и ухудшением функции почек показало, что фармакологический подход приводит к лучшему сохранению функции почек в течение 96 часов с момента начала терапии (Bart, 2012).
XIV. ИНТЕРМИТТИРУЮЩАЯ ГЕМОДИАФИЛЬТРАЦИЯ описана в главе 17.
XV. ОСОБЕННОСТИ CRRT ДЛЯ НЕКОТОРЫХ ГРУПП ПАЦИЕНТОВ
A. Отек мозга. У пациентов с острой почечной недостаточностью в критическом состоянии CRRT мало влияет на уменьшение отека мозга по сравнению с IHD. Однако рекомендации KDIGO 2012 AKI особо предписывают применение CRRT вместо обычного IHD для пациентов с признаками отека мозга либо с повышенным внутричерепным давлением. CRRT минимизирует резкие расстройства сердечно-сосудистой системы, особенно в плане объема и давления крови, тем самым уменьшая амплитуду колебаний мозгового перфузионного и внутричерепного давления. Пациенты с печеночной недостаточностью - одна из групп риска развития отека мозга из-за трудностей в поддержании саморегуляции мозгового кровотока. Davenport (1999) использовал С-HF и C-HD, чтобы справиться с повышенным внутричерепным давлением и отеком мозга. Совсем немного данных сравнения эффективности SLED и CRRT. В одном из исследований SLED и CRRT оказывали одинаковый эффект на внутричерепное давление у пациентов, получавших диализ после геморрагического инсульта (Wu, 2013).
Для пациентов с риском развития отека мозга следует использовать современную аппаратуру для С-HF и С-HD - со строгим волюметрическим контролем, применяя бисовместимымые мембраны. Если возможно, следует избегать проведения антикоагуляции, поскольку это может повысить риск кровоизлияний в мозг либо в месте травмы, либо вокруг датчика внутричерепного давления.
Диализирующий или замещающий раствор должен иметь относительно большую концентрацию натрия (>140 ммоль) и низкое содержание бикарбоната (30 ммоль). Повышенная концентрация натрия уменьшает осмотический градиент между кровью и тканями мозга и минимизирует поступление воды в мозг. Быстрое повышение уровня бикарбоната в плазме увеличивает перемещение СО2 в клетки мозга. Поскольку ионы бикарбоната имеют заряд, они хуже проникают в клетки, чем СО2, вызывая, таким образом, парадоксальное понижение pH в тканях мозга. Внезапное уменьшение уровня pH приводит к образованию идиогенных осмолей, повышающих осмотический градиент, что вызывает увеличение поступления жидкости в мозг.
В тяжелых случаях неконтролируемого повышения внутричерепного давления может быть полезным охлаждение диализирующего или замещающего раствора в дополнение к другим мерам, применяемым для понижения температуры тела до 32-33 °C, при которой потребности мозга в кислороде снижаются (Davenport, 2001).
B. Сепсис и полиорганная недостаточность. Синдром полиорганной недостаточности является следствием выброса провоспалительных (в частности, ФНОр, тромбоксан В2, фактор активации тромбоцитов) и противовоспалительных (в частности, интерлейкин 10) медиаторов. Такая реакция организма провоцируется, в частности, эндотоксинами грамотрицательных бактерий, грамположитель-ними бактериями, вирусами, мезентериальной ишемией или травмой. При С-HF многие из этих медиаторов обнаруживаются в фильтрате септических пациентов или адсорбируются на мембране гемофильтра, что позволяет предположить, что С-HF обладает возможностью выведения септических медиаторов из циркуляции. Для таких пациентов предлагается использование высокообъемной C-FFF. Однако несмотря на то, что указанные процедуры снижают концентрации септических медиаторов, клинический эффект от такой терапии не особенно заметен, поэтому решение о применении высокообъемной (2 л/ч) C-FFF для таких пациентов остается неоднозначным. Тем не менее многие медицинские учреждения предпочитают C-FFDF вместо C-FFD для пациентов с сепсисом с целью лучшего выведения медиаторов воспаления при сохранении эффективности диализной терапии. Обычной стратегией является выбор клиренса 35 мл/кг в час, распределенный поровну между диализом и гемофильтрацией. Подробности данного метода можно найти у Joannidis (2009).
C. Острое легочное повреждение и острый респираторный дистресс-синдром (ARDS). Раннее применение CRRT для выведения излишков жидкости может оказаться полезным для улучшения показателей оксигенации и вентиляции (соотношения PaO2/FiO2 и индекса оксигенации) у пациентов с ARDS и сопутствующей острой почечной недостаточностью. Улучшение функционирования респираторной системы связано больше с выведением излишков жидкости, чем с удалением медиаторов воспаления (Hoste, 2002).
D. Профилактика контраст-индуцированной нефропатии. Хотя ряд исследований выявил пользу CRRT для пациентов с хронической почечной недостаточностью, проходящих исследования с применением внутривенного введения рентгеноконтрастных веществ (Marenzi, 2003), рабочая группа KDIGO 2012 AKI сделала вывод, что пока убедительных данных для проведения CRRT в таких случаях недостаточно, необходимы дополнительные исследования.
E. Отравление диализуемыми или проходящими через мембрану токсинами и лекарственными препаратами. Использование различных режимов CRRT может быть эффективным при лечении разного рода отравлений, особенно если концентрации токсинов в плазме невелики (см. главу 20).
F. Экстракорпоральная мембранная оксигенация (ЕСМО). SCUF или С-HD может проводиться для пациентов, получающих ЕСМО, одновременно с CRRT. Магистрали крови для ЕСМО могут быть приспособлены для подсоединения параллельно диализатору. Это делает возможным одновременное проведение С-HD или SCUF. Поскольку у таких пациентов наблюдается ARDS или избыток жидкости в организме, требующие, в первую очередь, применения ЕСМО, может оказаться полезным дальнейшее выведение жидкости, особенно для пациентов с хронической почечной недостаточностью. Если для лечения сопутствующей острой почечной недостаточности у таких пациентов требуется применение С-HD, предпочтительно использование стерильных диализирующих растворов, поскольку может наблюдаться значительная обратная фильтрация из-за высокого давления в контуре ЕСМО. В качестве метода антикоагуляции применялась РЦА (Shum, 2014).
XVI. ПРИМЕНЕНИЕ CRRT ДЛЯ НОВОРОЖДЕННЫХ И ДЕТЕЙ. Данная тема находится за пределами рассмотрения нашего руководства. За подробностями можно обратиться к работе Sutherland (2012).
Ссылки и рекомендуемая литература
Augustine JJ, et al. A randomized controlled trial comparing intermittent with continuous dialysis in patients with ARF.Aw J Kidney Dis. 2004; 44: 1000-1007.
Baek NN, et al. The role of nafamostat mesylate in continuous renal replacement therapy among patients at high risk of bleeding. Ren Fail. 2012; 34: 279-285.
Bart BA, et al. The Heart Failure Clinical Research Network. Ultrafiltration in decompensated heart failure with cardiorenal syndrome. N Engl J Med. 2012; 367: 2296-2304.
Bunchman ТЕ, Maxvoid NJ, Brophy PD. Pediatric convective hemofiltration: normocarb replacement fluid and citrate anticoagulation. Am J Kidney Dis. 2003; 42: 1248-1252.
Chua HR, et al. Biochemical effects of phosphate-containing replacement fluid for continuous venovenous hemofiltration. Blood Purif. 2012; 34: 306-312.
Churchwell MD, et al. Drug dosing during continuous renal replacement therapy. Semin Dial. 2009; 22: 185-188.
Claure-Del Granado R, et al. Effluent volume in continuous renal replacement therapy overestimates the delivered dose of dialysis. Clin J Am Soc Nephrol. 2011; 6: 467-475.
Cole L, et al. High-volume haemofiltration in human septic shock. Intensive Care Med. 2001; Th 978-986.
Dager WE, White RH. Argatroban for heparin-induced thrombocytopenia in hepatorenal failure and CWHD. Ann Pharmacother. 2003; 37: 1232-1236.
Davenport A. Is there a role for continuous renal replacement therapies in patients with liver and renal failure? Kidney Int Suppl. 1999; 72: S62-S66.
Davenport A. Renal replacement therapy in the patient with acute brain injury. Am I Kidney Dis. 2001; 37: 457-466.
Egi M, et al. A comparison of two citrate anticoagulation regimens for continuous veno-venous hemofiltration. Int IArtif Organs. 2005; 28: 1211-1218.
Egi M, et al. The acid-base effect of changing citrate solution for regional anticoagulation during continuous veno-venous hemofiltration. Int IArtif Organs. 2008; 31: 228-236.
Eichler P, et al. Antihirudin antibodies in patients with heparin-induced thrombocytopenia treated with lepiru-din: incidence, effects on aPTT, and clinical relevance. Blood. 2000; 96: 2373-2378.
Fiaccadori E, et al. Efficacy and safety of a citrate-based protocol for sustained lowefficiency dialysis in AKI using standard dialysis equipment. Clin I Am Soc Nephrol. 2013; 8: 1670-1678.
Fischer KG, van de Loo A, Bohler J. Recombinant hirudin (lepirudin) as anticoagulant in intensive care patients treated with continuous hemodialysis. Kidney Int Suppl. 1999; 72: S46-S50.
Golper TA. Update on drug sieving coefficients and dosing adjustments during continuous renal replacement therapies. Contrib Nephrol. 2001; 132: 349-353.
Heintz BH, et al. Antimicrobial dosing concepts and recommendations for critically ill adult patients receiving continuous renal replacement therapy or intermittent hemodialysis. Pharmacotherapy. 2009; 29: 562-577.
Hofmann CL, Fissell WH. Middle-molecule clearance at 20 and 35 ml/kg/h in continuous venovenous hemodi affltration. Blood Purif. 2010; 29: 259-263.
Hoste EA, et al. No early respiratory benefit with CWHDF in patients with acute renal failure and acute lung injury. Nephrol Dial Transplant. 2002; 17: 2153-2158.
Jacobi J et al. Clinical practice guidelines for the sustained use of sedatives and analgesics in the critically ill adult. Crit Care Med. 2002; 30: 119-141.
James M, et al. Canadian Society of Nephrology Commentary on the 2012 KDIGO Clinical Practice Guideline for Acute Kidney Injury. Am I Kidney Dis. 2013; 61: 673-685.
Jaski BE, et al. Peripherally inserted veno-venous ultrafiltration for rapid treatment of volume overloaded patients. I Card Fail. 2003; 9: 227-231.
Joannidis M. Continuous renal replacement therapy in sepsis and multisystem organ failure. Semin Dial. 2009; 22: 160-164.
Jorres A, et al. The ad-hoc working group of ERBP. A European Renal Best Practice (ERBP) position statement on the Kidney Disease Improving Global Outcomes (KDIGO) Clinical Practice Guidelines on Acute Kidney Injury: part 2: renal replacement therapy. Nephrol Dial Transplant. 2013; 28: 2940-2945.
KDIGO. KDIGO clinical practice guidelines for acute kidney injury. Kidney Int. 2012; 2 (suppl 1): 1-141.
Kellum JA, Bellomo R, Ronco C, (eds). Continuous Renal Replacement Therapy. Oxford: Oxford University Press; 2010.
Kim IB, et al. Insertion side, body position and circuit life during continuous renal replacement therapy with femoral vein access. Blood Purif. 2011; 31: 42-46.
Kumar VA, et al. Extended daily dialysis: a new approach to renal replacement for acute renal failure in the intensive care unit. Aw I Kidney Dis. 2000; 36: 294-300.
Lexi-Comp, Inc. (Lexi-Drugs’”). Lexi-Comp, Inc. May 22, 2013.
Liangos O, et al. Dialyzer fiber bundle volume and kinetics of solute removal in continuous venovenous hemodialysis. Aw I Kidney Dis. 2002; 39: 1047-1053.
Lins RL, et al. For the SHARF investigators. Intermittent versus continuous renal replacement therapy for acute kidney injury patients admitted to the intensive care unit: results of a randomized clinical trial. Nephrol Dial Transplant. 2009; 26: 512-518.
Lowenstein DH. Treatment options for status epilepticus. Curr Opin Pharmacol. 2005; 5: 334-339.
Kalviainen R. Status epilepticus treatment guidelines. Epilepsia. 2007; 48: 99-102.
Marenzi G, et al. Interrelation of humoral factors, hemodynamics, and fluid and salt metabolism in congestive heart failure: effects of extracorporeal ultrafiltration./4 m J Med. 1993; 94: 49-56.
Marenzi G, et al. The prevention of radiocontrast-agent-induced nephropathy by hemofiltration. N Engl J Med. 2003; 349: 1333-1340.
Marshall MR, et al. Sustained low-efficiency daily diafiltration (SLEDD-f) for critically ill patients requiring renal replacement therapy: towards an adequate therapy. Nephrol Dial Transplant. 2004; 19: 877-884.
Marshall MR, et al. Mortality rate comparison after switching from continuous to prolonged intermittent renal replacement for acute kidney injury in three intensive care units from different countries. Nephrol Dial Transplant. 2011; 26: 2169-2175.
Matzke GR et al. Drug dosing consideration in patients with acute and chronic kidney disease - a clinical update from kidney disease: improving global outcomes (KDIGO). Kidney Int. 2011; 80: 1122-1137.
McLean AG, et al. Effects of lactate-buffered and lactate-free dialysate in CAVHD patients with and without liver dysfunction. Kidney Int. 2000; 58: 1765-1772.
Mehta RL. Indications for dialysis in the ICU: renal replacement vs. renal support. Blood Pur if. 2001; 19: 227232.
Meier-Kriesche HU, et al. Unexpected severe hypocalcemia during continuous venovenous hemodialysis with regional citrate anticoagulation. Am I Kidney Dis. 1999; 33: e8.
Meier-Kriesche HU, et al. Increased total to ionized calcium ratio during continuous venovenous hemodialysis with regional citrate anticoagulation. Crit Care Med. 2001; 29: 748-752.
Messer J, et al. Middle-molecule clearance in CRRT: in vitro convection, diffusion and dialyzer area. ASAIO I. 2009; 55:224-226.
Mitchell A, et al. A new system for regional citrate anticoagulation in continuous venovenous hemodialysis (CWHD). Clin Nephrol. 2003; 59: 106-114.
Monchi M, et al. Citrate vs. heparin for anticoagulation in continuous venovenous hemofiltration: a prospective randomized study. Intensive Care Med. 2004; 30: 260-265.
Morgan D, et al. A randomized trial of catheters of different lengths to achieve right atrium versus superior vena cava placement for continuous renal replacement therapy. Am I Kidney Dis. 2012; 60: 272-279.
Morgera S, et al. Long-term outcomes in acute renal failure patients treated with continuous renal replacement therapies. Am I Kidney Dis. 2002; 40: 275-279.
Naka T, et al. Low-dose citrate continuous veno-venous hemofiltration (CWH) and acid-base balance. Int I Artif Organs. 2005; 28: 222-228.
Oudemans-van Straaten HM, et al. Citrate anticoagulation for continuous venovenous hemofiltration. Crit Care Med. 2009; 37: 545-552.
Palevsky PM, et al. KDOQI US commentary on the 2012 KDIGO clinical practice guideline for acute kidney injury. Am I Kidney Dis. 2013; 61: 649-672.
RENAL Replacement Therapy Study Investigators, Bellomo R, et al. Intensity of continuous renal-replacement therapy in critically ill patients. N Engl I Med. 2009; 361: 1627-1638.
Rogiers P, et al. Blood warming during hemofiltration can improve hemodynamics and outcome in ovine septic shock. Anesthesiology. 2006; 104: 1216-1222.
Rokyta R Jr, et al. Effects of continuous venovenous haemofiltration-induced cooling on global haemodynamics, splanchnic oxygen and energy balance in critically ill patients. Nephrol Dial Transplant. 2004; 19: 623-630.
Sagedal S, Hartmann A. Low molecular weight heparins as thromboprophylaxis in patients undergoing hemo-dialysis/hemofiltration or continuous renal replacement therapies. Eur I Med Res. 2004; 9: 125-130.
Salvatori G, et al. First clinical trial for a new CRRT machine: the Prismaflex. Int I Artif Organs. 2004; Tit 404-409.
Schilder L, et al. Citrate confers less filter-induced complement activation and neutrophil degranulation than heparin when used for anticoagulation during CWH in critically ill patients. BMC Nephrol. 2014; 15: 19.
Schindler R, et al. Removal of contrast media by different extracorporeal treatments. Nephrol Dial Transplant. 2001; 16: 1471-1474.
Shum HP, et al. The use of regional citrate anticoagulation continuous venovenous haemofiltration in extracorporeal membrane oxygenation. ASAIO I. 2014.
Splendiani G, et al. Continuous renal replacement therapy and charcoal plasmaperfusion in treatment of amanita mushroom poisoning. Artif Organs. 2000; 24: 305-308.
Stevenson JM, et al. In vitro glucose kinetics during continuous renal replacement therapy: implications for caloric balance in critically ill patients. Int I Artif Organs. 2013; 36: 861-868.
Sutherland SM, Alexander SR. Continuous renal replacement therapy in children. Pediatr Nephrol. 2012; Th 2007-2016.
Swartz R, et al. Improving the delivery of continuous renal replacement therapy using regional citrate anticoagulation. Clin Nephrol. 2004; 61: 134-143.
Szamosfalvi B, Frinak S, Yee J. Automated regional citrate anticoagulation: technological barriers and possible solutions. Blood Purif. 2010; 29: 204-209.
Teo BW, et al. Machine generated bicarbonate dialysate for continuous therapy: a 10-year experience. Blood Purif. 2006; 24: 247-273.
Troyanov S, et al. Phosphate addition to hemodiafiltration solutions during continuous renal replacement therapy. Intensive Care Med. 2004; 30: 1662-1665.
Van Berendoncks AM, et al.; SHARF Study Group. Outcome of acute kidney injury with different treatment options: long-term follow-up. Clin J Am Soc Nephrol. 2010; 5: 1755-1762.
van der Sande EM, et al. Thermal effects and blood pressure response during postdilution hemo di afiltration and hemodialysis: the effect of amount of replacement fluid and dialysate temperature. J Am Soc Nephrol. 2001;12:1916-1920.
Wester JP, et al. Catheter replacement in continuous arteriovenous hemo di afiltration: the balance between infectious and mechanical complications. Crit Care Med. 2002; 30: 1261-1266.
Wu MY, et al. Regional citrate versus heparin anticoagulation for continuous renal replacement therapy: a meta-analysis of randomized controlled trials. Aw J Kidney Dis. 2012; 59: 810-818.
Wu VC, et al.; the NSARF Group. The hemodynamic effects during sustained low-efficiency dialysis versus continuous veno-venous hemofiltration for uremic patients with brain hemorrhage: a crossover study. J Neurosurg. 2013; 119: 1288-1295.
Yagi N, et al. Cooling effect of continuous renal replacement therapy in critically ill patients. Aw J Kidney Dis. 1998; 32: 1023-1030.
Yang Y, et al. Development of an online citrate/Ca2+ sensing system for dialysis. Analyst. 2011; 136: 317-320.
Yessayan L, et al. Treatment of severe hyponatremia in patients with kidney failure: Role of continuous venove-nous hemofiltration wit low sodium replacement fluid. Aw J Kidney Dis. 2014; 64: 305-310.
Интернет-ссылки
ADQI Initiative: http://www.adqi.org.
HDCN CRRT Channel: http://www.hdcn.com/ch/cavh/.
KDIGO Clinical Practice Guideline for Acute Kidney Injury: http://www.kdigo.org/clinical_practice_guideli-nes/AKI.php.
