- Диализному врачу
- 1. Ведение пациентов с ХБП 4-5-й стадии.
- 2. Подготовка к трансплантации, диализу или к консервативной терапии
- 3. Физиологические принципы и моделирование кинетики мочевины
- 4. Оборудование для гемодиализа и расходные материалы
- 5. Вода для диализа и диализирующий раствор
- 6. Артериовенозные фистулы и протезы. Основные положения
- 7. Центральный венозный катетер в качестве доступа: основы
- 8. Мониторинг артериовенозного доступа и осложнений
- 9. Инфекции и другие осложнения центральных венозных катетеров
- 10. Назначение острого гемодиализа
- 11. Назначение хронического гемодиализа
- 12. Осложнения в ходе процедуры гемодиализа
- 13. Повторное использование диализаторов
- 14. Антикоагуляция
- 15. Продленная заместительная почечная терапия
- 16. Гемодиафильтрация
- 17. Терапевтический аферез
- 18. Актуальность сорбционных технологий сегодня
- 19. Руководство по диализу
Антикоагуляция
I. ТРОМБООБРАЗОВАНИЕ В ЭКСТРАКОРПОРАЛЬНОМ КОНТУРЕ. Во время процедуры диализа кровь пациента контактирует с фистульными иглами, магистралями, воздушными ловушками, торцевыми крышками диализатора, с герметизирующим составом и мембраной. Эти поверхности в различной степени тромботенны и могут инициировать образование тромбов, особенно в случае контакта крови с воздухом в воздушных ловушках. В результате формирование тромбов может вызвать окклюзию и нарушение функции экстракорпорального контура. Процесс образования тромба в экстракорпоральном контуре начинается с активации лейкоцитов и тромбоцитов, приводящей к блебингу и высвобождению богатых липидами микрочастиц на поверхности мембран, инициирующих образование тромбина и запускающих коагуляционный каскад, что ведет к дальнейшему образованию тромбина и отложению фибрина. Факторы, вызывающие тромбообразование в экстракорпоральном контуре, приведены в табл. 14.1.
А. Оценка коагуляции в процессе диализа
1. Визуальный осмотр. Признаки тромбообразования в экстракорпоральном контуре перечислены в табл. 14.2. Визуально оценить состояния контура лучше всего путем промывки системы физиологическим раствором с временным перекрытием притока крови.
2. Давление в экстракорпоральном контуре. Изменения показаний датчиков артериального и венозного давления в результате тромбирования в экстракорпоральном контуре зависят от локализации тромба. Преимущество использования магистралей с дополнительным отводом к датчику давления после насоса крови заключается в том, что разница между давлениями после насоса и венозной магистрали может служить индикатором места тромбоза. Увеличение разницы в давлении наблюдается, когда тромбирование ограничивается самим диализатором (повышенное давление после насоса, сниженное венозное давление). В случае наличия тромба в венозной ловушке или дистальнее ее одновременно повышается давление как после насоса крови, так и в венозной части магистрали. Если тромбообразование обширное, рост давления будет стремительным. Тромбирование или неправильное положение венозной иглы также приведет к повышению показателя венозного давления.
Таблица 14.1 Факторы, вызывающие тромбообразование в экстракорпоральном контуре


3. Внешний вид диализатора после диализа. Нередко после диализа в диализаторе имеется несколько тромбированных волокон и под торцевыми крышками находятся небольшие сгустки крови и белесые отложения (особенно у пациентов с гиперлипидемией). Более значительное тромбообразование в диализаторе должно быть документировано медицинским персоналом и послужить клиническим признаком для коррекции дозы антикоагулянта. Для стандартизации записей целесообразно классифицировать уровень тром-бообразования на основе визуального определения процента тромбированных волокон в диализаторе. Так, если таких волокон <10% - это уровень 1; <50% - уровень 2; >50% - уровень 3.
4. Измерение остаточного объема диализатора. Если в диализном центре практикуется многократное использование диализаторов, то после каждой процедуры диализа используются автоматизированные или ручные методы определения потери части волокон вследствие их тромбоза. Для этого сравниваются объемы диализатора до и после процедуры. Диализаторы, предназначенные для многократного использования, обычно теряют менее 1% объема диализатора после каждого из первых 5-10 использований.
II. ИСПОЛЬЗОВАНИЕ АНТИКОАГУЛЯНТОВ ВО ВРЕМЯ СЕАНСА. Если при проведении 3-4-часовой процедуры гемодиализа антикоагулянты не применяются, частота тромбирования диализатора оказывается значимой (5-10%), и в этих случаях теряются диализатор и магистрали, а также 100-180 мл крови (совокупный объем заполнения диализатора и магистралей в экстракорпоральном контуре). Такой подход признается приемлемым у пациентов с высоким и средним риском антикоагулянт-индуциро-ванного кровотечения, поскольку кровотечение у таких пациентов может привести к катастрофическим последствиям, таким пациентам диализ проводится без антикоагулянтов (см. далее). Однако для абсолютного большинства пациентов с небольшим риском развития кровотечений какой-либо вид антикоагуляции следует применять обязательно. При наличии программы повторного использования диализаторов адекватное применение антикоагулянтов - ключевой фактор для достижения планируемой кратности повторного использования.
В разных регионах мира, странах и даже отдельных диализных центрах существуют различные взгляды на то, какие антикоагулянты следует использовать на гемодиализе. Несмотря на целый ряд перспективных альтернатив, наиболее распространенным антикоагулянтом остается гепарин. В США в основном используется нефракционированный гепарин (НФГ), тогда как в Евросоюзе низкомолекулярный (фракционированный) гепарин (НМГ) является препаратом выбора в соответствии с Европейскими рекомендациями по наилучшей практике по гемодиализу (2002)Е В незначительном числе диализных центров используют цитрат натрия и в особых случаях в качестве альтернативы - прямые ингибиторы тромбина, такие как аргатробан, гепариноиды (данапароид, фондапаринукс), простаноиды и нафамостата малеат (синтетический ингибитор протеолитичесих ферментов).
III. ИЗМЕРЕНИЕ ПОКАЗАТЕЛЕЙ СВЕРТЫВАНИЯ КРОВИ ВО ВРЕМЯ ДИАЛИЗА. Хотя важно понимать общие принципы, каким образом коагуляционные тесты можно использовать для мониторинга антикоагулянтной терапии, в США из экономических соображений, с учетом сравнительно низкого риска геморрагических осложнений в ходе диализа и регуляторных требований (необходимость сертификации локальной лаборатории), гепарин назначается эмпирически, без контроля коагуляции. У пациентов с повышенным риском кровотечения необходимость контроля антикоагуляции часто обходится проведением безгепаринового диализа.
Если же мониторинг проводится, то кровь для анализа берется из артериальной магистрали проксимальнее точки инфузии гепарина - для оценки коагуляционного статуса пациента, а не экстракорпорального контура. Трудно получить достоверные данные по пробам из венозного катетера, в котором может содержаться остаток гепариновой заглушки, поэтому этот подход используется очень редко (Elemmelder, 2003).
А. Тесты для мониторинга гепаринотерапии
1. Активированное частичное тромбопластиновое время (АЧТВ). Измеряется только при применении Е1ФЕ Это наиболее часто используемый стационарный тест. Абсолютные значения результатов данного теста могут варьировать в широких пределах, поэтому во многих центрах результаты мониторинга выражают в виде отношения к контролю (АРРТг). Состояние резистентности к гепарину может быть ложным из-за повышенного уровня фактора свертываемости VIII. Удлинение исходного показателя АЧТВ может также наблюдаться из-за наличия в крови волчаночного антикоагулянта (Olson, 1998).
2. Частичное тромбопластиновое время (ЧТВ) цельной крови. Анализ похож на предыдущий, но он проводится непосредственно рядом с пациентом. Процесс коагуляции ускоряется добавлением 0,2 мл препарата Тромбофакс к 0,4 мл крови. Смесь помещается в нагреватель с температурой 37 °C на 30 с, после чего пробирка с пробой наклоняется из стороны в сторону каждые 5 с - до образования кровяного сгустка. Увеличение ЧТВ имеет линейную зависимость от концентрации гепарина в крови (в диапазоне, применяемом для диализа). Данный метод не следует использовать при терапии НМГ.
1 EBPG - European Best Practice Guidelines for Haemodialysis
3. Активированное время свертывания (АВС). Тесты ЧТВ и АВС похожи, но для ускорения процесса свертывания используется кремниевый песок. АВС-тест менее воспроизводим, чем ЧТВ-тест, особенно при низких концентрациях гепарина в крови. Устройства, которые автоматически покачивают пробирку и определяют момент образования кровяного сгустка, упрощают стандартизацию и повышают воспроизводимость обоих тестов - ЧТВ и АВС. Тест АВС используется только при терапии НФГ.
4. Время свертывания крови по Ли-Уайту (ВСЛУ/LWCT). Тест Ли-Уайта производится путем добавления в пробирку 0,4 мл крови с последующим ее переворачиванием на 180° каждые 30 с, до образования кровяного сгустка. Важно, чтобы кровь была комнатной температуры. Недостатками теста Ли-Уайта являются длительное время до получения результата, затраты времени персоналом, низкая воспроизводимость метода. Тест Ли-Уайта - наименее предпочтительный из всех, применяемых во время диализа, и в настоящее время используется крайне редко.
5. Активированный Ха фактор свертывания. Активность Ха фактора свертывания может измеряться хромогенными либо функциональными методами. Результаты разных лабораторных тестов на анти-Ха активность отличаются, так как некоторые из них содержат экзогенно очищенный антитромбин (АТ), поэтому анти-Ха активность, измеренная лабораторно, не обязательно коррелирует с реальным биологическим эффектом (Greeves, 2002). Хотя эффективность НФГ можно контролировать по активности Ха фактора, обычно такие тесты проводятся в случаях терапии НМГ и гепариноидами, как правило, нацелены на пик анти-Ха активности 0,4-0,6 МЕ/мл во время процедуры диализа и <0,2 МЕ/мл в конце процедуры и сразу после нее.
6. Ха-активированное время свертывания (Xa-ABQ цельной крови. Данный тест был предложен для мониторинга антикоагуляции в ходе применения НМГ (Frank, 2004) как более чувствительный, чем традиционный тест АВС, но не получил широкого распространения в клинической практике.
IV. МЕТОДЫ АНТИКОАГУЛЯЦИИ
А. Нефракционированный гепарин (НФГ)
1. Механизм действия. Гепарин изменяет конформацию антитромбина, что приводит к быстрой инактивации факторов свертывающей системы крови, в особенности Па. К сожалению, гепарин стимулирует агрегацию и активацию тромбоцитов, но этот нежелательный эффект компенсируется влиянием на связывание и активацию коагуляционных факторов на мембране тромбоцитов. Нежелательными побочным эффектами гепарина являются: зуд, анафилактоидные реакции, алопеция, остеопороз, гиперлипидемия, тромбоцитопения, а также повышенный риск кровотечений.
2. Целевые значения времени свертывания крови. Для больных, не склонных к повышенной кровоточивости, гепарин можно использовать свободно во время процедуры диализа, не опасаясь спровоцировать кровотечение. Эффект двух стандартных схем гепаринизации на время свертывания крови представлен на рис. 14. Е Целью является поддержание значений ЧТВ или АВС на 80% выше их исходных величин на протяжении большей части диализа (табл. 14.3). Однако к концу процедуры время свертывания крови должно уменьшаться (только на 40% выше исходных значений ЧТВ или АВС) с целью снижения риска кровотечения из сосудистого доступа после удаления игл.
РИСУНОК 14.1. Влияние различных режимов гепаринизации на время свертывания: А - обычный режим: несколько болюсных введений гепарина; В - обычный режим: метод постоянной инфузии гепарина; С - осторожный режим: метод постоянной инфузии гепарина в пониженных дозах
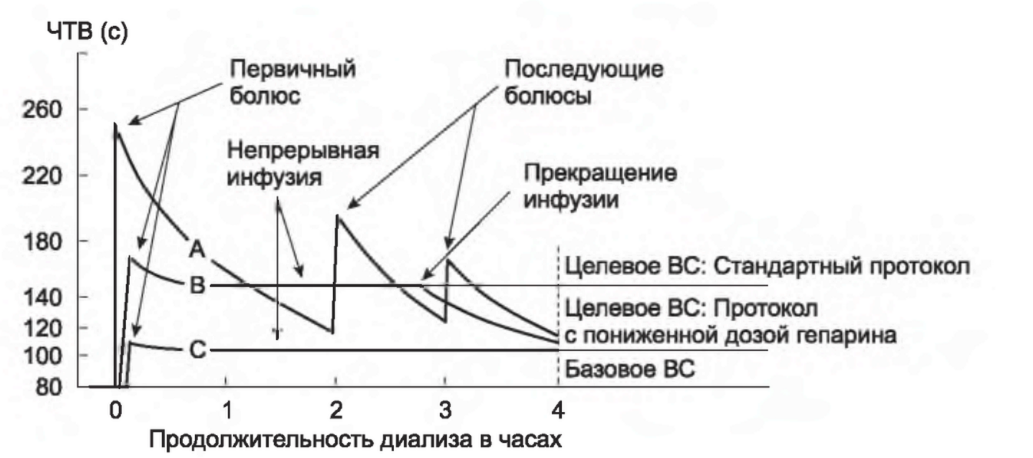
Таблица 14.3 Целевое время свертывания крови при диализе
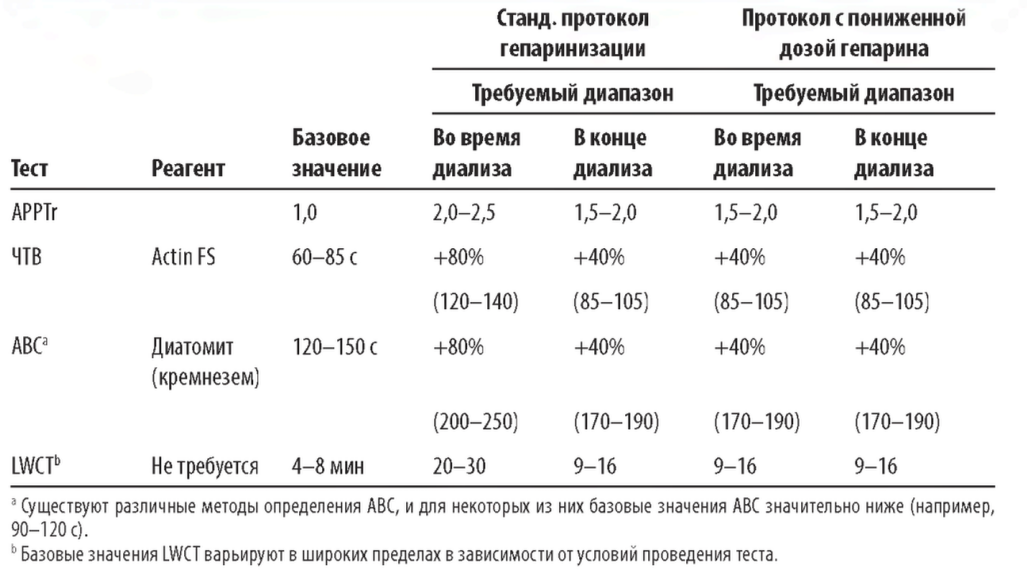
Целевые значения времени свертывания крови по Ли-Уайту (LWCT) также приведены в табл. 14.3. В отличие от ЧТВ цельной крови или АВС целевое значение свертывания крови по Ли-Уайту во время диализа значительно выше, чем на 80% от его исходной величины, а в конце процедуры -выше, чем на 40% от исходных значений.
3. Стандартные методы гепаринизации на диализе. Для стандартного введения гепарина на диализе существуют два метода: первый подразумевает начальное болюсное введение гепарина в систему, после чего он подается постоянно путем инфузии; второй заключается в том, что после первого болюсного введения гепарин вводится повторными болюсами по мере необходимости. В качестве демонстрации приводим примеры назначения каждого из этих режимов.
Стандартная гепаринизация методом постоянной инфузии
Производится первичное болюсное введение гепарина в систему (например, 2000 ЕД). Его лучше производить через венозную линию, после чего промывать физраствором (а не в артериальную магистраль). При введении гепарина в артериальную магистраль поступающая из фистулы негепарини-зированная кровь будет прокачиваться через экстракорпоральный контур, пока порция крови с введенным гепарином не пройдет через весь контур и антикоагулянтный эффект не развернется в системном кровотоке. Перед началом диализа необходимо подождать 3-5 минут для распределения гепарина, после чего можно начинать инфузию гепарина в артериальную часть контура (со скоростью, например, 1200 Ед/ч).
Стандартная гепаринизация единичной дозой или методом повторных болюсных введений
В данном случае вводится первичный болюс (например, 4000 ЕД). Затем по мере необходимости дополнительно подается по 1000-2000 ЕД.
В США, однако, методы гепаринизации значительно варьируют. В тех центрах, где предусмотрено многоразовое использование диализаторов, применяют большие дозы гепарина для максимального увеличения кратности их использования. В одних центрах ограничиваются одной дозой гепарина в начале процедуры (например, 2000 ЕД) без дальнейшего постоянного или болюсного введения, в других используют большой первичный болюс гепарина (75-100 Ед/кг), за которым следуют 500-750 Ед/ч путем инфузии. В настоящее время не проведено достаточного количества исследований, чтобы убедительно продемонстрировать оптимальный метод гепаринизации (Brunet, 2008).
a. Влияние массы тела на выбор дозы гепарина. Хотя исследования фармакокинетики среди населения показали, что объем распределения гепарина растет с увеличением массы тела (Smith, 1998), многие диализные центры, как правило, не проводят коррекции доз гепарина для пациентов с массой тела в диапазоне от 50 до 90 кг. Другие центры корригируют как нагрузочную, так и поддерживающую дозы гепарина в соответствии с массой тела.
b. Эффект назначения пероральных антикоагулянтов на выбор дозы гепарина. В настоящее время пожилые пациенты в соответствии с современными рекомендациями все чаще принимают варфарин и новые ингибиторы фактора свертывания крови Ха (апиксабан, ривароксабан), а также прямые ингибиторы тромбина (дабигатран). Эти новые вещества выводятся в основном почками, а значит, высока вероятность их накопления в организме диализных пациентов, что увеличивает риск кровотечений. Большинство пациентов, принимающих варфарин, с МНО <2,5 нуждаются, тем не менее, в применении антикоагулянтов на диализе. Однако для тех, кто имеет металлические протезы сердечных клапанов и МНО >3,0, гепаринизации на диализе, как правило, не требуется. Аналогично пациентам, принимающим аспирин и другие антиатретанты, требуются стандартные дозы гепарина, а для пациентов с тромбоцитопенией (<50 000х106/л) введение гепарина необходимо исключить или снизить. В настоящее время мало клинических данных об антикоагулянтах нового поколения, поэтому их рекомендуется принимать с осторожностью, особенно прямые ингибиторы тромбина и Ха фактора.
c. Когда прекращать инфузию гепарина. Время полувыведения гепарина у диализных пациентов в среднем около 50 минут, хотя может колебаться от 30 минут до 2 часов. Если у пациента (со средним временем полувыведения гепарина 1 час) гепаринизация на диализе увеличивает ЧТВ или АВС на 80% от исходных значений, прекращение подачи гепарина в систему за 1 час до окончания процедуры приводит к требуемому уровню ЧТВ или АВС - на 40% выше исходных значений. При использовании венозных катетеров инфузию гепарина обычно продолжают до окончания процедуры диализа.
d. Постдиализное кровотечение из мест пункции сосудистого доступа. Если такое кровотечение происходит, помимо пересмотра дозы гепарина необходимо оценить сосудистый доступ (протез или фистулу) на наличие стеноза, так как повышенное давление в сосудистом доступе может быть причиной такого кровотечения. Следует также провести оценку правильности положения игл. Е(еправильная пункция протеза в одном и том же месте может привести к повреждению его стенки и кровотечению после удаления иглы независимо от того, как хорошо контролируется антикоагуляция.
4. Контроль тромбообразования при стандартной гепаринизации. Редкое непреднамеренное тромбирование экстракорпорального контура, вполне возможно, и не требует изменения дозы гепарина на процедуре. Однако это является поводом для выяснения причины данного события. Чаще всего причина является устранимой (например, коррекция сосудистого доступа). Технические ошибки, перечисленные в табл. 14.4, следует регулярно обсуждать и не допускать их посредствам соответствующего обучения персонала. Повторяющееся же тромбообразование в экстракорпоральном контуре требует пересмотра метода или дозы гепаринизации для данного пациента.
5. Кровотечение при стандартной гепаринизации. Повышенный риск кровотечений при обычной гепаринизации составляет 25-50% у пациентов с высоким риском ЖКК (при наличии гастрита, язвы желудка и ангиодисплазии), после недавних оперативных вмешательств, при перикардите и тромбоцитопении. Кровотечения могут затрагивать центральную нервную систему, забрюшинное пространство и средостение. Склонность к кровотечениям усиливается дефектами функций тромбоцитов и эндотелия, связанными с уремией.
В. Режим гепаринизации малой дозой
1. Общие комментарии. Режим легкой гепаринизации рекомендуется пациентам с незначительным риском развития кровотечений, но носящим хронический и затяжной характер, когда безгепариновый диализ оказался неэффективен из-за частого тромбирования. При мониторинге гепаринизации путем контроля Ч Т В или A ВС целевое время сверты вания крови (см. табл. 14.3 и кривую С на рис. 14.1) определяется как повыш енное на 40% от исходного значения. Целевое время сверты вания крови по Л и -У ай ту приведено в табл. 14.3. Если основное время Ч ТВ или A ВС пациента оказы вается больше 140% от средних исходных значений в диализном центре, лучше все ж е использовать безгепариновый диализ или метод регионарной цитратной антикоагуляции.
Таблица 14.4 Технические факторы, приводящие ктромбообразованию в экстракорпоральном контуре

2. Техника легкой гепаринизации с пониженными дозами. Введение болюса гепарина с последующей постоянной инфузией - лучший метод гепаринизации, так как позволяет избежать подъемов и падения времени свертывания крови, неизбежных при повторном болюсном введении. Алгоритм таков:
- определить исходные значения времени свертывания крови (ЧТВ или АВС);
- ввести болюс с дозой гепарина 750 ЕД;
- через 3 минуты проверить значение ЧТВ или АВС;
- если необходимо, ввести болюс повторно для достижения ЧТВ или АВС более 40% от их исходных значений;
- начать диализ с инфузии гепарина со скоростью 600 ЕД в час;
- контролировать время свертывания крови каждые 30 минут;
- установить дозу гепарина для поддержания ЧТВ или АВС на уровне более 40% от их исходных значений;
- продолжать инфузию гепарина до конца диализа.
С. Осложнения, связанные с применением гепарина. Помимо кровотечений это повышение липидов в крови, тромбоцитопения, а также повышение риска развития гипоальдостеронизма и нарастание гиперкалиемии, особенно у пациентов со значительной остаточной функцией почек. Некоторые пациенты могут жаловаться на выпадение волос.
1. Уровень липидов крови. Гепарин активирует липопротеинлипазу и тем самым может стать причиной повышения уровня триглицеридов в крови. Низкий уровень липопротеидов высокой плотности (ЛПВП) связан с высокими дозами гепарина.
2. Гепарин-индуцированная тромбоцитопения (ГИТ). Существует два типа гепарин-индуцированной тромбоцитопении. При I типе ГИТ уменьшение числа тромбоцитов зависит от времени экспозиции и дозы гепарина и отвечает на снижение дозы. При II типе ГИТ наблюдаются агглютинация тромбоцитов и парадоксальные артериальные и/или венозные тромбозы, что происходит в результате выработки антител - иммуноглобулинов G (IgG) или М (IgM) - к комплексу «гепарин - тромбоцитарный фактор 4», и чаще встречается при применении бычьего, а не свиного гепарина, и реже при использовании НМГ Учитывая частоту распространения ГИТ в недиализной популяции, остается загадкой, почему данный вид тромбоцитопении не встречается чаще у пациентов на диализе. Диагностика ГИТ второго типа осуществляется методом иммуноферментного анализа (ИФА/ELISA) на выявление антител к комплексу «гепарин - тромбоцитарный фактор 4» (АТ-ПФ4-гепарин) в сочетании с тестом на нарушение агрегации тромбоцитов.
НМГ не следует применять на диализе при наличии ГИТ, потому что часто наблюдается перекрестная реакция этих препаратов с АТ-ПФ4-гепа-рин. В качестве альтернативных антикоагулянтов можно использовать прямой ингибитор тромбина - аргатробан (Tang, 2005) и гепариноиды - данапа-роид и фондапаринукс (Haase, 2005). Варфарин не следует применять, пока число тромбоцитов не восстановится до 150 000 х 106/л, имеется риск возникновения некроза кожи и гангрены конечностей, если препарат используется в острой стадии ГИТ (Srinivasan, 2004).
3. Зуд. Гепарин может вызывать локальный кожный зуд при подкожном введении, поэтому высказывались предположения, что он может быть также причиной зуда и других аллергических реакций во время диализа. С другой стороны, НМГ используются для лечения зуда при наличии красного плоского лишая в связи с подавлением активности гепариназы Т-лимфоцитов (Hodak, 1998). Нет доказательств, что удаление гепарина из экстракорпорального контура существенно улучшает течение уремического зуда.
4. Анафилактоидные реакции - см. главу 12.
5. Гиперкалиемия. Гепарин-индуцированная гиперкалиемия как результат подавления гепарином синтеза альдостерона хорошо описана в литературе. Считается, что у диализных больных с олигурией альдостерон обеспечивает желудочно-кишечный механизм выведения калия (Hottelart, 1998).
6. Остеопороз. Длительное применение гепарина может привести к остеопорозу.
D. Безгепариновый диализ
1. Общие комментарии. Безгепариновый диализ - это метод выбора для пациентов с активным кровотечением или высоким риском его развития, а также для тех, у кого есть противопоказания к применению гепарина (например, аллергия на гепарин). Показания к безгепариновому диализу приведены в табл. 14.5. Из-за простоты и безопасности метода в настоящее время многие центры используют его у всех пациентов при проведении процедур в отделениях интенсивной терапии. Важно тщательное заполнение системы для минимального контакта крови с воздухом, что предотвращает тромбооб-разование в экстракорпоральном контуре. Необходимо также использовать наименее длинные магистрали, устранить возможные участки застоя крови или ее турбулентности, которые обычно возникают при резком изменении внутреннего диаметра просвета магистрали, а также в трехходовых коннекторах. Кроме того, охлаждение диализирующего раствора помогает снизить активацию тромбоцитов.
Таблица 14.5 Стратегия антикоагуляции: показания к диализу без гепарина

2. Процедура проведения безгепаринового диализа. Существует множество разных методик, но все они похожи на приведенную ниже.
a. Промывка экстракорпорального контура раствором гепарина (не проводится в случае имеющейся у пациента гепарин-индуцированной тромбоцитопении). Для промывки системы используется физраствор, содержащий 3000 ЕД/л гепарина, чтобы он мог покрыть внутренние поверхности магистралей и мембраны диализатора и смягчить тромбогенный ответ. Чтобы гепарин не попал в системный кровоток, необходимо вытеснить гепарин-содержащий раствор из системы либо кровью пациента, либо чистым физраствором в начале диализа.
b. Относительно высокая скорость кровотока. Скорость кровотока следует установить достаточно высокой - на уровне 300-400 мл/мин при хорошей переносимости. Если же высокая скорость противопоказана из-за риска развития дизэквилибриум-синдрома (маленький пациент, очень высокий преддиализный уровень мочевины), можно применить серию ультракоротких (например, часовых) процедур диализа с перерывами на изолированную ультрафильтрацию. Кроме того, следует попробовать использовать диализаторы с небольшой площадью мембраны и/или уменьшить скорость потока диализирующего раствора. Как правило, двухпросветные диализные катетеры способны обеспечить достаточную скорость кровотока для эффективного безгепаринового диализа.
с Периодическая промывка физраствором. Мнения по поводу этой методики противоречивы: одно из исследований показало, что периодическая промывка системы может способствовать свертыванию крови (возможно, из-за попадания пузырьков воздуха) (Sagedal, 2006). Основной целью такой промывки является возможность осмотра диализатора на наличие сгустков крови с целью своевременного прекращения диализа или замены диализатора. Также кое-кто полагает, что периодическая промывка физраствором снижает тромбообразование и уменьшает риск тромбоза.
Методика: быстро промывать диализатор 250 мл физраствора, перекрыв входную магистраль, каждые 15 минут. Частота промываний может быть снижена или увеличена по необходимости. Рекомендуется контролировать объем физраствора, используемого для промывки диализатора (и поступающего в пациента), и соответственно, корректировать объем ультрафильтрации.
d. Материал мембраны диализатора. Молекула гепарина имеет высокий отрицательный электрический заряд и может адсорбироваться на поверхности мембраны диализатора; этот эффект был использован для производства мембран с гепариновым покрытием. Сообщалось, что такие диализаторы позволяют проводить безгепариновый диализ или диализ со сниженными дозами гепарина (Evenepoel, 2007).
e. Площадь поверхности мембраны. Теоретически большая площадь поверхности мембраны ассоциируется с повышенным риском тромбообразования, особенно при низкой скорости потока крови по наружным волокнам диализатора. Дизайн диализаторов с меньшей площадью поверхности мембраны обеспечивает более высокий поток по наружным волокнам диализатора, поэтому их использование предпочтительнее.
f. Ультрафильтрация и гемодиафильтрация. Слишком высокий объем ультрафильтрации способствует гемоконцентрации и повышает риск тромбоцитарно-мембранных реакций, что приводит к тромбообразованию в диализаторе.
д. Трансфузия компонентов крови или введение липидов. Считается, что проведение трансфузий через входную магистраль экстракорпорального контура повышает риск тромбообразования во время диализа.
Е. Бикарбонатный диализирующий раствор с небольшим содержанием цитрата (Citrasate™). Небольшое количество лимонной кислоты используется вместо уксусной в качестве агента, повышающего pH. После смешивания кислотного и основного концентратов с водой полученный раствор содержит 0,8 ммоль/л (2,4 мЭкв/л) цитрата. Это небольшое количество цитрата образует с кальцием комплексное соединение, что подавляет коагуляцию крови и активацию тромбоцитов на поверхности мембраны диализатора. Это приводит к улучшению его клиренса и увеличивает кратность его повторного использования (Ahmad, 2005). Такой тип диализирующего раствора может применяться вместе с пониженной дозой гепарина или для безгепаринового диализа. Концентрация цитрата в нем достаточно низкая, так что мониторинг уровня ионизированного кальция не требуется.
V. ДРУГИЕ МЕТОДЫ АНТИКОАГУЛЯЦИИ
А. Применение низкомолекулярного гепарина (НМГ). Фракции НМГ (молекулярная массой 4000-6000 Да) получают химическим разложением, ферментацией или просеиванием исходного гепаринового сырья с молекулярной массой 200025 000 дальтон. НМГ подавляет фактор Ха, фактор ХПа и калликреин и лишь в незначительной степени тромбин и факторы IX и XI, поэтому частичное тромбопластиновое и тромбиновое время увеличиваются на 35% только в течение первого часа, а далее повышаются незначительно, что снижает риск кровотечений.
Гемодиализ с использованием НМГ в качестве единственного антикоагулянта был изучен в длительных исследованиях и показал свою безопасность и эффективность. Пролонгированный период полувыведения НМГ позволяет достичь антикоагуляционного эффекта введением одной дозы в начале диализа, хотя дробное дозирование может быть предпочтительным при продолжительных сеансах диализа. НМГ по сравнению с НФГ имеет большую биодоступность и меньшую неспецифическую способность к связыванию с эндотелием, белками плазмы и тромбоцитами. Таким образом, НМГ начинает действовать быстрее НФГ и в меньшей степени активирует тромбоциты и лейкоциты (Aggarwal, 2004), а также не способствует формированию фибринового осадка на внутренней поверхности диализатора. Учитывая, что НМГ имеет меньшую молекулярную массу, некоторая часть дозы может быть потеряна при его введении в систему до диализатора, особенно при проведении гемодиафильтрации (Sombolos, 2009).
Препараты НМГ доступны в США, но на диализе широко не используются из-за большей стоимости и регуляторных аспектов. Доза НМГ обычно выражается в единицах aXaICU (анти-Ха фактора, единицах института Шой). Имеется несколько различных НМГ, отличающихся молекулярной массой, периодом полувыведения и относительной активностью по отношению к факторам Ха и ХПа. Характеристики доступных НМГ и их средние начальные дозы приведены в табл. 14.6. Меньшие дозы следует использовать для пациентов с умеренным риском развития кровотечений. Антикоагуляционные тесты при применении НМГ рутинно не проводятся, поскольку анализ на анти-Ха активность труднодоступен. В одном предварительном исследовании набор для оценки анти-Ха активности у постели пациента показал многообещающие результаты для препарата тинзапарин (Pauwels, 2014). Потенциальные преимущества НМГ, как отмечалось ранее, включают простоту его применения и более предсказуемые результаты; НМГ могут снижать риск развития остеопороза, вызываемого длительным использованием НФГ (Lai, 2001). Европейские рекомендации по лучшей клинической практике склонны отдавать предпочтение НМГ над НФГ.
1. Анафилактические реакции на болюсное введение НМГ. Так называемый синдром первого использования (см. главу 12) наблюдается при применении не только НФГ, но и НМГ. Если у пациента имеет место подобная реакция, то она будет проявляться на любой гепарин. Из-за выраженного отрицательного заряда молекулы гепарина при прохождении гепаринизированной крови через диализатор могут образовываться брадикинин и анафилатоксины (СЗа и С5а), приводящие к гипотензии (Kishimoto, 2008). Это объясняет клинические ситуации, когда пациент с вероятной аллергией на гепарин не переносит процедуру с болюсным введением, но успешно диализируется методом постоянной инфузии гепарина (De Vos, 2000).
Таблица 14.6 Наиболее распространенные препараты НМГ

2. Кровотечения. У пациентов с ХБП, получающих НМГ, одновременный прием клопидогреля и аспирина часто осложняется кровотечениями (Farooq, 2004).
B. Гепариноиды (данапароид и фондапаринукс). Данапароид - это смесь из 84% гепарина, 12% дерматана и 4% хондроитина сульфата. Препарат действует преимущественно на фактор Ха, следовательно, проконтролировать его эффективность можно с помощью анализов на анти-Ха активность. Период полувыведения данапароида при почечной недостаточности увеличивается, так что иногда приходится проводить мониторинг его анти-Ха активности до следующей процедуры диализа. Для пациентов с массой тела более 55 кг рекомендуется нагрузочная доза данапароида 750 ME, а для пациентов с меньшей массой доза может быть уменьшена до 500 ME. Последующие дозы титрируются до достижения анти-Ха активности от 0,4 до 0,6 после болюсного введения. В 10% случаев данапароид может вступать в перекрестные реакции с ГИТ-антителами. Совсем недавно были разработаны синтетические пентасахариды, такие как фондапаринукс, которые не вступают в перекрестные реакции с ГИТ-антите-лами. Обычная преддиализная доза фондапаринукса - 2,5-5,0 мг. Поскольку препарат также имеет продолжительное время полувыведения, во избежание накопления гепариноидов в организме проводится мониторинг их анти-Ха активности для поддержания целевой преддиализной концентрации на уровне <0,2 МЕ/мл. При гемодиафильтрации увеличиваются потери как данапароида, так и фондапаринукса, поэтому может потребоваться увеличение дозы.
C. Регионарная (в высокой концентрации) цитратная антикоагуляция. Альтернативой без-гепариновому диализу может являться антикоагуляция крови в экстракорпоральном контуре путем снижения в нем концентрации ионизированного кальция (кальций необходим для процесса коагуляции). Снижение концентрации ионизирующего кальция в крови экстракорпорального контура осуществляется путем инфузии в артериальную магистраль раствора тринатриевого цитрата (который связывает кальций) и применением диализирующего раствора, не содержащего кальций. Для предупреждения возврата пациенту крови с очень низким содержанием ионизированного кальция производится обратный процесс методом инфузии хлорида кальция в венозную магистраль. Около одной трети поступившего в систему цитрата диализируется и выводится, а остальные две трети быстро метаболизируются в организме. Преимущество регионарной цитратной антикоагуляции над безгепариновым диализом состоит в следующем: а) тромбообразование наблюдается крайне редко; б) не требуется высокой скорости потока крови. Основные недостатки данного метода - необходимость обеспечения двух инфузионных систем (для цитрата и кальция) и мониторинга уровня ионизированного кальция в плазме. Из-за того что при метаболизме цитрата натрия образуется бикарбонат, уровень последнего в плазме крови значительно повышается. Поэтому регионарную цитратную антикоагуляцию следует применять с осторожностью у пациентов, склонных к алкалозу. При постоянной антикоагуляции таким методом во избежание метаболического алкалоза следует снизить уровень бикарбоната в диализирующем растворе, например, до 25 ммоль (van der Meulen, 1992). Регионарная цитратная антикоагуляция не получила широкого применения для интермиттирующего хронического гемодиализа, но достаточно популярна при продленных процедурах. Теоретически одним из преимуществ такого метода является предотвращение активации и дегрануляции тромбоцитов (Gritters, 2006).
D. Ингибиторы тромбина. Аргатробан - синтетический пептид, производный аргинина, действует как прямой ингибитор тромбина, метаболизируется в печени. Препарат лицензирован для лечения пациентов с ГИТ. Во время гемодиализа проводится его болюсное введение в количестве 250 мкг/кг с последующей инфузией 2 мкг/кг/мин или 6-15 мг/ч (Murray 2004), с титрованием дозы до достижения АЧТВ 2,0-2,5. Его инфузия, как и гепарина, должна быть прекращена за 20-30 минут до окончания диализа с целью предотвращения чрезмерного кровотечения из мест пункции фистулы. Аргатробан незначительно выводится при высокопоточном диализе или гемодиафильтрации, так как способен связываться с белками, но для пациентов с болезнями печени требуется снижение дозы (Greinachre 2008). Похожий препарат, мелагатран, использовался как антикоагулянт посредством добавления к диализирующему раствору, но эта терапия остается на стадии эксперимента (Flanigan, 2005).
Лепирудин - рекомбинантный препарат гирудина, необратимо ингибирует тромбин. Выводится из организма почками, поэтому у диализных пациентов наблюдается увеличение периода его полувыведения. Загрузочная доза лепирудина при хроническом гемодиализе - 0,2-0,5 мг/кг (5-30 мг). Препарат выводится при гемодиафильтрации и при использовании высокопроницаемых диализаторов на ГД (Benz, 2007). Считается, что у одной трети пациентов вырабатываются гирудиновые антитела, что усиливает антикоагуляционный эффект. Подбор болюсной дозы лепирудина производится путем оценки уровня АРРТг перед последующей процедурой диализа, в стремлении к показателю менее 1,5 для предотвращения его накопления. Поскольку АРРТг не коррелирует с концентрацией лепирудина в плазме, разработаны тесты для контроля терапевтической концентрации препарата на уровне 0,5-0,8 мкг/мл. Риск развития кровотечений - основной при применении лепирудина. Препарат не имеет антидота, поэтому в случае развития осложнений может потребоваться свежезамороженная плазма или концентрат фактора Vila. Лепирудин иногда может вызывать анафилактоидные реакции. Бивалирудин - прямой ингибитор тромбина, период полувыведения которого гораздо меньше, чем у лепирудина. Обычная скорость его инфузии - 1,0-2,5 мг/ч (0,009-0,023 мг/кг/ч); целевое значение АРРТг - около 1,5-2,0.
E. Простаноиды. Простациклин (PGI2) и его аналог эпопростенол - мощные антикоагулянты, блокирующие цАМФ. Препараты могут применяться для регионарной антикоагуляции на диализе у пациентов с риском кровотечений. Хотя PGI2 является сильным вазодилататором, риск гипотензии можно снизить, начав инфузию с дозы препарата 0,5 нг/кг/мин, затем постепенно увеличивая ее до 5 нг/кг/мин, переключившись после начала диализа на системную инфузию, поскольку 40% дозы теряется с диализатом.
F. Нафамостата малеат. Нафамостата малеат - ингибитор протеаз с коротким периодом полувыведения, который может применяться в качестве регионарного антикоагулянта. Наибольший опыт накоплен в Японии, сначала рекомендуется болюсное введение дозы 20 мг, а затем - инфузия, начиная со скорости 40 мг/ч с последующей корректировкой дозы для поддержания целевого значения АРРТг на уровне 1,5-2,0 или АВС в пределах 140-180 секунд.
Ссылки и рекомендуемая литература
Aggarwal A. Attenuation of platelet reactivity by enoxaparin compared with unfractionated heparin in patients undergoing haemodialysis. Nephrol Dial Transplant. 2004; 19: 1559-1563.
Ahmad S, et al. Increased dialyzer reuse with citrate dialysate. Hemodial Int. 2005; 9: 264.
Apsner R, et al. Citrate for long-term hemodialysis: prospective study of 1,009 consecutive high-flux treatments in 59 patients. Aw I Kidney Dis. 2005; 45: 557.
Benz K, et al. Hemofiltration of recombinant hirudin by different hemodialyzer membranes, implications for clinical use. Clin I Am Soc Nephrol. 2007; 2: 470-476.
Brunet P, et al. Pharmacodynamics of unfractionated heparin during and after a haemodialysis session. Am J Kidney Dis. 2008; 51: 789-795.
Caruana RJ, et al. Heparin-free dialysis: comparative data and results in high-risk patients. Kidney Int. 1987; 31: 1351.
De Vos JY, Marzoughi H, Hombrouckx R. Heparinisation in chronic haemodialysis treatment: bolus injection or continuous homogeneous infusion? EDTNA ERCA I. 2000; 26 (1): 20-21.
European Best Practice Guidelines. V.1-V.5 Hemodialysis and prevention of system clotting (V.l and V.2); prevention of clotting in the HD patient with elevated bleeding risk (V.3); heparin-induced thrombocytopenia (V.4); and side effects of heparin (V.5). Nephrol Dial Transplant. 2002; 17 (suppl 7): 63.
Evenepoel P, et al. Hep ar in-coated polyacrylonitrile membrane versus regional citrate anticoagulation: a prospective randomized study of 2 anticoagulation strategies in patients at risk of bleeding. Am I Kidney Dis. 2007;49:642-649.
Farooq V, et al. Serious adverse incidents with the usage of low molecular weight heparins in patients with chronic kidney disease. Am I Kidney Dis. 2004; 43: 531.
Flanigan MJ. Melagatran anticoagulation during haemodialysis - ’Primum non nocere’. Nephrol Dial Transplant. 2005; 20: 1789.
Frank RD, et al. Factor Xa-activated whole blood clotting time (Xa-ACT) for bedside monitoring of dalteparin anticoagulation during haemodialysis. Nephrol Dial Transplant. 2004; 19: 1552.
Gotch FA, et al. Care of the patient on hemodialysis. In: Cogan MG, Garovoy MR, (eds). Introduction to Dialysis, 2nd ed. New York, NY: Churchill Livingstone; 1991.
Gouin-Thibault I, et al. Safety profile of different low-molecular weight heparins used at therapeutic dose. Drug Sdf 2005; 28: 333.
Greaves M. Control of anticoagulation subcommittee of the scientific and standardization committee of the International Society of Thrombosis and Haemostasis: limitations of the laboratory monitoring of heparin therapy. Scientific and standardization committee communications on behalf of the control of anticoagulation subcommittee of the scientific and standardization committee of the International Society of Thrombosis and Haemostasis. Thromb Haemost. 2002; 87: 163-164.
Greinacher A, Warkentin ТЕ. The direct thrombin inhibitor hirudin. Thromb Haemost. 2008; 99: 819-829.
Gritters M, et al. Citrate anticoagulation abolishes degranulation of polymorphonuclear cells and platelets and reduces oxidative stress during haemodialysis. Nephrol Dial Transplant. 2006; 21: 153.
Haase M, et al. Use of fondaparinux (ARIXTRA) in a dialysis patient with symptomatic heparin-induced thrombocytopaenia type II. Nephrol Dial Transplant. 2005; 20: 444.
Handschin AE, et al. Effect of low molecular weight heparin (dalteparin) and fondaparinux (Arixtra) on human osteoblasts in vitro. Br I Surg. 2005; 92: 177.
Hemmelder MH, et al. Heparin lock in hemodialysis catheters adversely affects clotting times: a comparison of three catheter sampling methods [Abstract]. J Aw Soc Nephrol. 2003; 14:729A.
Ho G, et al. Use of fondaparinux for circuit patency in hemodialysis patients. Aw I Kidney Dis. 2013; 61: 525526.
Hodak E, et al. Low-dose low-molecular-weight heparin (enoxaparin) is beneficial in lichen planus: a preliminary report. I Am Acad Dermatol. 1998; 38: 564.
Hottelart C. Heparin-induced hyperkalemia in chronic hemodialysis patients: comparison of low molecular weight and unfractionated heparin. Artif.Organs. 1998; 22: 614-617.
Kishimoto TK, et al. Contaminated heparin associated with adverse clinical events and activation of the contact system. N Engl I Med. 2008; 358: 2457-2467.
Krummel T, et al. Haemodialysis in patients treated with oral anticoagulant: should we heparinize? Nephrol Dial Transplant. 2014; 29: 906-913.
Lai KN, et al. Effect of low molecular weight heparin on bone metabolism and hyperlipidemia in patients on maintenance hemodialysis. Int J Artif Organs. 2001; 24: 447.
Lim W, et al. Safety and efficacy of low molecular weight heparins for hemodialysis in patients with end-stage renal failure: a meta-analysis of randomized trials. J Am Soc Nephrol. 2004; 15: 3192.
McGill RL, et al. Clinical consequences of heparin-free hemodialysis. Hemodial Int. 2005; 9: 393.
Molino D, et al. In uremia, plasma levels of anti-protein C and anti-protein S antibodies are associated with thrombosis. Kidney Int. 2005; 68: 1223.
Murray PT, et al. A prospective comparison of three argatroban treatment regimens during hemodialysis in end-stage renal disease. Kidney Int. 2004; 66: 2446.
Olson JD, et al. College of American Pathologists Conference XXXI on laboratory monitoring of anticoagulant therapy: laboratory monitoring of unfractionated heparin therapy. Arch Pathol Lab Med. 1998; 122: 782-798.
Ouseph R, et al. Improved dialyzer reuse after use of a population pharmacodynamics model to determine heparin doses. Am I Kidney Dis. 2000; 35: 89.
Pauwels R, et al. Bedside monitoring of anticoagulation in chronic haemodialysis patients treated with tinzapa-rin. Nephrol Dial Transplant. 2014; 29: 1092-1096.
Sagedal S, et al. Intermittent saline flushes during haemodialysis do not alleviate coagulation and clot formation in stable patients receiving reduced doses of dalteparin. Nephrol Dial Transplant. 2006; 21: 444.
Schwab SJ, et al. Hemodialysis without anticoagulation: one year prospective trial in hospitalized patients at risk for bleeding. Am I Med. 1987; 83: 405.
Smith BP, et al. Prediction of anticoagulation during hemodialysis by population kinetics in an artificial neural network. Artif Organs. 1998; 22:731.
Sombolos KI, et al. The anticoagulant activity of enoxaparin sodium during on-line hemodiahltration and conventional haemodialysis. Haemodial Int. 2009; 13: 43-47.
Srinivasan AF, et al. Warfarin-induced skin necrosis and venous limb gangrene in the setting of heparin-induced thrombocytopenia. Arch Int Med. 2004; 164: 66.
Tang IY, et al. Argatroban and renal replacement therapy in patients with heparin-induced thrombocytopenia. Ann Pharmacother. 2005; 39: 231.
Van Der Meulen J, et al. Citrate anticoagulation and dialysate with reduced buffer content in chronic hemodialysis. Clin Nephrol. 1992; 37: 36-41.
Wright S, et al. Citrate anticoagulation during long term haemodialysis. Nephrology (Carlton). 2011; 6: 396-402.
Zhang W, et al. Clinical experience with nadroparin in patients undergoing dialysis for renal impairment. Hemodial Int. 2011; 15: 379-394.
