- Диализному врачу
- 1. Ведение пациентов с ХБП 4-5-й стадии.
- 2. Подготовка к трансплантации, диализу или к консервативной терапии
- 3. Физиологические принципы и моделирование кинетики мочевины
- 4. Оборудование для гемодиализа и расходные материалы
- 5. Вода для диализа и диализирующий раствор
- 6. Артериовенозные фистулы и протезы. Основные положения
- 7. Центральный венозный катетер в качестве доступа: основы
- 8. Мониторинг артериовенозного доступа и осложнений
- 9. Инфекции и другие осложнения центральных венозных катетеров
- 10. Назначение острого гемодиализа
- 11. Назначение хронического гемодиализа
- 12. Осложнения в ходе процедуры гемодиализа
- 13. Повторное использование диализаторов
- 14. Антикоагуляция
- 15. Продленная заместительная почечная терапия
- 16. Гемодиафильтрация
- 17. Терапевтический аферез
- 18. Актуальность сорбционных технологий сегодня
- 19. Руководство по диализу
Артериовенозные фистулы и протезы. Основные положения
I. ВВЕДЕНИЕ: ТИПЫ СОСУДИСТОГО ДОСТУПА. Артериовенозные (AV) фистулы и протезы являются типичным сосудистым доступом для программного гемодиализа. Формирование AV-фистулы включает создание анастомоза между артерией и веной, что позволяет крови протекать непосредственно из артерии в вену. Традиционно анастомоз создается на предплечье между лучевой артерией и головной веной. Хотя возможно множество вариаций: анастомоз в анатомической табакерке, на предплечье, в области локтевого сгиба или на плече. AV-протез аналогичен фистуле за исключением расстояния между питающей артерией и веной, которые соединены трубкой из материала протеза. Наиболее часто используемым материалом является политетрафторэтилен. Третьим типом доступа является перманентный венозный катетер с муфтами, который обсуждается в соответствующей главе.
AV-фистула не может использоваться немедленно после создания, поскольку ее созревание требует от 6 до 8 недель. В ходе созревания кровоток по вновь созданной фистуле прогрессивно увеличивается вследствие расширения как артерии, так и вены. Ремоделирование (утолщение стенки фистульной вены), индуцируемое давлением и кровотоком, укрепляет стенку фистулы и ограничивает повреждение стенки и гематомы в зоне пункции диализной иглой, тогда как расширение вены облегчает будущие пунктирования. Протез может использоваться раньше фистулы, как правило, через 1-3 недели после установки.
Хорошо функционирующая фистула остается предпочтительным сосудистым доступом в сравнении с протезом благодаря более низкой частоте инфекции, лучшему сохранению проходимости и общему улучшению выживаемости пациентов. Однако AV-фистула несет в себе проблемы, важной из них является медленное созревание при неудовлетворительном состоянии сосудов, в частности, у пожилых пациентов. Протез может быть лучшим выбором у пациентов со слабо развитой сосудистой системой. При продолжительном использовании протеза происходит расширение вен ниже по кровотоку; иногда эти вены можно использовать для создания AV-фистулы, переводя протез в фистулу.
А. Неоинтимальная гиперплазия. Протез является менее приемлемым сосудистым доступом, чем фистула, поскольку создает больший риск неоинтимальной гиперплазии. Она развивается в венозном сегменте, следующем за анастомозом «протез-вена». Гиперплазия сужает просвет вены, приводя к ухудшению кровотока и продолжительному кровотечению после удаления диализных игл из-за возрастания давления внутри протеза. В конечном счете это приводит к тромбозу протеза. Причиной ускоренной неоинтимальной гиперплазии считается турбулентный поток в анастомозе и несоответствие в податливости давлению в относительно жестком протезе и более растяжимой вене. Воздействие активированной в ходе сеанса крови может ускорять этот процесс, хотя стеноз в протезе может развиваться и в отсутствие его использования для диализа.
Хотя протез уступает созревшей фистуле в качестве сосудистого доступа, он имеет преимущество перед центральным венозным катетером. Пациенты с фистулами и протезом менее подвержены инфекции, имеют более низкую коморбидность и лучшую выживаемость, чем пациенты с венозными катетерами. Недавно худшие результаты при использовании центральных катетеров связали с предвзятостью отбора (венозные катетеры часто устанавливаются у более коморбидных пациентов), а риск инфицирования венозных катетеров, особенно у пациентов пожилого возраста, оказался относительно низким. Таким образом, в определенных обстоятельствах, обсуждаемых в следующей главе, центральный венозный катетер остается полезным вариантом сосудистого доступа.
II. КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ СТАВЯТ ЦЕЛЬЮ РАСШИРЕНИЕ ИСПОЛЬЗОВАНИЯ AV-фИСТУЛЫ. Рекомендации KDOQI и инициатива Fistula First (см. web-ссылки) побуждают к созданию AV-фистулы, ставя целью ее использование как минимум у 68% пациентов на диализе. Раннее обращение пациентов с ХБП к нефрологу до старта гемодиализа предоставляет необходимое время для создания AV-фистулы. Это исключает риски, связанные с центральным венозным катетером, который требуется при позднем обращении непосредственно перед стартом диализа. Недавно был предложен экстренный старт перитонеального диализа как начальный метод лечения для пациентов, экстренно нуждающихся в нем. Такой подход позволяет стабилизировать состояние пациента без использования хронического венозного катетера. Одним из ключевых факторов, способствующих увеличению доли AV-фистул, является наличие обученного и квалифицированного сосудистого хирурга, работающего в составе команды.
За последние десятилетия после реализации правительственной программы Fistula First использование фистул в США возросло с 26% до 61%. Многие центры в США и Европе достигли несравненно большей доли (более 90%). В США, однако, частота использования центральных венозных катетеров не снизилась в той мере, как планировалось, что привело к видоизменению целей инициативы Fistula First на Fistula First and catheter last («На первом месте - фистула, на последнем месте -катетер»).
III. ПОДГОТОВКА СОСУДОВ. У пациентов с прогрессирующей ХБП, ожидающих начала диализа, подкожные глубокие вены на обеих руках следует защищать в ожидании их возможного использования в качестве сосудистого доступа. Соответственно, следует минимизировать пункцию вен и установку периферических инфузионных катетеров на верхних конечностях, особенно в головную вену и в сгибе локтя с обеих сторон. В качестве венозного доступа можно использовать вены на кисти, если это возможно. В связи с риском центрального венозного стеноза не следует использовать подключичные вены, если в этом нет абсолютной необходимости, равно как следует отказаться и от подкожно устанавливаемых центральных венозных магистралей. Лучевую и плечевую артерии следует сохранять для будущего сосудистого доступа; соответственно, эндоваскулярные чрескожные интервенции не следует проводить через эти артерии. Установки эндоваскулярных электродов для имплантируемых кардиальных устройств следует избегать, поскольку это может негативно сказаться на проходимости сосудов. Кроме того, долгосрочный риск инфекции также может оказаться высоким. Вместо этого у пациентов с ХБП, требующих установки водителя ритма или подобных устройств, целесообразно рассмотреть эпикардиальный подход или подкожную установку электродов.
А. Проект Американской ассоциации нефрологических сестер «Сохрани вену». Эта организация имеет веб-сайт, предлагающий пациент-ориентированную брошюру на английском или испанском языке, описывающую необходимость сохранения вен. Веб-сайт также предлагает пациентам возможность получить браслет с надписью: «Сохраняйте вены. Не используйте для внутривенных введений и забора крови».
IV. ПЛАНИРОВАНИЕ AV-ДОСТУПА
A. Обучение пациента и вопросы времени. Для пациентов со скоростью клубочковой фильтрации (СКФ) меньше 30 мл/мин следует провести обучение в отношении модальностей заместительной почечной терапии, включая перитонеальный диализ и трансплантацию. Пациентам, выбравшим гемодиализ, фистулу следует наложить по меньшей мере за 6 месяцев до планируемого начала диализа. Для пациентов, выбравших перитонеальный диализ, создание AV-фистулы является опцией. Такая резервная фистула иногда создается, чтобы исключить риски, связанные с центральным венозным катетером, если перитонеальный диализ придется на время остановить, например, для замены катетера или из-за нарушения функции или тяжелого перитонита. Однако число перитонитов в настоящее время существенно ниже, чем в прошлом, поэтому большинство центров более не создают резервных фистул. Пациентов, планирующих получить пересадку почки от живого донора в ближайшем будущем, но не требующих диализа, в течение короткого времени можно вести без перманентного доступа. У таких пациентов адекватным является краткосрочное (меньше 6 месяцев) использование перманентного катетера при отсутствии противопоказаний, таких как клапанный порок сердца, предрасполагающий к эндокардитам.
B. Предсказание потребности в диализе. Определить ожидаемое время потребности в диализе не всегда простая задача. Преждевременное создание доступа является, возможно, не всегда обоснованным ресурсом, и многие пожилые пациенты погибают до начала диализа. Один из инструментов, предсказывающий потребность в диализной терапии, разработан Tangri (2011, 2013), хотя это уравнение предсказывает риск развития т-ХПН во временном интервале в три года. Аналогичное предсказательное уравнение, построенное на пациентах мужского пола, ветеранах армии США, было разработано Drawz (2013). Оно предсказывает риск т-ХПН в течение одного года.
V. ПРЕДОПЕРАЦИОННОЕ ОБСЛЕДОВАНИЕ
А. Анамнез. Требуется тщательный сбор анамнеза, особенно в отношении установки центральных венозных катетеров, водителей ритма, подкожных центральных катетеров и сосудистой хирургии. Сопутствующая патология в виде хронической сердечной недостаточности, сахарного диабета или периферической болезни сосудов может ограничить возможность создания сосудистого доступа. Пациенты с тяжелой сердечной недостаточностью могут не перенести дополнительное увеличение сердечного выброса, требующееся для циркуляции крови по доступу. Пациенты с тяжелыми сосудистыми болезнями вследствие атеросклероза или диабета или пациенты с выраженным повреждением вен на руках или AV-фистулами в прошлом могут не иметь адекватных сосудов для создания AV-доступа. Хотя и у таких пациентов AV-фистулу можно создать на верхних конечностях, используя инновационные хирургические техники.
B. Физикальное обследование. Следует проверить и зафиксировать пульс на всех артериях верхней конечности, измерить артериальное давление на обеих руках. Разницу в давлении на двух руках следует рассматривать как нормальную при величине менее 10 мм рт. ст., пограничную - в диапазоне в 10-20 мм рт. ст. и проблемную - больше 20 мм рт. ст. Тест Allen, который оценивает коллатерали между лучевой и локтевой артериями по ладонной арке, выполняется или при физикальном обследовании, или при помощи допплер-УЗИ (см. ниже). Чувствительность теста Allen можно увеличить, комбинируя его с пульс-оксимет-рией (Paul and Feeny, 2003). Детали того, как проводить тест Allen, приведены в табл. 6.1. Пациента следует осмотреть на признаки ранее существовавших центральных катетеров, наличие травм или хирургических вмешательств на руках, грудной клетке, шее, включая предшествующие попытки создания ААдоступа. Наличие отека руки, коллатеральных вен, различие в размерах конечностей должно побудить к обследованию центральных вен.
C. Визуализирующие исследования. Рутинное предоперационное картирование руки для оценки вен и артерий помогает в выборе наиболее адекватного подхода и места создания доступа. Использование визуализирующих исследований продемонстрировало увеличение частоты установки хорошо функционирующих фистул.
1. Допплер-УЗИ. Это исследование, которое может оценить скорость кровотока и внутренний диаметр артерий и периферических вен, следует проводить всем пациентам для определения подходящих для создания доступа артерий и вен. Плохая визуализация центральных вен при допплер-УЗИ является ограничением метода. Лучше всего исследование проводить в операционной после региональной анестезии, поскольку после применения анестезии вены несколько расширяются; в обычных условиях вены могут быть сужены и не визуализироваться в достаточной мере.
а) Минимальный размер артерий и вен. Существует противоречивое мнение в отношении питающей артерии и вены для успешного функционирования доступа. Исследования показывают, что просвет вены должен быть не меньше 2,5 мм (Okada and Shenoy, 2014), а минимальный диаметр артерии составляет 2,0 мм. Меньшие «пограничные» размеры сосудов от 1,5 мм (для артерий и вен) используются для успешного создания фистул, но требуют участия квалифицированного хирурга (Pirozzi, 2010). Более важным критерием может оказаться способность артерий и вен расширяться после наложения анастомоза, что позволяет кровотоку увеличиваться.
Таблица 6.1 Тест Allen (тест на проходимость ладонной дуги)
1. Посадите пациента к себе лицом с вытянутой рукой ладонью вверх
2. Пережмите лучевую и локтевую артерии на запястье
3. Сохраняя прижатие артерий, попросите пациента повторно сжимать и разжимать кулакдо побеления ладоней
4. Когда ладони побелеют, отпустите локтевую артерию и наблюдайте за ладонью, станет ли она розовой.
Затем отпустите лучевую артерию
5. Повторите шаги 2-4 для лучевой артерии
Интерпретация. Если розовая окраска ладоней возвращается при отпускании артерии, это указывает на ее проходимость и отражает адекватный кровоток. Сохранение бледности в течение 5 секунд и более означает положительный результат теста на недостаточность кровотока по артерии
Модифицировано из: Beathard GD. A practicioner's resource guide to physical examination of the vascular access. ESRD Network of Texas. http://www.esrdnetl5.org/QI/C5D.pdf.
b) Тест расширения вен. Во время допплер-УЗИ проксимальная вена пережимается жгутом; при этом фиксируется увеличение размера. Средняя величина этого увеличения в 50% связана с успешным исходом (Malovrh, 2002).
c) Тест расширения артерий. Во время допплер-УЗИ исследуется профиль пульса на артерии. В норме он трехфазный в результате периферического сопротивления. Пациента просят сжать кулак на 2 минуты и затем разжать. В результате ответ в виде гиперемии переводит трехфазный профиль пульса в двухфазный у пациентов, способных к нормальной дилатации артерий.
d) Картирование. Системы головной и локтевой вены следует оценить на предмет непрерывности от отсутствия стриктур. Некоторые хирурги производят картирование с наложенным проксимальным жгутом для расширения и лучшего выявления вен, удобных для создания фистулы.
2. Венография. Венографию следует резервировать для оценки центральных вен, особенно у пациентов с трансвенозной установкой водителя ритма, отеками верхних конечностей, коллатеральными венами вокруг плеча или грудной клетки и/или неодинаковыми размерами конечностей. Для проведения венографии используется 30 мл (или меньше) неионного контраста низкой осмолярности, разведенного в соотношении 1:4 для предотвращения нефротоксичности. Неразведенный контраст обычно не требуется для венографии. Венография сама по себе не помогает в оценке артериального дерева.
3. Артериография. Атериография показана при отчетливом снижении или отсутствии пульса в предпочтительной зоне или при разнице в артериальном давлении на двух руках больше чем 20 мм рт. ст.
VI. ВОЗМОЖНОЕ РАСПОЛОЖЕНИЕ ФИСТУЛЫ НА ВЕРХНИХ КОНЕЧНОСТЯХ (См. обзор Okada and Shenoy (2014) - табл. 6.2)
А. Фистула на предплечье. AV-фистулы можно разделить на обычные и транспонированные, в зависимости от соединения артериальной и венозной систем. Обычная фистула создается соединением поверхностной артерии и вены и обычно не требует значимой иммобилизации сосудов. Транспонированная фистула использует более глубокую вену и требует ее перемещения в подкожный туннель для облегчения пункции иглой. В сравнении с обычными фистулами транспонированные являются технически более сложными и требуют большего времени для заживления. Обычная AV-фистула создается, как правило, в рамках одной хирургической процедуры, тогда как транспонированная может потребовать второго этапа.
Как минимум девять возможных мест для создания фистулы можно использовать на верхней конечности. Фистула в анатомической табакерке является дистальным вариантом лучеголовной фистулы, создаваемой между коротким и длинным сухожилиями экстензора большого пальца. Классическая лучеголовная фистула на запястье Brescia-Cimino (рис. 6.1) формируется на недоминантной руке и является предпочтительным доступом. Другие фистулы на предплечье, такие как соустье между локтевой артерией и базилярной веной, могут рассматриваться при невозможности создания лучеголовной фистулы. Перед рассмотрением плечевой фистулы следует оценить возможность создания транспонированных фистул на предплечье, например, головная вена на предплечье к проксимальному участку лучевой или плечевой артерии; транспонированная базилярная вена предплечья к лучевой или плечевой артериям. Если создание фистулы на предплечье невозможно, что нередко бывает у пациентов с сахарным диабетом и пожилых пациентов с атеросклерозом, возможными опциями являются: проксимальная часть плечевой артерии - головная вена (рис. 6.2); транспонированная базилярная вена - плечевая артерия (рис. 6.3). Менее типичными возможностями являются фистула Gracz, использующая перфорирующую вену, через которую артериолизируются головная и базилярная вена на предплечье, и плечевая двунаправленная головная фистула (артериолизация головной вены на предплечье и плече). Использование перфорирующей вены было модифицировано (Коппег, 1999). Если все места на недоминантной руке исчерпаны, используется доминантная рука.
Таблица 6.2 Места создания артериовенозной фистулы на верхних конечностях
Типичные В анатомической табакерке(наиболее дистальная)
Лучеголовная (радиоцефальная) или Brescia-Cimino (лучевая артерия с головной веной предплечья на запястье)
Локтевая артерия с базилярной веной предплечья (менее типично)
Плечевая артерия с головной веной (на локтевом сгибе)
Транспонированные
Базилярная вена предплечья к лучевой артерии на запястье
Базилярная вена предплечья к плечевой артерии (конфигурация петли)
Головная вена предплечья к плечевой артерии (конфигурация петли)
Перенесенная базилярная вена в верхней части плеча к плечевой артерии
Перфорирующие вены в проксимальной части предплечья к проксимальной части лучевой артерии (модификация Коппег для фистулы Gracz)
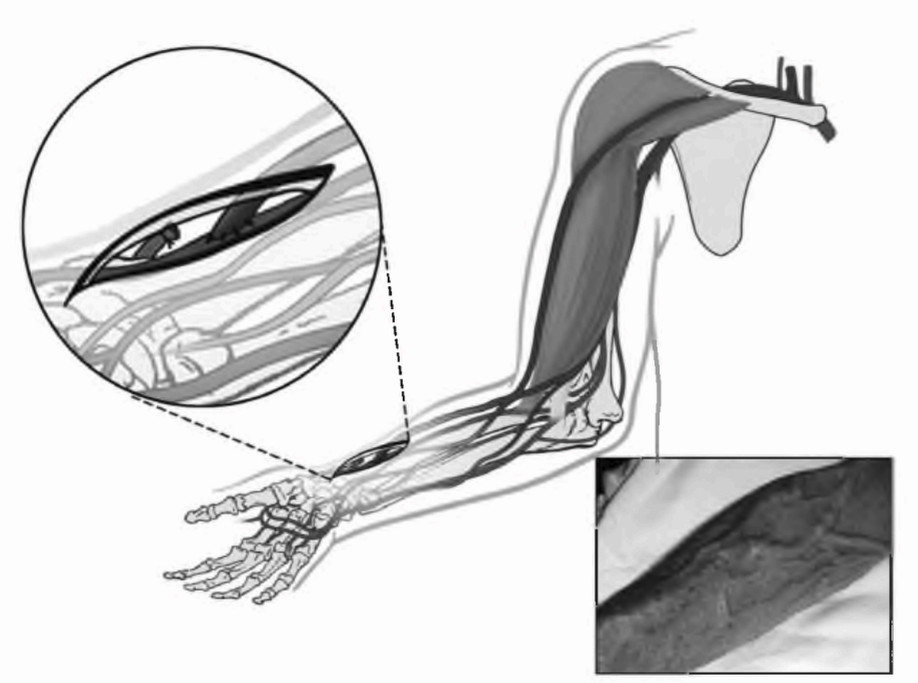
РИСУНОК 6.1. Лучеголовная (радиоцефальная) артериовенозная фистула. Воспроизведено с разрешения из Atlas of Dialysis Vascular Access - http://www.fistulafirst.org
1. Первоначальное использование локтевой перфорирующей вены у пожилых пациентов или пациентов с коморбидностью. У таких пациентов часто находят кальцинированную лучевую артерию с маленьким просветом и толстой стенкой; фистула, питаемая такой артерией, вероятно, будет плохо функционировать. В одном небольшом исследовании (Palmes, 2011) фистула на предплечье у таких пациентов создавалась только если лучевая и локтевая артерии были больше 2 мм диаметром на запястье и не было выявлено кальцификации и сегментарного сужения. Кроме того, диаметр головной вены под наложенным жгутом должен был составлять больше 2,5 мм. В противном случае, если перфорирующая вена присутствовала в локтевом сгибе, а плечевая артерия и головная вена были подходящего диаметра, создавалась AV-фистула на перфорирующей вене в локтевом сгибе с использованием модификации Коппог (см. выше) или подхода Gracz. В группе пожилых пациентов с плохими сосудами при таком подходе проходимость фистул через 24 месяца составляла впечатляющие 78%.
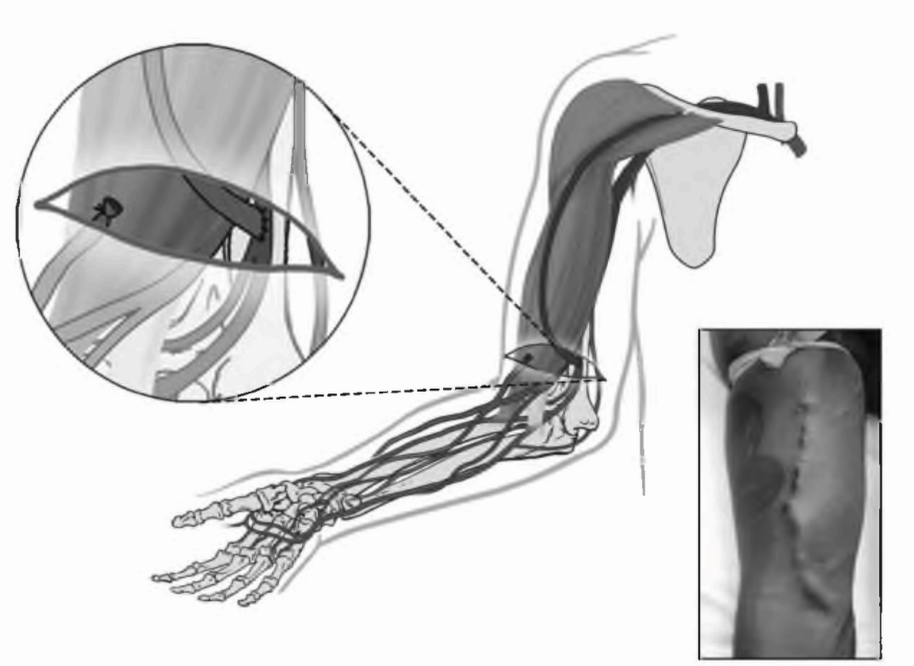
РИСУНОК 6.2. Плечеголовная (брахиоцефальная) артериовенозная фистула. Воспроизведено с разрешения из Atlas of Dialysis Vascular Access - http://www.fistulafirst.org
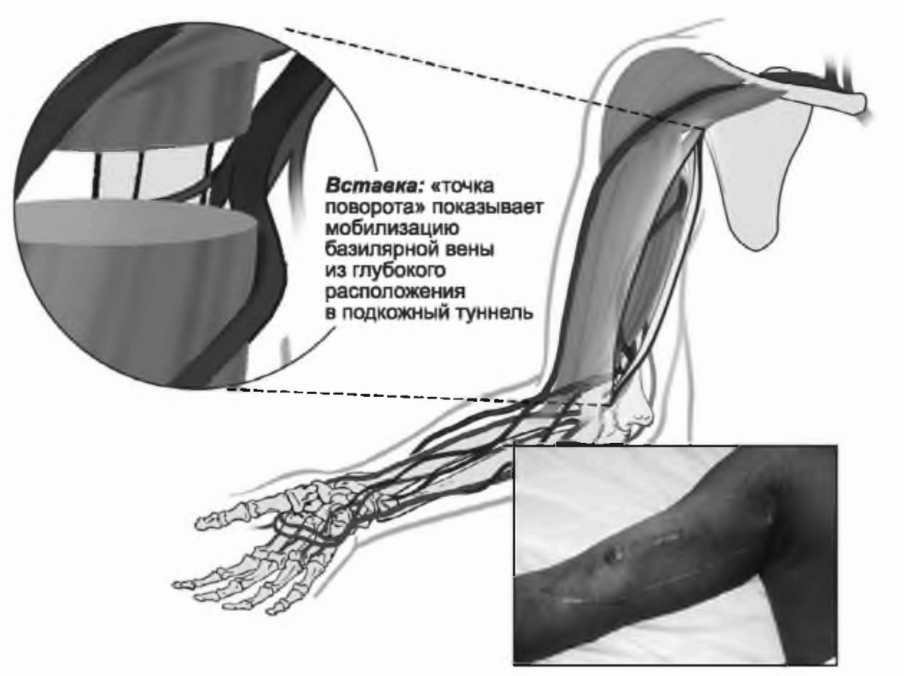
РИСУНОК 6.3. Артериовенозная фистула с базилярной веной, перенесенной к плечевой артерии. Воспроизведено с разрешения из Atlas of Dialysis Vascular Access - http://www.fistulafirst.org
B. Фистулы на ноге. AV-фистулы на ниж них конечностях создаю тся редко из-за большей частоты осложнений и худш их исходов, но они остаю тся опцией, если все потенциальные места на верхних конечностях исчерпаны. Возм ож ны м и м естами создания являю тся фистулы, соединяющие поверхностную бедренную артерию и бедренную вену или подкожную вену и подколенную артерию.
C. Синдром обкрадывания вследствие размещения фистулы на той же стороне, что и коронарный протез. В настоящее время у таких пациентов AV-фистулу следует формировать на противоположной руке для предотвращ ения этой проблемы (Coskun, 2013).
VII. оперативная процедура создания AV-фистулы. Операция по созданию AV-фистулы обычно производится в операционной под местной анестезией. А настомоз обы чно мож ет быть по типу или «бок артерии в бок вены», или «бок артерии в конец вены». В обоих случаях дистальный кровоток по артерии сохраняется. При использовании метода «бок в бок» иногда большее давление мож ет передаваться в дистальную вену, вы зы вая отек и так назы ваемы й синдром красной руки. А настом оз «бок артерии в конец вены» предотвращ ает венозную гипертензию в руке, поскольку дистальный участок вены перевязы вается. Детали оперативной техники вы ходят за границы этой книги. Важно подчеркнуть, что формирование AVфистулы - это не та процедура, которую можно доверить малоопытным хирургам, но операция, которую следует вы полнять хирургу с большим опытом и интересом к выполнению этих иногда слож ны х и проблемных операций.
A. Измерение кровотока по лучевой артерии во время операции. Обычно кровоток по лучевой артерии составляет 2 0 -3 0 мл/мин, но увеличивается до 2 0 0 -3 0 0 мл/мин немедленно после создания анастомоза (Konner, 1999). В одном из исследований измеренный кровоток сразу после операции меньш е 120 мл/мин предсказывал последующую несостоятельность фистулы.
B. Прогнозирование созревания фистулы вычислительными алгоритмами. Группа исследователей разработала алгоритм предсказания конечного кровотока по фистуле для различны х типов фистул, базируясь на демографических данных и предоперационных измерениях диаметра сосудов и кровотоков (Caroli, 2013). Этот алгоритм еще не используется клинически широко.
VIII. ПЕРИОПЕРАТИВНАЯ ПОМОЩЬ И СОЗРЕВАНИЕ ФИСТУЛЫ. Некоторые центры готовят пациента к созданию AV-фистулы, предлагая пациентам в течение нескольких недель перед операцией давать физическую нагрузку на руку, предполагая, что это может увеличить диаметр вен до требуемого размера в 2,5 мм. После операции руку следует держать в приподнятом состоянии. Следует избегать плотного бинтования руки. Физические упражнения (кистевой эспандер) могут помочь увеличить кровоток и давление в фистуле; считается, что это помогает созреванию фистулы, хотя эта концепция никогда не была подтверждена в рандомизированных исследованиях. Фистулу никогда не следует использовать для венопункции. Кровоток по фистуле следует проверять ежедневно, а в начале чаще, по пальпаторному ощущению шума над местом анастомоза или аускультацией. Врачи, сестры, технический персонал и даже хорошо информированные пациенты должны уметь провести физикальное обследование фистулы. Основы физикального обследования доступа описаны ниже в настоящей главе.
A. Правило шестерок. Все новые фистулы необходимо обследовать в течение 4-6 недель от момента создания на предмет созревания. Ко времени планируемого использования диаметр вены должен быть как минимум 6 мм. Созревшая фистула должна соответствовать «правилу шестерок». Она должна быть 6 мм в диаметре, располагаться на глубине не более 6 мм под кожей, иметь кровоток как минимум 6 мл в минуту и включать в себя прямой сегмент, доступный для пункции как минимум 6 см длиной. Как правило, созревание фистулы должно закончиться к шести неделям после операции.
B. Детали созревания фистулы. Опытный и хорошо тренированный исследователь может клинически разделить созревшую и несозревшую фистулу. Фистуле необходимо дать время для созревания, поскольку попытки пункции несозревшей фистулы могут повлечь за собой гематомы, сдавление сосуда и необратимую потерю фистулы. Первичная невозможность созревания фистулы может быть результатом атеросклеротического повреждения артерии, неадекватного анастомоза, неспособности артерии и/или вены расшириться из-за повреждения сосуда, например, из-за сосудистой кальцификации или склероза. Одной из устранимых причин является наличие множественных ветвей вены, дренирующей фистулу. По этим ветвям может оттекать значительная часть кровотока, ограничивая поток по основному каналу. Перевязка боковых ветвей может обеспечить или ускорить процесс созревания. Если фистула не может быть пунктирована или обеспечить диализную терапию больше чем через 6 месяцев, следует выполнить фистулограмму, для того чтобы найти источник проблем.
IX. ПЕРВОЕ ПРОБНОЕ ПУНКТИРОВАНИЕ НОВОЙ ФИСТУЛЫ. Если физикальное обследование указывает на адекватное созревание фистулы, следующим шагом является пробная пункция.
A. День недели. По возможности пробную пункцию следует выполнить в междиализный день. Это исключит возможные осложнения, связанные с применением гепарина. Если пробное пунктирование невозможно, лучше начинать пункции нового доступа в середине недели. Это помогает минимизировать такие проблемы, как перегрузка жидкостью, нарастание азотемии после длинного междиализного интервала.
B. Техника заполненной иглы. Для того чтобы убедиться, что игла установлена правильно, ее расположение следует подтвердить промыванием физраствором перед подсоединением игл к системе магистралей. Получения крови из иглы недостаточно для подтверждения правильного положения иглы. Одной из возможностей проверки правильного положения иглы является использование заполненной иглы. Из иглы шприцем с физраствором вытесняется воздух, и если игла правильно не расположена в сосуде, безопаснее введение под кожу физраствора, чем крови. Заполненная игла также предотвращает разбрызгивание крови, как в случае, если пункция проводится сухой иглой, а колпачок открывается, чтобы заполнить иглу кровью. Открывание колпачка создает риски попадания крови на персонал и пациентов.
C. Игла с обратным отверстием. Иглы с обратным отверстием напротив среза всегда следует использовать в качестве артериальных для увеличения кровотока из доступа и снижения риска прилипания иглы к стенке сосуда.
D. Выбор размера иглы. Выбор размера иглы для начального пунктирования является критичным. Визуальное и тактильное исследование позволяет персоналу определить размер иглы, наиболее соответствующий размеру сосуда. Можно приложить иглу размера 17G или 16G над местом будущей пункции (оставляя колпачок на иголке) и сравнить размер вены и иглы с наложенным жгутом и без него. Если размер иглы больше, чем вена при наложенном жгуте, ее использование может привести к гематоме в процессе пунктирования. Е1еобходимо использовать иглу размером равным или меньшим, чем вена (без жгута). Как правило, для начального пунктирования используют самые маленькие из доступных игл (например, 17G). Следует помнить, что при использовании такой иглы кровоток будет ограничен.
Мониторинг давления перед насосом необходим, чтобы убедиться, что скорость кровотока не превышает возможности иглы. Давление не должно быть меньше -250 мм рт. ст. Основываясь на производительности фистулы с иглой 17G, можно сделать вывод о возможности увеличить размер иглы. Как правило, игла 17G обеспечит кровоток не более 250 мл в минуту, a 16G - 350 мл в минуту. Движение от иглы 17G к большим размерам зависит от адекватности размера сосуда и кровотока по нему.
E. Процедура начального пунктирования
1. Е(аложите жгут.
2. Дезинфицируйте место пункции по протоколу центра.
3. Присоедините к игле 10 мл шприц, заполненный 8 мл физраствора, но не заполняйте иглу до момента непосредственно перед пункцией.
4. Сожмите иглу за крылышки и заполните ее физраствором, пока воздух не будет вытеснен. Закройте зажим на игле. Удалите защитный колпачок и немедленно приступайте к пунктированию.
5. Осторожно пунктируйте фистулу под углом 25°. Когда в иглу поступит кровь (возможно, придется снять зажим, чтобы увидеть обратный ток крови), опустите иглу до уровня параллельно с кожей и продвиньте ее в просвет фистулы.
6. Когда игла окажется в сосуде, снимите жгут и аккуратно зафиксируйте иглу пластырем по протоколу. Если поступление крови будет видно, аспирируйте 1-5 мл раствора в 10-мл шприц.
7. Промойте иглу физраствором и закройте зажим. Шприц должен легко забирать и возвращать раствор. Проверяйте признаки и симптомы поступления раствора под кожу. Пациенты в этом случае обычно испытывают острую боль.
8. Повторите шаги 1-7 для второй иглы, если не предполагается возвращать кровь в венозный катетер (см. ниже).
F. Техника одной иглы с возвратом в венозный катетер. При наличии венозного катетера нет необходимости начинать диализ на новой фистуле с использованием двух игл. Риск гематомы выше для иглы, используемой для возврата. В ходе первых двух-трех сеансов кровь можно возвращать через венозный катетер. Следующие сеансы можно выполнять с двумя иглами, и только после нескольких успешных сессий венозный катетер можно удалить.
X. АРТЕРИОВЕНОЗНЫЙ ПРОТЕЗ. Как описано во введении в настоящую главу, AV-протез менее желателен, чем AV-фистула. В первую очередь, из-за меньшей длительности сохранения проходимости и большей потребности в эндоваскулярных вмешательствах для поддержания проходимости. AV-протез имеет некоторые преимущества, включая большую протяженность участка для пунктирования, простоту пунк-тирования, короткое время созревания и более простую технику установки.
Большая часть AV-протезов, используемых в США, выполнена из PTFE. Выбор синтетического или биологического материала основывается на предпочтениях хирурга и его опыте. Использование криоконсервированных венозных протезов, особенно при установке на бедро, связывают с большими рисками инфекции. Короткие протезы не имеют преимущества над длинными протезами в отношении проходимости и выживаемости. Конусовидные протезы или эластичные протезы не продемонстрировали лучших исходов, чем стандартные PTFE-протезы. Модификация дистального анастомоза протеза венозной муфты снижает частоту венозных стенозов и улучшает выживаемость протеза. Новые, покрытые гепарином материалы протеза не продемонстрировали долгосрочных преимуществ.
А. Возможные места расположения AV-протезов.
1. Обычная локация. Протезы могут быть установлены в прямой, петлевой или изогнутой конфигурации (рис. 6.4). Типичными начальными вариантами установки протеза являются прямой протез от лучевой артерии на запястье к базилярной вене, петлевой протез на предплечье от плечевой артерии к базилярной вене (рис. 6.5) или протез на плече от плечевой артерии к акси-лярной вене (рис. 6.6). Особенности пациента и предполагаемое время лечения диализом помогают определиться с выбором места для протеза. Предпочтительным первоначальным вариантом является дистальный протез на недоминантной руке. Хотя этот подход сохраняет проксимальные места для будущих сосудистых доступов, использование дистального протеза связано с большей частотой эпизодов тромбоза. Дистальный протез (например, прямой протез на предплечье от лучевой артерии к вене в локтевом сгибе) иногда может использоваться для созревания проксимальной вены для будущего создания AV-фистулы.
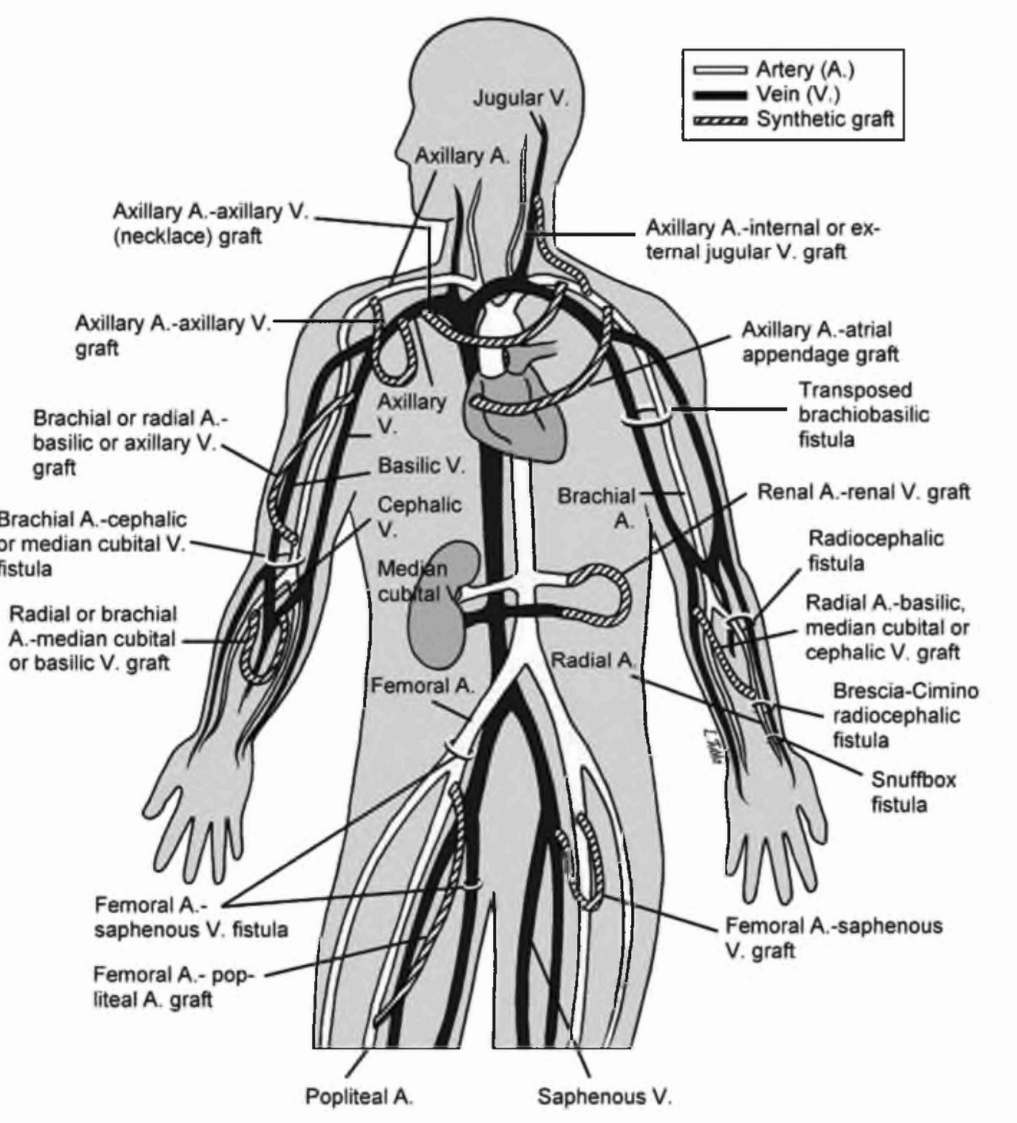
РИСУНОК 6.4. Различные конфигурации и участки для формирования AV-протезов. Воспроизведено с разрешения Paulson WD, Ram SJ, Zibari GB. Vascular access: anatomy, examination, management. Semin Nephrol. 2002; 22:183-194
2. Необычная локация. Аксилярную артерию можно использовать для создания петлевого протеза на верхних конечностях. Протез может проходить от плеча к внутренней яремной вене, чтобы обойти стеноз подключичной вены на той же стороне. AV-протез можно расположить также на бедре, но это связано с большей частотой осложнений. Аксилярный протез на грудной клетке («ожерелье») является еще одной возможностью, когда остальные варианты исчерпаны. Может быть использовано множество других мест расположения, включая протез от аксилярной артерии к бедренной вене, в зависимости от индивидуальных особенностей пациента и опыта хирурга.
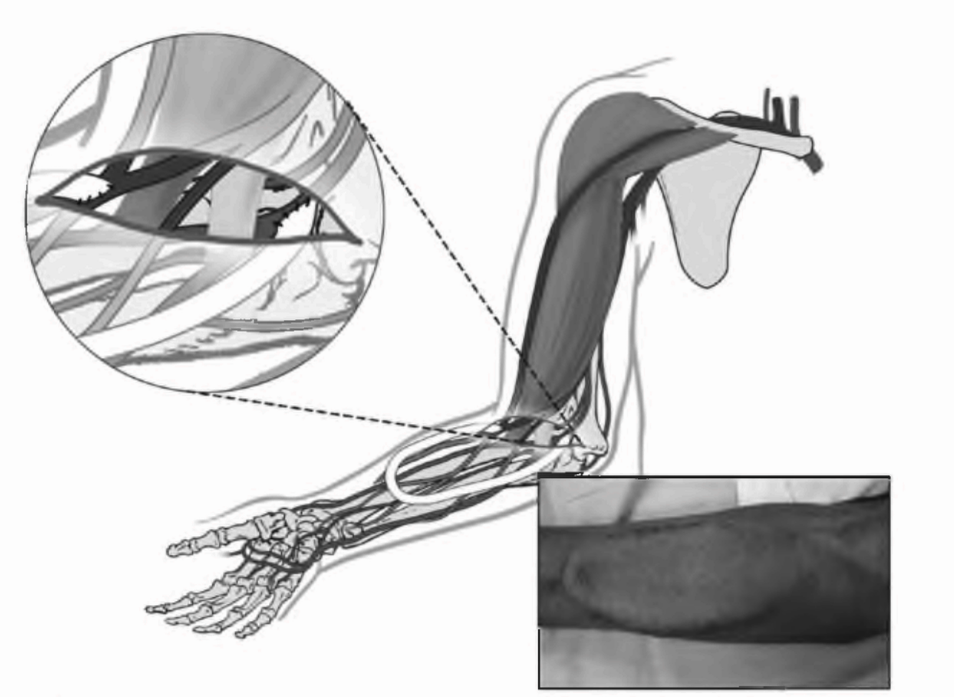
РИСУНОК 6.S. Петлеобразный AV-протез на предплечье. Воспроизведено с разрешения Atlas of Dialysis Vascular Access - http://www.fistulafirst.org
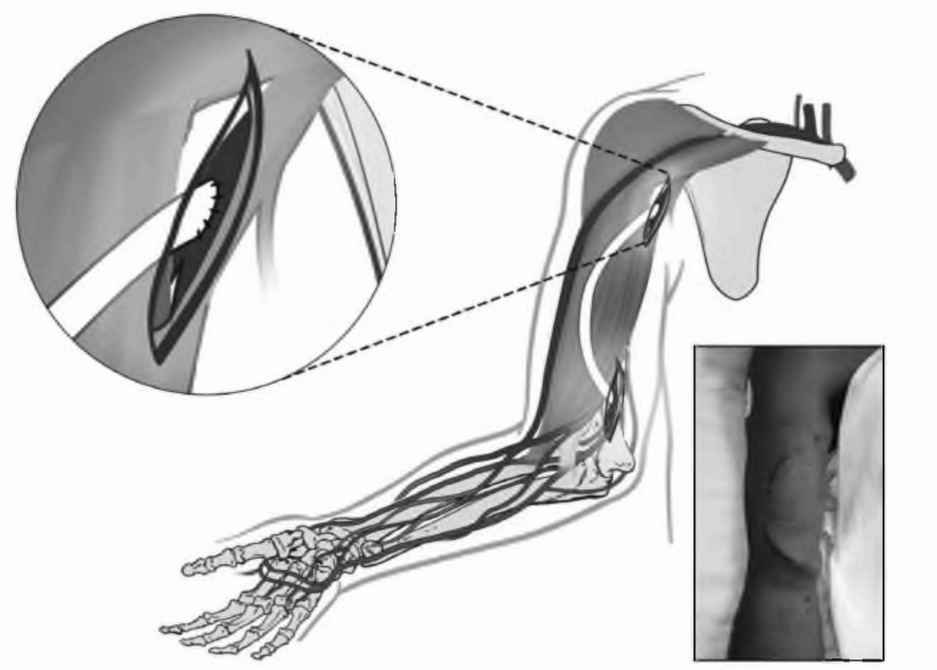
РИСУНОК 6.6. Высокий AV-протез на плече. Воспроизведено с разрешения Atlas of Dialysis Vascular Access - www. fistulafirst.org
B. Хирургическая процедура установки. Непосредственно перед операцией профилактически применяются антибиотики. Анастомоз следует выполнять по типу «конец протеза в бок вены или артерии», для того чтобы минимизировать взаимодействие с кровотоком по естественным сосудам. В некоторых исследованиях показано, что непенетрирующие клипсы могут иметь преимущества перед обычными швами за счет предупреждения повреждения эндотелия. На артериальном и венозном анастомозе необходимо установить клипсы для последующей идентификации в ходе ангиографии.
C. Послеоперационный уход. Послеоперационный уход аналогичен таковому при создании AV-фистулы. Конечность держат в возвышенном положении в течение нескольких дней. Функционирование протеза регулярно проверяется по наличию пульсации и шума при пальпации. Нет логики в использовании физических упражнений для ускорения созревания.
D. Созревание. Протез из PTFE не следует пунктировать по крайней мере 2 недели после установки; он считается созревшим, когда отек и покраснение вокруг разрешаются и протез становится легко доступен для пальпации. Для предотвращения гематом требуется формирование адгезии между протезом и подкожным тоннелем, что занимает 2-3 недели. Пунктирование протеза, который нельзя легко пропальпировать, или протеза в отечных тканях приводит к неточному введению иглы, образованию гематом и повреждению протеза. Пациентам с персистирующим отеком руки, который не отвечает на ее возвышенное положение, требуется произвести визуализирующее исследование для оценки состояния центральных вен.
1. Рано используемые протезы. Было разработано несколько протезов для немедленного использования после операции с целью предотвратить осложнения, связанные с центральным венозным катетером. Производительность многослойного самозаживляемого полиуретанового протеза сравнима с таковой для обычного PTFE-протеза; его можно использовать вскоре после установки. Установка требует большего опыта, чем для PTFE-протеза, из-за риска сгибания и перекручивания в тоннеле. Композитный протез не следует пунктировать как минимум 24 часа после установки и до уменьшения отека вокруг раны; протез должен легко пальпироваться. Само заживляемый протез из поликарбоната со связанным гепарином доступен для пункции немедленно после установки.
2. Протез изаутотканей. Представлен предварительный опыт использования аутологичных сосудистых протезов на основе тканевой инженерии (Wystrychow-ski, 2013). Неизвестно, однако, в какой мере эти протезы предотвратят долгосрочные осложнения и насколько устойчивы они окажутся к повторным пункциям при регулярном диализе.
XI. ФИЗИКАЛЬНОЕ ОБСЛЕДОВАНИЕ AV-фИСТУЛЫ И ПРОТЕЗА. Физикальное обследование является неинвазивным и дешевым тестом в оценке AV-доступа. Множество исследований продемонстрировали, что физикальное обследование может точно выявить и локализовать стеноз у абсолютного большинства пациентов. Физикальное обследование полезно не только в послеоперационном мониторинге новых фистул и протезов, но и в оценке дисфункции доступа. Последняя тема детально обсуждена в главе 8.
A. Осмотр. Осмотр не должен ограничиваться местом расположения AV-доступа, но включать в себя остальную часть руки, плечо, грудную клетку, шею и лицо. Наличие отека на любой из этих областей следует зафиксировать; это должно вызвать подозрение в наличии стеноза далее по ходу кровотока, равно как и наличие коллатеральных вен. Любые шрамы на грудной клетке следует тщательно осмотреть как возможные признаки предшествующих установок катетеров. Наличие отека на лице, шее или грудной клетке обычно указывает на центральный венозный стеноз.
B. Пальпация и аускультация
1. Пульс. Обычно на AV-доступе обнаруживаются мягкие пульсовые волны, которые можно легко пережать несильным сдавлением. При наличии стеноза ниже по кровотоку пульс становится увеличенным (гиперпульсация). В анамнезе при такой ситуации часто присутствуют длительные кровотечения после удаления игл. Напротив, слабый пульс (гипопульсация) указывает на стеноз выше по кровотоку. В анамнезе имеются указания на частые проблемы с функционированием артериальной иглы (высокое отрицательное давление).
2. Дрожание. Дрожание в области AV-доступа можно почувствовать, приложив пальцы. Дрожание может быть непрерывным или прерывистым. В норме дрожание бывает непрерывным во всех случаях, кроме артериального анастомоза, где дрожание в норме прерывистое. Дрожание следует проследить от анастомоза до стенки грудной клетки. Часто стеноз головной арки дает прерывистое дрожание в зоне арки на передней поверхности плеча. При наличии стеноза дрожание становится прерывистым; часто систолическое дрожание наблюдают сразу за стенозом.
3. Аускультация. Аускультация проводится для оценки шума над AV-доступом. Как и дрожание при пальпации, аускультация позволяет выявлять наличие и локализацию стенозов.
C. Усиление пульса. Существуют два дополнительных теста, которые можно использовать для быстрой оценки доступа. Тест усиления пульса оценивает входящий сегмент, тогда как тест поднятия руки - выходящий тракт.
1. Тест усиления пульса. Тест проводится полным пережатием доступа на несколько сантиметров выше артериального анастомоза, оценивается сила пульса. Результат рассматривается как нормальный, если на участке фистулы ниже пережатия отмечается усиление пульса. Для AV-фистулы в ходе теста можно выявить боковые ветви. При пережатии оттока AV-доступа пальцем обычно наблюдаются два явления: 1) исчезает дрожание, 2) участок доступа ниже пережатия становится гиперпульсирующим. Если дрожание под пальцами сохраняется при пережатии, следует заподозрить наличие дополнительного оттока. В этом случае усиления пульса не происходит в ожидаемой мере, поскольку давление распределяется по дополнительным путям оттока. Можно найти точку отхода боковых ветвей, перемещая сдавливающий палец к анастомозу фистулы. Когда дрожание исчезнет и усиление пульса восстановится, можно сделать вывод, что палец только что прошел точку отхода боковой ветви. Движение пальца в обратном направлении от анастомоза вновь восстановит дрожание. Этот прием подтверждает место отхода боковой ветви.
2. Тест поднятия руки. Тест проводится поднятием руки, оценивается спадение фистулы. Тест рассматривается как отклоняющийся от нормы, когда фистула остается наполненной после подъема руки и не спадается. Это указывает на наличие стеноза ниже по кровотоку.
XII. ОБЩИЕ ВОПРОСЫ ПУНКТИРОВАНИЯ ФИСТУЛЫ И ПРОТЕЗА
A. Подготовка кожи. Следует использовать асептическую технику для любой пункции.
B. Анестезия. У чувствительных к боли пациентов аналгезирующий крем можно наложить на кожу за 30 минут до пункции, хотя это требуется редко. Большинство пациентов, особенно с новым доступом, требуют подкожной инъекции лидокаина перед введением иглы. Введение анестетика особенно полезно, если предполагаются манипуляции с иглой. Пациенты с установившейся фистулой часто хорошо переносят пункцию без анестезии, и некоторые считают, что инъекция с анестетиком более болезненна, чем прямая пункция.
C. Использование жгута для AV-фистулы. Для увеличения и стабилизации вены с облегчением пунктирования используют жгут или манжету для измерения АД. Жгут должен быть снят до начала проведения лечения; фистула, которая работает только под наложенным жгутом, является неразработанной, обычно из-за стеноза притока. Такая фистула требует больше времени для созревания или повторной оценки перед продолжением ее использования.
Если жгут не требуется для проведения пункции, а фистула не смягчается при подъеме руки, возможно, имеется стеноз ниже по кровотоку, что требует проведения визуализирующих исследований.
D. Размер иглы. Как отмечалось выше, в начальный период использования постоянного доступа, особенно фистулы, некоторые нефрологи рекомендуют применять иглы малого диаметра (16G или 17G) и низкую скорость кровотока. При созревшей фистуле требуются иглы большего диаметра (15G) для обеспечения кровотока более 350 мл/мин при высокоэффективном диализе.
E. Положение и ориентация игл. Две иглы располагаются в фистульной вене или в протезе. Артериальная игла всегда располагается выше по кровотоку, но как минимум на 3 см выше артериального анастомоза. Эта игла может быть направлена как вверх, так и вниз по кровотоку. В некоторых странах популярно направлять иглу вниз по кровотоку. Обоснованием служит суждение, что «клапан» на стенке сосуда после удаления иглы закрывается более естественно по кровотоку. Однако подтверждение этому суждению отсутствует. Венозную иглу следует вводить по направлению кровотока примерно на 5 см ниже от артериальной иглы для минимизации рециркуляции. В одном из исследований показано, что рециркуляции не происходит, даже если иглы разнесены на 2,5 см (Rothera, 2011). В некоторых центрах иглы поворачивают на 180 градусов вдоль оси для предотвращения повреждения глубокой стенки сосуда кончиком иглы. Этот вопрос не был систематически исследован, и оснований для такой рекомендации нет.
1. Риск смены игл забора и возврата. Особое внимание следует уделить пункции петлевых протезов на плече. В более чем 80% таких протезов артериальная ветвь будет располагаться медиально (с локтевой стороны), но в остальных случаях артериальная ветвь может лежать с лучевой стороны предплечья. Можно допустить обратное расположение игл, если не знать направления тока по протезу. Обратное расположение игл увеличивает рециркуляцию (более 20%) и может привести к неадекватной дозе диализа. Это случается чаще, чем можно было бы ожидать, поскольку доступ может быть создан в другом центре, а карта доступа отсутствует. В случае сомнений внимательное физикальное обследование с временным пережатием доступа пальцем и оценкой пульсации поможет выявить направление кровотока. Для контроля очень полезна карта доступа, предоставляемая хирургом, выполнявшим операцию.
F. Повторные пункции: поворот иглы. Способ, которым вводятся иглы, влияет на долгосрочную проходимость и выживаемость доступа, особенно AV-фистулы. Целесообразна перемена места введения иглы по всей длине доступа без формирования типичных двух точек. Использование двух типичных мест введения иглы ослабляет стенку фистулы, провоцируя аневризму.
G. Пунктирование по методу пуговицы. Одну из техник пунктирования AV-фистулы называют пуговичным методом. AV-фистула всегда пунктируется через ограниченное число мест, которые могут ротироваться. Иглу следует вводить точно по месту предыдущего введения. После зон введения, созданных острой иглой, используются специальные тупые иглы для минимизации повреждения тракта. Первоначальный энтузиазм, связанный с этим подходом, в последующем отступил из-за предположений об увеличении частоты инфекционных осложнений при отсутствии свидетельств увеличения продолжительности работы фистулы (MacRae, 2014; Muir, 2014). Степень успеха при таком подходе может существенно зависеть от техники исполнения. Отсутствует опубликованный опыт использования метода на AV-протезах, и не следует его применять до проведения дальнейших исследований.
Метод требует строго придерживаться мер инфекционного контроля и предотвращения связанных с методикой осложнений (Dinwiddie, 2013).
1. Соблюдайте четкую последовательность шагов выбранной методики (подготовка кожи, удаление корочек, повторная обработка кожи, корректное введение тупых игл).
2. Пользуйтесь крылышками иглы, чтобы мягко пройти иглой кожу и стенку сосуда - избыточное давление не позволяет ощутить пальцами сопротивление продвижению.
3. Всегда пунктируйте тракт, созданный по пуговичному методу, в одинаковых условиях. Если жгут использовался для создания тракта, его следует использовать постоянно. В противном случае ткани вокруг тракта не будут находиться в прежних пространственных соотношениях. Рассматривайте пациента как кандидата на самостоятельные пункции. Выигрыш может состоять в меньшей болезненности, простоте пунктирования, поскольку пациент приобретет квалификацию в пункции собственной фистулы.
H. Предотвращение и лечение гематом. Образование гематомы может произойти во время пунктирования, в ходе диализа, когда насос продолжает вращаться, или после диализа в процессе удаления илы. Следует всегда следить за симптомами и признаками гематом. Быстрый ответ на возникновение гематомы поможет минимизировать ее размер.
1. Если гематома возникает на фоне применения гепарина, важно уделить внимание тому, чтобы затромбировался тракт иглы, а не фистула. В некоторых случаях адекватным будет решение оставить иглу на месте и пунктировать доступ в другом месте. Немедленное использование льда уменьшает боль, размер гематомы и может сократить время кровотечения.
2. Будьте осторожны при фиксации иглы пластырем. Избегайте поднимать иглу, если она уже в вене. Некорректное движение иглы может привести к гематоме.
3. Если вокруг фистулы возникла гематома, лучше сделать перерыв в использовании фистулы как минимум на один сеанс. Если это невозможно, следующую пункцию следует произвести ниже по кровотоку. Если у пациента еще остался центральный венозный катетер, можно восстановить режим пункции одной иглой, возвращая кровь через венозный катетер. В последующем можно вернуться на режим двух игл большего размера и с большими кровотоками, когда позволит состояние доступа.
4. Корректное удаление иглы предотвращает гематомы после диализа. Перед удалением иглы приложите салфетку к точке вкола, но не применяйте пока давление. Затем осторожно удалите иглу примерно под тем же углом, под которым она была введена. Это предотвратит протягивание иглы через кожу. Удаление иглы под слишком большим углом может вызвать повреждение стенки вены острым окончанием иглы.
5. Е1е применяйте давление к месту пункции, пока игла полностью не удалена.
6. Сообщайте остальному персоналу о возникновении гематомы. В некоторых случаях правильным будет сделать перерыв в использовании иглы. В других случаях могут потребоваться иные вмешательства.
I. Гемостаз после сеанса. Лучшим методом гемостаза после удаления иглы является прямое давление кончиками одного-двух пальцев, не настолько сильное, чтобы пережать фистулу. Для предотвращения возникновения гематомы следует контролировать кровотечение в месте выхода. Давление следует сохранять как минимум десять минут перед тем, как проверить место выхода на продолжающееся кровотечение. Адгезивную повязку не следует накладывать, пока не достигнут полный гемостаз.
Продолжительное кровотечение (больше 20 минут) может указывать на повышенное давление внутри сосудистого доступа вследствие незамеченного стеноза. Кровотечение также удлиняется у пациентов, получающих терапевтические дозы антикоагулянтов, таких как варфарин. Другой причиной кровотечения может стать поступление гепарина из замка венозного катетера у пациентов, которые переводятся с венозных катетеров на AV-фистулу в том случае, когда венозный катетер применяется для возврата крови в ходе начального использования фистулы.
Ссылки и рекомендуемая литература
Agarwal АК. Central vein stenosis: current concepts. Adv Chronic Kidney Dis. 2009; 16: 360-370.
Agarwal R, McDougal G. Buzz in the axilla: a new physical sign in hemodialysis forearm graft evaluation. Am J Kidney Dis. 2001; 38: 853-857.
Asif A, et al. Early arteriovenous fistula failure: a logical proposal for when and how to intervene. Clin J Am Soc Nephrol. 2006; 1: 332-339.
Asif A, et al. Vascular mapping techniques: advantages and disadvantages. J Nephrol. 2007; 20: 299-303.
Asif A, et al. Accuracy of physical examination in the detection of arteriovenous graft stenosis. Semin Dial. 2008;21:85-88.
Beathard GA. An algorithm for the physical examination of early fistula failure. Semin Dial. 2005; 18: 331-335. Bharat A, Jaenicke M, and Shenoy S. A novel technique of vascular anastomosis to prevent juxta-anastomotic stenosis following arteriovenous fistula creation. J Vase Surg. 2012; 55: 274-80.
Campos PR, et al. Stenosis in hemodialysis arteriovenous fistula: evaluation and treatment. Hemodial Int. 2006; 10: 152-161.
Campos PR, et al. Accuracy of physical examination and intra-access pressure in the detection of stenosis in hemodialysis arteriovenous fistula. Semin Dial. 2008; 21: 269-273.
Caroli A, et al; for the ARCH project Consortium. Validation of a patient-specific hemodynamic computational model for surgical planning of vascular access in hemodialysis patients. Kidney Int. 2013; 84: 1237-1245.
Chemla ES, et al. Complex bypasses and fistulas for difficult hemodialysis access: a prospective, single-center experience. Semin Dial. 2006; 19: 246-250.
Coskun I, et al. Hemodynamic effects of left upper extremity arteriovenous fistula on ipsilateral internal mammary coronary artery bypass graft. Thorac Cardiovasc Surg. 2013; 61: 663-667.
Crowther MA, et al. Low-intensity warfarin is ineffective for prevention of PTFE graft failure in patients on hemodialysis: a randomized controlled trial. Clin J Am Soc Nephrol. 2002; 13: 2331-2337.
Dember LM, et al; Dialysis Access Consortium (DAC) Study Group. Effect of clopidrogrel on early failure of arteriovenous fistulas for hemodialysis: a randomized controlled trial. JAMA. 2008; 299: 2164-2171.
Dinwiddie LC, et al. What nephrologists need to know about vascular access cannulation. Semin Dial. 2013; 26: 315-322.
Drawz PE, et al. A simple tool to predict end-stage renal disease within 1 year in elderly adults with advanced chronic kidney disease. J Am Geriatr Soc. 2013; 61: 762-768.
Feldman L, et al. Effect of arteriovenous hemodialysis shunt location on cardiac events in patients having coronary artery bypass graft using an internal thoracic artery. J Am Soc Nephrol. 2013; 24: 214A (abstract).
Gradzki R, et al. Use of ACE inhibitors is associated with prolonged survival of arteriovenous grafts. Am J Kidney Dis. 2001; 38: 1240-1244.
Hoggard J, et al. ASDIN guidelines for venous access in patients with chronic kidney disease: a position statement from the American Society of Diagnostic and Interventional Nephrology Clinical Practice Committee and the Association for Vascular Access. Semin Dial. 2008; 21: 186-191.
Huijbregts HJ, Blankestijn PJ. Dialysis access - guidelines for current practice. Eur J Vase Endovasc Surg. 2006; 31:284-287.
Jaberi A, et al. Arteriovenous fistulas for hemodialysis: application of high-frequency US to assess vein wall morphology for cannulation readiness. Radiology. 2011; 216: 616-624.
Kaufman JS, et al. Randomized controlled trial of clopidogrel plus aspirin to prevent hemodialysis access graft thrombosis. J Aw Soc Nephrol. 2003; 14: 2313-2321.
Konner K. A primer on the AV fistula - Achilles’ heel, but also Cinderella of haemodialysis. Nephrol Dial Transplant. 1999; 14:2094-2098.
Lin CC, et al. Effect of far infrared therapy on arteriovenous fistula maturation: an open-label randomized controlled trial. Am J Kidney Dis. 2013; 62: 304-311.
Lok CE, Davidson I. Optimal choice for dialysis access for chronic kidney disease patients: developing a life plan for dialysis access. Semin Nephrol. 2012; 32: 530-537.
Lok CE, et al. Cumulative patency of cotemporary fistulas versus grafts (2000-2010). Clin J Am Soc Nephrol. 2013;8:810-818.
MacRae JM, et al. Arteriovenous fistula survival and needling technique: long-term results from a randomized buttonhole trial. Aw J Kidney Dis. 2014; 63: 636-642.
Malovrh M. Native arteriovenous fistula: preoperative evaluation. Aw J Kidney Dis. 2002; 39: 1218-1225.
Maya ID, et al. Vascular access stenosis: comparison of arteriovenous grafts and fistulas. Aw J Kidney Dis. 2004; 44:859-865.
Moist LM, et al. Optimal hemodialysis vascular access in the elderly patient. Semin Dial. 2012; 25: 640-648.
Moist LM, et al. Education in vascular access. Semin Dial. 2013; 26: 148-153.
Muir CA, et al. Buttonhole cannulation and clinical outcomes in a home hemodialysis cohort and systematic review. Clin J Am Soc Nephrol. 2014; 9: 110-119.
Murea M, et al. Risk of catheter-related bloodstream infection in elderly patients on hemodialysis. Clin J Am Soc Nephrol. 2014; 9: 764-770.
National Kidney Foundation. 2006 NKF-K/DOQI clinical practice guidelines for vascular access: update 2006. Aw J Kidney Dis. 2006; 48 (suppl 1): S177-S277.
Ohira S, Коп T, Imura T. Evaluation of primary failure in native AV-fistulae (early fistula failure). Hemodial Int. 2006; 10: 173-179.
Okada S, Shenoy S. Arteriovenous access for hemodialysis: preoperative assessment and planning. J Vase Access. 2014; 15 (suppl 7): 1-5.
Ortega T, et al. The timely construction of arteriovenous fistulas: a key to reducing morbidity and mortality and to improving cost management. Nephrol Dial Transplant. 2005; 20: 598-603.
Palmes D, et al. Perforating vein fistula is superior to forearm fistula in elderly haemodialysis patients with diabetes and arterial hypertension. Nephrol Dial Transplant. 2011; 26: 3309-3314.
Paul BZS, Feeny CM. Combining the modified Allens test and pulse oximetry for evaluating ulnar collateral circulation to the hand for radial artery catheterization of the ED patient. CalifJEmergMed. 2003; 4:89-91.
Pirozzi N, et al. Microsurgery and preventive haemostasis for autogenous radial-cephalic direct wrist access in adult patients with radial artery internal diameter below 1.6 mm. Nephrol Dial Transplant. 2010; 25: 520-525.
Rothera С, et al. The influence of between-needle cannulation distance on the efficacy of hemodialysis treatments. Hemodial Int. 2011; 15: 546-552.
Saad TF, et al. Cardiovascular implantable device leads in CKD and ESRD patients: review and recommendations for practice. Semin Dial. 2013; 26: 114-123.
Saucy F, et al. Is intra-operative blood flow predictive for early failure of radiocephalic arteriovenous fistula? Nephrol Dial Transplant. 2010; 25: 862-867.
Shenoy S. Surgical anatomy of upper arm: what is needed for AVF planning. J Vase Access. 2009; 10: 223-232.
Tangri N, et al. A predictive model for progression of chronic kidney disease to kidney failure. JAMA. 2011; 305: 1553-1559.
Tangri N, et al. Validation of the kidney failure risk equation in an International Consortium [abstract SA-OR055]. J Am Soc Nephrol. 2013; 24: 84A.
Vachharajani TJ. Diagnosis of arteriovenous fistula dysfunction. Semin Dial. 2012; 25: 445-450.
Vachharajani TJ, et al. Re-evaluating the fistula first initiative in octogenarians on hemodialysis. Clin J Am Soc Nephrol. 2011; 6: 1663-1667.
Vaux E. Effect of buttonhole cannulation with a polycarbonate peg on in-center hemodialysis fistula outcomes: a randomized controlled trial. Am J Kidney Dis. 2013; 62: 81-88.
Wystrychowski W, et al. First human use of an allogeneic tissue-engineered vascular graft for hemodialysis access. J Vase Surg. 2014, in press.
Xue JL, et al. The association of initial hemodialysis access type with mortality outcomes in elderly Medicare ESRD patients. Am J Kidney Dis. 2003; 42: 1013-1019.
Интернет-ссылки
American Nephrology Nurses’ Association «Save the Vein» project, http://www.annanurse.org/resources/save-the-vein-campaign.
American Society of Diagnostic and Interventional Radiology, http://www.asdin.org/.
Atlas of Dialysis Vascular Access, http://www.theisn.org/hemodialysis/education-bytopic.
Fistula First initiative: http://www.fistulafirst.org.
Physical examination of arteriovenous fistula. http://www.youtube.com/watch?v=ml-C61AOY3Q.
