- Диализному врачу
- 1. Ведение пациентов с ХБП 4-5-й стадии.
- 2. Подготовка к трансплантации, диализу или к консервативной терапии
- 3. Физиологические принципы и моделирование кинетики мочевины
- 4. Оборудование для гемодиализа и расходные материалы
- 5. Вода для диализа и диализирующий раствор
- 6. Артериовенозные фистулы и протезы. Основные положения
- 7. Центральный венозный катетер в качестве доступа: основы
- 8. Мониторинг артериовенозного доступа и осложнений
- 9. Инфекции и другие осложнения центральных венозных катетеров
- 10. Назначение острого гемодиализа
- 11. Назначение хронического гемодиализа
- 12. Осложнения в ходе процедуры гемодиализа
- 13. Повторное использование диализаторов
- 14. Антикоагуляция
- 15. Продленная заместительная почечная терапия
- 16. Гемодиафильтрация
- 17. Терапевтический аферез
- 18. Актуальность сорбционных технологий сегодня
- 19. Руководство по диализу
Назначение хронического гемодиализа
Предлагаем заново обратиться к главе 3, так как далее используются концепции, подробно описанные в ней.
I. МОЧЕВИНА КАК МОЛЕКУЛА-МАРКЕР. Уремия обусловлена присутствием в крови токсичных веществ как с малой, так и с большой молекулярной массой. Мочевина - самый низкомолекулярный токсин, размером 60 Да, быстрее и легче всего проходит через поры диализной мембраны. По этой причине (и на основании практических лабораторных данных) назначаемая доза диализа рассчитывается исходя из количества удаленной мочевины. Мочевина обладает незначительной токсичностью, но ее концентрация в плазме позволяет получить примерное представление о содержании уремических токсинов с большей молекулярной массой, предположительно более вредных для организма.
A. Удаление мочевины и ее уровень в плазме. Как удаление мочевины, так и ее уровень в плазме должны контролироваться с целью оценки адекватности диализа, причем мониторинг выведения мочевины в данном случае более важен. Если ее выведение неадекватно, тогда и адекватность всего диализа будет недостаточной, несмотря на то, каким в итоге стал уровень мочевины в крови. С другой стороны, низкий уровень мочевины в плазме не обязательно означает, что проведенный диализ адекватен, так как он зависит не только от объема выведения мочевины, но и от объема ее образования в организме. Уровень образования мочевины отражается величиной продукции белкового азота (PNA), поскольку большая часть этого азота выводится именно с мочевиной. Невысокий уровень мочевины плазмы может наблюдаться и у пациентов с недостаточным ее выведением из организма, за счет ее низкого образования (например, из-за малобелкового рациона питания).
B. Измерения удаления мочевины. К ним относятся: процент снижения мочевины (URR), а также индексы дозы диализа - однопуловый Kt/V (spKt/V), выравненный Kt/V (eKt/V) и стандартный недельный Kt/V (stdKt/V) (см. главу 3).
C. Выбор дозы по удаленной мочевине при диализе 3 раза в неделю. По итогам вторичного анализа первого рандомизированного объединенного национального исследования диализа (NCDS1, США) у пациентов, получавших диализ 3 раза в неделю, процент неблагоприятного прогноза лечения был значительно выше при spKt/V <0,8 по сравнению с теми, у кого этот индекс был >1,0. В других больших наблюдательных исследованиях были получены похожие результаты. По этой причине рабочие группы KDOQI2 по оценке адекватности диализа рекомендуют минимальное значение индекса spKt/V - 1,2, а целевое - как минимум 1,4. Это соответствует stdKt/V по мочевине - 2,1, при условии что stdKt/V рассчитан методом, учитывающим снижение объема распределения мочевины. В Европейских рекомендациях по наилучшей практике минимальная доза диализа несколько выше - eKt/V = 1,2. Значения индекса eKt/V, как правило, ниже значения spKt/V на 0,15 единицы. Серьезный уровень доказательности должен основываться на результатах крупных рандомизированных исследований, а по адекватности диализа, помимо NCDS, проводилось лишь еще одно такое исследование - НЕМО3 (США), в котором результаты диализа при уровне spKt/V в 1,7 сравнивались с spKt/V = 1,3 (доза диализа в данном исследовании определялась индексом eKt/V). В результате у пациентов, дозы диализа которых были более высокими, не наблюдалось увеличения продолжительности жизни, не уменьшалась частота их госпитализаций, не появлялось улучшений в состоянии питания или каких-либо других благоприятных изменений. Помимо двух вышеперечисленных исследований имеется мало достоверных данных, касающихся результатов лечения диализом в зависимости от дозы, и практически все рекомендации в данном вопросе основаны, в первую очередь, на субъективных мнениях.
1. Выбор дозы диализа в зависимости от пола пациента. В результате анализа рандомизированного исследования НЕМО оказалось, что у женщин в группе с более высокой дозой диализа продолжительность жизни была выше, а у мужчин с большей дозой выживаемость была немного хуже. Поэтому общий эффект повышенной дозы диализа в рамках данного исследования оказался нейтральным. Пока не ясно, по какой причине женщинам требуется большая доза диализа и действительно ли существует какая-то взаимосвязь между полом пациента и необходимойему диализной дозой. Как подробно описано в главе 3, альтернативным методом подбора индивидуальной дозы диализа для пациента является расчет, скорректированный на площадь поверхности тела (BSA) вместо объема распределения мочевины (V). У здоровых пациентов и у детей скорость клубочковой фильтрации (СКФ) стандартизируется по площади поверхности тела. Взрослые мужчины и женщины со схожими значениями BSA будут иметь примерно одинаковую СКФ (Daugirdas, 2009). При существующих рекомендациях по выбору дозы диализа, если мужчина и женщина имеют одинаковые уровни V, то они получат одну и ту же дозу диализа. Однако соотношения V к BSA у женщин и мужчин отличаются на 12-15%, поэтому можно предположить, что доза диализа для женщин должна быть примерно на 15% выше. Если говорить об индексе stdKt/V, то в этом случае его увеличение для женщин должно составлять 15% по сравнению с мужчинами. Однако помимо результатов, полученных в исследовании НЕМО и в некоторых обзорных исследованиях, не существует других достоверных данных, позволяющих заменить параметр V на BSA при подборе индивидуальной дозы диализа.
KDOQI - Kidney Disease Outcome Quality Initiative - инициатива качества лечения и исходов заболеваний почек - группы экспертов, привлеченных Национальным почечным фондом США (NKF)
2. Небольшие пациенты. Есть четыре причины, по которым небольшие пациенты должны получать большую дозу диализа.
a. Небольшие пациенты (величины V которых малы) получили бы большую дозу диализа, если бы она рассчитывалась исходя из BSA.
b. KDOQI рекомендуют использовать индекс spKt/V, а не eKt/V, а постдиализный «рикошет» мочевины у небольших пациентов более выражен.
c. Имеется кажущаяся простота в обеспечении высоких значений Kt/V у небольших пациентов (а также женщин) при короткой процедуре (например, 2,5 часа). Однако такого непродолжительного диализа может оказаться недостаточно ни для выведения веществ со средней молекулярной массой, ни для адекватного удаления жидкости, что приведет к ее хронической задержке в организме.
d. Короткие процедуры диализа могут обеспечить кажущийся адекватным уровень Kt/V, но у пациентов с большим накоплением жидкости в междиализный период при более коротких процедурах потребуется увеличение скорости ультрафильтрации, что может привести к неблагоприятным отдаленным исходам.
3. Выбор дозы диализа для пациентов с недостаточностью питания. Существует мнение, что, если масса тела пациента значительно ниже нормального уровня или пациент сильно потерял в весе, следует подстраивать дозу диализа под его оптимальный «сухой» вес до снижения, а не под текущий. Имеется в виду, что увеличенная доза позволит вернуть пациента в прежнее состояние - до болезненного ухудшения.
4. Остаточная функция почек. Вопрос о назначении пациентам с остаточной функцией почек пониженной дозы диализа остается открытым. По данным крупного исследования, доза диализа мало влияла на выживаемость пациентов с суточным объемом мочи более 100 мл (Temorshuizen, 2004). Методы коррекции дозы диализа при сохраненной остаточной функции почек основываются исключительно на субъективном мнении. В Европейских рекомендациях по наилучшей клинической практике (2002) и рекомендациях NKF-KDOQI 2006 г. разработан ряд моделей для выбора дозы диализа для таких случаев.
D. Показатели адекватности диализа при его частоте, отличной от 3 раз в неделю. Нет убедительных свидетельств, чтобы рекомендовать какую-либо дозу диализа при частоте выше 3 раз в неделю. Одним из подходов является поддержание stdKt/V (рассчитанного с применением моделирования мочевины или по формуле из исследования FEIN4) не менее 2,1 при всех графиках проведения диализа (табл. 11.1). Это значение было выбрано из-за того, что оно соответствует spKt/V = 1,2 при трехразовом диализе в неделю (NKF-KDOQI, 2006).
1. Четыре или шесть сеансов в неделю. В одном из рандомизированных исследований, выявившем преимущества более частых сеансов (FHN Daily Trial), среднее значение stdKt/V было 3,7 - это значительно выше, чем минимум данного показателя, предложенный NKF-KDOQI. В среднем сеансы проводились 5 раз в неделю по 154 минуты (FHN Trial Group, 2010).
2. Диализ 2 раза в неделю. В развивающихся странах и США многим пациентам диализ проводится только два раза в неделю. Анализ stdKt/V показывает, что подобный режим диализа не может быть адекватным для всех, особенно для тех пациентов, у которых нет значительной остаточной функции почек.
Таблица 11.11 Минимальные3 значения spKt/V для разных графиков диализа

Одно из обзорных исследований двухразового диализа в США не смогло выявить негативных последствий такого подхода, а итоги данной стратегии лечения оказались даже несколько лучше, чем при трехразовом диализе. Правда, отсутствие указанных последствий могло быть вызвано преобладанием среди наблюдаемых пациентов людей с остаточной функцией почек (Hanson, 1999), но убедительных свидетельств в пользу этого объяснения нет.
Е. Показатели адекватности диализа помимо клиренса по мочевине
1. Продолжительность процедуры диализа. Выведение мочевины - лишь один из показателей адекватности диализа. Для эффективного удаления из организма веществ, таких как фосфаты и молекулы со средней молекулярной массой, важнейшим параметром является общее время, затраченное на диализ в неделю. Если время недельного диализа укорочено, то невозможно эффективно и безопасно вывести из организма и излишки жидкости.
Рабочая группа KDOQI 2006 г. по адекватности гемодиализа рекомендует как минимум трехчасовую длительность процедур для пациентов с остаточной функцией почек при 3-разовом диализе. В рекомендациях Европейской группы по наилучшей практике 2002 г. устанавливается минимальная продолжительность сеанса в 4 часа. Преимущества диализа продолжительностью 3,5 часа неясны и наиболее выражены в Японии и в меньшей степени в Европе. В США эти преимущества трудно продемонстрировать (Tentori, 2012) , возможно, потому, что принято использовать более интенсивный диализ. Кроме того, на эффект дозы диализа на твердые исходы может влиять предвзятость, связанная с достижением целевой дозы (dose-targeting bias), состоящая в том, что выживаемость может быть лучшей у пациентов, которые достигают целевой дозы, какой бы она не была установлена (Daugirdas, 2013) . В США средняя продолжительность диализа - 3,5 часа, но наблюдается тенденция к ее увеличению до 4 часов, вслед за остальными странами. В настоящее время в США проводится крупное рандомизированное исследование (TiMe Trial), цель которого - определить, приведет ли установка продолжительности диализа 4 ч 15 мин для новых пациентов, независимо от их массы тела, к значимому улучшению прогноза. Существенное число пациентов в США получают диализ в центрах, каждую ночь в течение 6-9 часов. Данная практика более подробно описана в главе 16.
Еще одним аргументом против ориентирования диализа на Kt/V является довод, что данный показатель зависит от клиренса мочевины, что требует применения высокоэффективного диализа, больших диализаторов и скоростей потока крови, что, в свою очередь, ведет к нарушению равновесия растворенных веществ (дизэквилибриум) и к возможным нежелательным эффектам во время процедуры. К тому же для обеспечения высоких потоков крови требуется применение более толстых игл, которые с большей вероятностью могут вызвать турбулентность крови и тромбообразование, а значит, стать причиной дисфункции сосудистого доступа. Возникает также вопрос, следует ли «оптимизировать» диализ в рамках избранной продолжительности, используя более высокие скорости потока крови на протяжении всей процедуры и самые эффективные диализаторы (с более высоким коэффициентом массопереноса К0А), которые только может позволить себе медицинское учреждение. Альтернативный, «мягкий» диализ остается популярным в Европе. При таком подходе используются низкие скорости потока крови и относительно небольшие диализаторы. Рандомизированных исследований, позволяющих сделать обоснованный выбор между двумя указанными стратегиями, до сих пор не существует. Поэтому на сегодняшний день лучшим подходом, по-видимому, является определение целевых доз диализа на основе продолжительности процедуры и Kt/V (возможно, с более высокими минимумами целевых показателей для женщин и небольших пациентов). Если же при подборе дозы диализа заменить показатель Kt/V на BSA, то малое время процедуры для женщин и небольших пациентов становится бессмысленным, поскольку доза диализа, рассчитанная по BSA, у них существенно больше, а это требует увеличения продолжительности процедуры.
II. ПЕРВИЧНОЕ НАЗНАЧЕНИЕ ДИАЛИЗА
А. Доза диализа: К х t. Назначение диализа предполагает установку двух основных параметров: К - клиренс диализатора и t - время процедуры. К зависит от размера используемого диализатора и скорости потока крови. Скорость потока диализирующего раствора также играет свою небольшую роль, как было показано в главе 3.
1. Клиренсдиализатораобычнонаходитсяв диапазонеот200 до260мл/мин. Для взрослых пациентов, при потоке крови в 400 мл/мин, К будет примерно 230 ± 30 мл/ мин. Для оценки клиренса диализатора и его коэффициента массопереноса (К0А), учитывая скорость кровотока, можно использовать калькулятор кинетики мочевины или номограмму (рис. 13.6). Если предположить, что для четырехчасовой процедуры диализа клиренс диализатора будет 250 мл/мин, то К х t будет 250 х 240 = 60 000 мл (60 л). Это соответствует объему крови с полностью удаленной из него мочевиной за время указанной процедуры.
2. Выбор К х t в зависимости от массы тела пациента и требуемого значения Kt/V. Допустим, клиренс равен 250 мл/мин, а продолжительность диализа - 4 часа. Какова должна быть масса тела пациента, чтобы наш диализ соответствовал существующим рекомендациям? KDOQI рекомендует придерживаться уровня (К х t)/V в 1,4 ед., чтобы фактическая доза оказалась выше 1,2. Мы вычислили, что за 4 часа диализа очистится 60 л крови (К х t). Если мы хотим достичь желаемого уровня Kt/V в 1,4, то V должен быть 60/1,4 = 43 л, что соответствует весу пациента в 78 кг. Дополнительно см. примеры в табл. 11.2 и 11.3.
Таблица 11.2 Первоначальное назначение параметров диализа конкретному пациенту для достижения целевого spKt/V
Задача: получить желаемый уровень spKt/V для конкретного пациента.
Шаг1. Оценить параметру пациента.
Шаг 2. Умножить V на желаемое значение Kt/V, чтобы получить требуемое Кхt.
Шаг 3. Вычислить требуемый клиренс К для заданного времени диализа t либо требуемое время t для заданного клиренса К.
Шаг 1. Оценка V. Данную оценку лучше производить при помощи антропометрических уравнений, учитывающих рост, вес, возраст и пол пациента, как предлагает Уотсон (Приложение А). Если пациент афроамериканец, следует добавить 2 кг к параметру Уотсон (Vant). Можно также использовать уравнения Юма-Уэйерса (Hume—Weyers) или номограмму из Приложения А. В результате данных вычислений объем (Vant) в нашем случае оказался около 40 л.
Шаг 2. Вычисление К х t. Если требуемое значение Kt/V -1,5, а V равен 40 л, следовательно, К xt равно 60 л.
Шаг 3. Вычисление требуемого К либо t. Желаемое К х t может быть достигнуто применением разных комбинаций клиренса (величина которого зависит от К0А, QB и QD) и времени диализа. Есть несколько компьютерных программ, позволяющих смоделировать варианты диализа и выдать для них соответствующие комбинации К и t. Для этой цели также существуют онлайн-калькуляторы, ссылки на которые можно найти в списке интернет-ресурсов в конце этой главы.
Как вычислить К, имея заданное время диализа t? Вопрос можно переформулировать так: какой диализатор и какие скорости потока крови и диализирующего раствора взять, чтобы получить требуемое значение К х t? Как и в предыдущем расчете, здесь нужно провести простые вычисления. Исходные данные:
Желаемый spKt/V = 1,5; Vant = 40 л; К х t = 60 л.

Таблица 11.3 Как определить необходимое время процедуры для двух диализаторов, исходя из заданной фактической скорости потока крови (QB)?

В. Влияние изменения массы тела во время процедуры на назначаемую дозу диализа. Для пациентов, которые набирают значительный вес между сеансами, потребуются более высокие значения Kt/V с заданным URR, чем для пациентов с минимальным набором веса (см. рис. 3.14 в главе 3). Например, для достижения URR в 70% следует назначать Kt/V не более 1,3, если не планируется удаление жидкости в процессе диализа, и Kt/V = 1,5, если потеря веса (UF/W) в результате ультрафильтрации достигает 6% (см. кривую 0,06 UF/W на рис. 3.14).
III. КОНТРОЛЬ ОБЕСПЕЧЕННОЙ ДОЗЫ ДИАЛИЗА. Доза диализа обычно оценивается по итогам месяца в соответствии с рекомендациями KDOQI по пред- и постдиализным уровням мочевины в плазме (Ur). Дополнительно или в качестве альтернативы можно контролировать клиренс диализатора in vivo во время каждой процедуры по клиренсу по натрию либо оценивать дозу диализа, отслеживая поглощение УФ-излучения отработанным диализирующим раствором, как описано в главе 3.
Пред- и постдиализные значения Ur используются для вычисления величины ДСМ (URR), которая затем, совместно со значениями UF/W и некоторыми поправками, позволяет определить spKt/V проведенного диализа. Один нюанс: при измерении ДСМ (URR) нужно тщательно следовать рекомендациям по взятию постдиализных проб крови. Если имела место значительная рециркуляция в сосудистом доступе и при взятии проб крови не использовалась техника остановки потока диализирующего раствора или уменьшения скорости потока крови, то показатели крови, взятой на анализ, могут быть заниженными из-за поступления в сосудисты й доступ очищенной крови из диализатора. K D O Q I рекомендует два метода взятия крови, описанные в табл. 11.4, а доводы в их пользу приведены в главе 3
Таблица 11.4 Рекомендации по взятию проб крови для определения постдиализного уровня мочевины крови

А. Методы вычисления spKt/V с использованием пред- и постдиализного уровня мочевины крови.
Определение по номограмме. Следует использовать график 3.14, как описано ранее. Предположим, что измеренный уровень U RR состави л 0,70 (70% ). В зависим ости от объема выведенной на диализе ж идкости (0,3 или 6% от массы тел) целевой уровень spKt/V проведенного диализа будет 1,3; 1,4 или 1,5 соответственно.
2. Более точные методы. Оптимальным методом, рекомендуемым K D O Q I, является вычисление Kt/V с помощ ью программы компьютерного моделирования кинетики мочевины. Базовы е принципы работы таких программ описаны в главе 3. Данные программы имеются в продаже, и по крайней мере, одна из них, Solu te Solver, доступна в Интернете по адресу w w w .ureakinetics.org.
IV. коррекция программы ДИАЛИЗА. Даже если для пациента уж е выбрана определенная программа диализа и стратегия лечения не меняется, показатели Kt/V, рассчитанного по итогам измерения URR, могут значительно отличаться от месяца к м есяцу. Причины этого не вполне понятны. Вероятно, имеют значение лабораторные ошибки в определении уровня Ur разными методами, отклонения от предписанной продолжительности процедуры и колебания клиренса диализатора. М ож ет быть полезным вычисление среднего значения spKt/V по итогам трех месяцев. Это позволит понять, достигается ли при лечении стандартный минимум spKt/V в 1,2.
Пример: Допустим, нам нужно получить значение spKt/V по итогам диализа в 1,5 ед. И меются данные ежемесячного мониторинга U RR и вычисленных при п омощи них значений spKt/V:

Среднее значение величин spKt/V равно 1,4. Это удовлетворяет критериям KDOQI адекватности диализа, но при необходимости достижения целевого значения spKt/V в 1,5 нужно увеличить числитель данного индекса (К х 1) на 1,5/1,4, то есть на 1,07 (7%). Теперь необходимо решить, какой из параметров (К или!) можно увеличить на 7% (или увеличить оба, чтобы их произведение тоже увеличилось на 7%).
Самый простой способ поднять значение Kt/V с 1,4 до 1,5 - увеличить время диализа на 7%. Для четырехчасовой процедуры это будет 17 минут (1,07 х 240 = 257 мин). В качестве другого варианта можно попробовать увеличить параметр К, перейдя на большую скорость потока крови, более производительный диализатор или большую скорость потока диализирующей жидкости. Часто бывает сложно поднять скорость потока крови выше определенного предела. Эффект от перехода на более эффективный диализатор можно оценить по номограмме зависимости клиренса от К0А на рис. 3.6. Повышение скорости потока диализирующего раствора до 800 мл/мин, которое обычно дает прирост клиренса на 5-10% при условии, что скорость потока крови >400 мл/мин, не всегда эффективно на некоторых современных диализаторах, где поток диализирующей жидкости изначально оптимизирован (Ward, 2011).
V. КОНЦЕПЦИЯ МОДЕЛИРОВАНИЯ ОБЪЕМА V. Преимуществом использования программы для моделирования диализа является то, что компьютер вычисляет объем выведенной мочевины, а затем, на основе полученного значения URR, изменения массы тела и продолжительности процедуры, рассчитывает объем тела, из которого была выведена мочевина. Для этого он использует метод «мраморных шариков», описанный в главе 3 (раздел VI). Важно понимать, что параметр V - это инструмент для оценки адекватности диализа. Он не всегда отражает истинный объем распределения мочевины в организме. Компьютер может оперировать только теми данными, которые в них заложены. Например, если значения URR, и соответственно spKt/V, резко упадут из-за партии бракованных диализаторов, то все, что компьютер будет знать об этом, это что Kt/V вдруг упал, но он не будет знать, что клиренс диализатора (К) тоже изменился. Более того, время процедуры (!) при этом не изменилось. Как тогда компьютер сможет объяснить внезапное уменьшение spKt/V, если произведение К х t для него осталось неизменным? Единственным выводом для компьютера в данном случае будет, что объем распределения мочевины в организме (V) увеличился. Значительное изменение истинного объема распределения мочевины пациента происходит довольно редко, поэтому увеличение смоделированного объема V обычно означает, что по каким-то причинам пациент получил дозу диализа меньше необходимой.
А. Индивидуальный мониторинг смоделированного объема V
Пример 1. У пациента в мае был достигнут уровень spKt/V в 1,5 ед., и компьютер смоделировал объем V = 43 л. Данные параметров, соответствующие последующим четырем месяцам, приведены ниже.
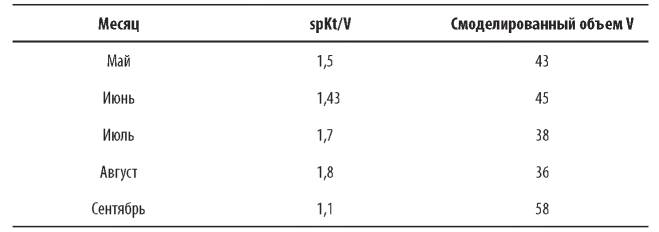
Был замечен временный всплеск параметра V в сентябре из-за неожиданно низкого индекса spKt/V. Что следует делать в таком случае?
Шаг 1. Проверить отчет о результатах диализа в сентябре. Низкий уровень spKt/V и скачок V, скорее всего, связаны с незафиксированным снижением К или 1. Необходимо ответить на следующие вопросы. Сокращалось ли время какой-либо процедуры? Снижалась ли скорость потока крови во время процедуры? Не мог ли концентрат диализирующего раствора закончиться во время процедуры? Наблюдались ли проблемы с сосудистым доступом? Если ответ на все эти вопросы отрицательный, можно предположить, что полученные данные - результат ошибки измерения.
Шаг 2. В случае если один из вышеперечисленных фактов имел место, не следует сразу корректировать программу диализа. Несколько дополнительных измерений пред- и постдиализного уровня Ur могут помочь понять, чем вызвано понижение spKt/V и на что нужно обратить особое внимание. В любом случае среднее сентябрьское значение spKt/V равно 1,1, что близко к рекомендованному KDOQI минимуму - 1,2. Результаты же следующего месяца помогут понять, насколько закономерны подобные изменения. Кроме того, значения клиренса, рассчитанные с использованием фактических результатов диализа, полученных измерением клиренса по натрию или поглощению УФ-излучения в диализате, будут большим подспорьем в дальнейших расчетах, поскольку их можно измерять на каждой процедуре. Это поможет понять причину снижения spKt/V в сентябре. Наиболее вероятной причиной достоверного снижения данного показателя может быть ухудшение кровотока в сосудистом доступе.
Другие возможные причины приводятся в табл. 11.5.
Пример 2 (выраженное падение величины V). Предположим, что у другого пациента по непонятным причинам наблюдается значительное увеличение spKt/V, приводящее к понижению смоделированного значения V
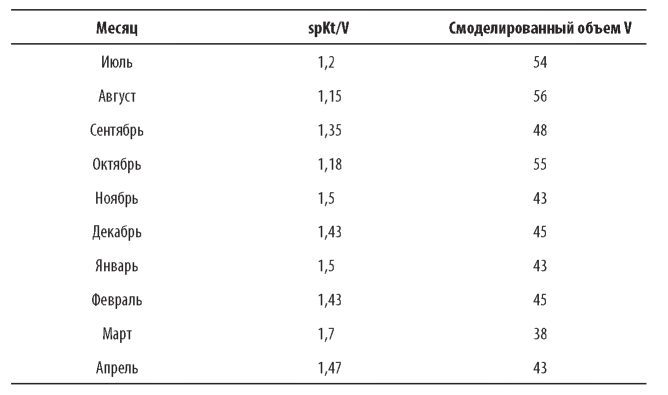
Возьмем пациента, объем V которого изначально был 54 л, а к ноябрю внезапно упал до 43 л. Показатель spKt/V увеличился с 1,2 до 1,5, несмотря на отсутствие изменений в лечении. Компьютер расценил это как «усыхание» пациента. Что могло стать причиной этого?
Шаг 1. Выяснить, не снизился ли «сухой вес» пациента. Если да, то с чем это связано: с улучшением выведения хронических излишков жидкости или изменением мышечной массы. Последнее может быть связано с сопутствующей патологией пациента.
Шаг 2. Проверить отчеты о результатах диализов. Если масса тела пациента уменьшалась незначительно, то и фактический объем распределения мочевины не должен был уменьшиться. А значит, вероятнее всего, увеличилось К х 1. Необходимо провести анализ отчетов о результатах процедур до октября и после. Возможно, обнаружится проблема, существовавшая до октября и препятствовавшая соблюдению назначенного режима процедур, устраненная к ноябрю.
ШагЗ. Оценить состояние сосудистого доступа и расположение игл при его пункции. Если в октябре с сосудистым доступом все-таки произошли какие-то изменения или имело место неправильное положение игл, то это могло повлиять на ухудшение кровотока в нем. А после октября проблема была обнаружена и устранена.
Шаг4. Проверить, не было ли принципиальных нарушений в технике взятия проб крови. Представим, что у пациента всегда был хороший кровоток в сосудистом доступе и до октября постдиализные пробы крови брались как положено - с предварительным снижением скорости потока крови в системе и с последующей остановкой насоса. Затем, в октябре, появился новый сотрудник, который брал пробы крови после простой остановки насоса, без предварительного снижения скорости потока крови. Это могло привести к внезапному и необъяснимому падению постдиализного уровня азота мочевины, которое стало следствием ложного роста показателей URR и spKt/V и как следствие - уменьшением величин смоделированного объема V.
Таблица 11.5 Причины, по которым spKt/V, рассчитанный исходя из величин URR, может отличаться от рекомендуемого уровня Kt/V

VI. СТАТИСТИКА ИЗМЕНЕНИЯ ОБЪЕМА V КАК ПОКАЗАТЕЛЬ КАЧЕСТВА РАБОТЫ ДИАЛИЗНОГО ЦЕНТРА.
Учитывая часто возникающие у некоторых пациентов изменения V, внедрение в диализном отделении мониторинга отклонений среднего значения смоделированного объема V как инструмента показателя качества очень актуально. Это позволяет выявить и устранить проблемы, возникающие при проведении диализа. Полезно также вычислять антропометрический объем V (Уш,), смоделированный объем V для каждого пациента и наблюдать их соотношение (V/V^,), которое должно быть близко к 0,9-1,0. Если больше единицы, это означает, что один из параметров К х t (или оба параметра) превышает необходимые величины.
VII. НЕВОЗМОЖНОСТЬ ДОСТИЖЕНИЯ ЖЕЛАЕМОГО УРОВНЯ spKVV. Пациенты, для которых уровень spKt/V в 1,2 оказывается труднодостижимым, обычно делятся на три категории: а) пациенты с несостоятельным сосудистым доступом, что приводит к ограничению скорости потока крови или к рециркуляции, иногда и к тому, и к другому; б) очень крупные пациенты; с) пациенты с гипотензией, стенокардией или другими симптомами, требующими частого понижения скорости потока крови во время процедуры.
А. Диализ 4 раза в неделю. Четырехразовый график проведения диализа становится особенно популярным для лечения более крупных пациентов, а также людей с повышенным артериальным давлением и проблемами с удалением из организма излишков жидкости. В рекомендациях KDOQI 2006 г. при таком графике, если остаточный клиренс по мочевине в собственных почках ниже 2 мл/мин на 1,73 м2, рекомендуется понизить минимальный уровень spKt/V с 1,2 до 0,8 ед. (табл. 11.1). Еще одно преимущество четырехразового графика в том, что он позволяет избежать длительного перерыва в диализе, приходящегося на конец недели, во время которого наиболее часто проявляются осложнения и происходят смертельные случаи среди диализных пациентов (Foley, 2011).
VIII. ВЫЧИСЛЕНИЕ И МОНИТОРИНГ СТАНДАРТИЗОВАННОГО БЕЛКОВОГО ЭКВИВАЛЕНТА ВЫВЕДЕНИЯ АЗОТА (nPNA - стБВА). Данная процедура описана в главе 3, а мониторинг нутритивного статуса обсуждается в главе 31.
IX. ВЫБОР ДИАЛИЗАТОРА
A. Материал мембраны. Проблемы, связанные с биосовместимостью мембран и острыми реакциями на них, обсуждаются в главах 4, 10 и 12.
B. Следует ли использовать с высокопроницаемые диализаторы (high-flux)? На этот вопрос частично отвечает рандомизированное исследование НЕМО, проведенное Национальным институтом здоровья США. Несмотря на то что применение highflux-мембран ассоциируется с повышением выживаемости пациентов примерно на 8%, данные итоги нельзя считать статистически значимыми, т. к. заметный рост данного показателя наблюдался у пациентов, лечившихся диализом к тому времени в среднем 3,7 года. Также у пациентов на диализе с использованием high-flux-мембран был ниже процент смертности от сердечно-сосудистых осложнений. Эти данные в целом коррелируют с итогами европейского исследования МРО5 (Locatelli, 2009). На основе результатов этих двух исследований в 2006 г. (а затем в 2015 г.) рабочая группа KDOQI по изучению адекватности диализа совместно с Европейской группой по наилучшей практике рекомендовала применение high-flux-мембран при условии обеспечения надлежащей подготовки воды для диализа. Использование high-flux-мембран может также снизить вероятность появления бета-2 микроглобулинового амилоидоза у пациентов, многие годы находящихся на диализе. Пока не ясно, вызвано ли это повышенным выведением бета-2 микроглобулинов или другими эффектами современных диализных технологий, связанных с применением high-flux-мем-бран, вызывающих снижение хронического воспаления.
X. РЕКОМЕНДАЦИИ ПО ВЫВЕДЕНИЮ ЖИДКОСТИ
А. Концепция «сухого веса» или оптимальная постдиализная масса тела. Так называемый сухой вес (лучше использовать термин «оптимальный вес после диализа») - это постдиализный вес, когда весь излишек жидкости (или его большая часть) был выведен из организма. Если «сухой вес» задан слишком высоким, то после диализа какая-то часть излишней жидкости останется в организме. В результате дополнительное поступление в организм жидкости между сеансами диализа может стать причиной водной перегрузки организма, отека и застоя в легких.
МРО - Membrane Permeability Outcome (Study) Если «сухой вес» занижен, избыточная ультрафильтрация может приводить к частым эпизодам гипотензии у пациента к концу процедуры, а после диализа -вызывать выраженное утомление, судороги и головокружение. Восстановление в междиализный период у таких пациентов происходит труднее.
На практике оптимальный постдиализный вес пациента приходится определять методом проб и ошибок. При расчете объема ультрафильтрации на процедуре следует учитывать 200 мл раствора хлорида натрия, которые пациент получает по завершении диализа в процессе возврата крови. Также нужно брать в расчет объем жидкости, получаемый пациентом с препаратами и питьем во время процедуры.
1. Частая корректировка оптимального постдиализного веса. Типичная ошибка персонала отделений диализа - недостаточно регулярная проверка и корректировка постдиализного веса пациента. Если пациент теряет вес за счет уменьшения массы тканей, рассчитанный ранее «сухой вес» становится завышенным, что может привести к гипергидратации и госпитализации пациента с клиникой водной перегрузки организма. Поэтому пересмотр оптимального постдиализного веса пациента хотя бы каждые 2 недели достаточно актуален.
Прогрессирующее уменьшение «сухого веса» может быть следствием скрытых проблем с усвоением питательных веществ или какого-либо патологического процесса. Как указывается в главе 33, клиническое определение оптимального постдиализного веса исходя из признаков отечности или хрипов в легких является недостоверным. Так, например, устройства с применением биоимпедансного анализа выявляют излишки жидкости в организме пациентов без внешних признаков гипергидратации.
Другая часть пациентов - те, чей оптимальный постдиализный вес был завышен (Hecking, 2013). Поскольку пациенты ориентируются на него, не прибегая к ограничению потребления натрия, это может приводить к значительным междиализным прибавкам веса, а в итоге - к ускоренной утрате остаточной функции почек. Измерение биоимпеданса вместе с другими технологиями, такими как «ультразвуковые кометы легких», или В-линии, которые более подробно обсуждаются в главе 33, помогает определить оптимальный постдиализный вес. Очевидно, что новые технологии приносят пользу, однако имеется лишь небольшой опыт работы с ними. В случае с измерением биоимпеданса тела, например, пока не ясно, насколько результаты оценки объема излишков жидкости в организме данным методом применимы для диализных пациентов с разными индексами массы тела.
В. Скорость удаления жидкости. Обычно жидкость удаляется с постоянной скоростью на протяжении всего диализа. Имеет смысл идея ограничения максимальной скорости ультрафильтрации в целях повышения качества процедуры. Факты показывают, что среди пациентов со скоростью ультрафильтрации <12 мл/кг массы тела в час выживаемость выше (Movilli, 2007). Пока не ясно, что лучше: ограничивать скорость ультрафильтрации в расчете на массу тела, площадь поверхности тела или ориентироваться на какую-либо постоянную величину (например <800 мл в час) (Lacson, 2014). Существует несколько подходов к снижению скорости ультрафильтрации. Наиболее очевидный способ - продление времени диализа. Однако снижение прибавки веса между процедурами путем ограничения потребления натрия зачастую более приемлемо и легко выполнимо для пациента (Burkart, 2012). Кроме того, у пациентов с сохраненной остаточной функцией почек снижения объема ультрафильтрации можно добиться путем увеличения суточного объема мочи с помощью назначения им диуретиков - если, конечно пациент намерен контролировать потребление жидкости. Интересным является также подход, при котором скорость ультрафильтрации изменяют в течение процедуры диализа, т. е. повышают на первые один-два часа диализа и понижают к концу процедуры. Для поддержания осмотического давления крови при таком профилировании в первые часы процедуры может потребоваться повышение концентрации натрия в диализирующем растворе. Преимущества данного подхода остаются спорными.
XI. РАСТВОРЫ ДЛЯ ДИАЛИЗА (табл. 11.6)
A. Скорость потока диализирующего раствора. Стандартная скорость потока диализирующего раствора - 500 мл/мин. Когда скорость потока крови высока (например, >400 мл/мин) и используется диализатор с высокой эффективностью (К0А), повышение скорости потока диализата до 800 мл/мин увеличивает клиренс диализатора (К) на 5-10%. Оптимальное соотношение скоростей потока диализирующего раствора и крови - 1,5-2,0.
B. Состав
1. Концентрация бикарбоната. В настоящее время бикарбонатные растворы для диализа становятся все более популярными, а использование растворов на основе ацетата в большинстве стран остается в прошлом.
Концентрация оснований должна быть рассчитана таким образом, чтобы преддиализный уровень бикарбоната в плазме был приблизительно 20-23 ммоль/л. Клинического преимущества повышения преддиализного уровня НСО3 выше 20-23 не наблюдается. У таких пациентов может развиваться постдиализный метаболический алкалоз, теоретически повышается вероятность образования кальций-фосфорного осадка и нарушения сердечного ритма.
Как уже обсуждалось в главе 4, в диализных аппаратах, в которых можно регулировать концентрацию бикарбоната, на мониторе отображается содержание бикарбоната в произведенном растворе без учета бикарбонат-образующих анионов, таких как ацетат или цитрат. Ацетат, в особенности, когда в концентрате используется диацетат натрия, может добавлять в раствор до 8 ммоль бикарбонат-образующих оснований. Об этой добавочной концентрации оснований следует помнить при титровании диализирующего раствора до соответствующего уровня бикарбоната в плазме. Средний уровень бикарбоната в диализирующем растворе несколько выше в США, чем в некоторых европейских странах, и это ассоциируется с повышенной смертностью (Tentori, 2013). Рост смертности связан больше с инфекционными событиями, чем с сердечно-сосудистыми осложнениями. Поэтому нельзя сказать определенно, случайна данная связь или это результат влияния каких-либо дополнительных факторов. У пациентов с пониженным уровнем бикарбоната плазмы в качестве дополнительного фактора выступала недостаточность питания и поступления в организм отдельных питательных веществ. Повышенное содержание бикарбоната в диализирующем растворе, действуя синергически с пониженными концентрациями кальция и фосфатов (Di Iorio, 2012), удлиняет интервал QT на электрокардиограмме, что повышает риск возникновения аритмий.
Таблица 11.6 Назначение диализного раствора

2. Уровень калия в диализирующем растворе. Обычная концентрация калия в растворе - 2 ммоль. Если преддиализный уровень калия в плазме <4,5 ммоль или пациент принимает сердечные гликозиды, концентрация калия в диализирующей жидкости должна быть увеличена до 3,0 ммоль. Если при использовании раствора с концентрацией калия 3 ммоль пробы крови во время диализа покажут повышенный уровень калия в плазме, может потребоваться постоянный прием полистиролсульфоната натрия. В настоящее время проходят клинические испытания новых, потенциально более безопасных и эффективных веществ, связывающих калий в ЖКТ, таких как ZS-9 (ZS Pharma, США) и Patiromer (Relypsa, США).
У пациентов с недостаточностью питания может наблюдаться пониженный преддиализный уровень калия в плазме. Для них с целью снижения риска гипокалиемии нужно использовать концентраты с повышенным содержанием калия. Во избежание же гиперкалиемии, с которой связан риск остановки сердца, необходим раствор с концентрацией калия 1,0 ммоль (Lafrance, 2006). Хотя, если используется таковой, то это следует делать в течение непродолжительного периода, потому что, если пациент по какой-либо причине прекращает употреблять продукты с высоким содержанием калия, дальнейшее использование диализирующего раствора с пониженным уровнем калия может привести к нежелательным последствиям. Наилучшая выживаемость наблюдается у пациентов, у которых на диализе использовался диализирующий раствор с концентрацией калия не менее 3 ммоль/л (Jadoul, 2012).
3. Уровень натрия в диализирующем растворе. Обычная концентрация натрия в растворах для диализа - от 135 до 145 ммоль. Уровень выше 138 ммоль приводит к повышению жажды и значительному набору веса в междиализный период, артериальное давление может повыситься, хотя во время диализа удаление лишней жидкости происходит лучше и без неприятных симптомов. Уровни натрия в растворе ниже 135 ммоль повышают вероятность появления гипотензии и судорог.
Одно из исследований предполагает, что у каждого пациента может быть свой «установочный» уровень натрия (Keen, 1997). Немного известно о причинах низкого преддиализного уровня натрия, гипонатриемию перед диализом связывают с гипергидратацией, и соответственно, набором веса между диализами. Гипонатриемия ассоциируется с повышенным риском смерти как у пациентов на диализе, так и у обычных людей. У них, как правило, имеет место нарушение сердечной функции, связанное с неосмотическим выделением в кровь вазопрессина, например, при синдроме «больных клеток» с нарушением в них ионного обмена калия и натрия. У пациентов с низким установочным уровнем натрия логично использовать диализирующий раствор с меньшим содержанием натрия, что может уменьшить постдиализную жажду и междиализную прибавку веса. Однако в одном из «срезовых» одномоментных исследований была выявлена лучшая выживаемость пациентов, у которых использовался диализат с повышенным содержанием натрия (Hecking, 2012).
4. Уровень глюкозы в диализирующем растворе. В США к растворам для диализа принято добавлять 200 мг/дл (или 11 ммоль/л) глюкозы. Ее содержание в диализирующем растворе может снизить риск развития гипогликемии во время диализа. В Европе обычно используют растворы с концентрацией глюкозы 100 мг/дл (или 5,5 ммоль/л). Возможно, европейцы правы, поскольку ряд данных показывает, что более низкий уровень глюкозы в растворах также предотвращает развитие гипогликемии, но позволяет лучше контролировать сахар крови. Кроме того, растворы с высоким содержанием глюкозы вызывают перемещение калия (и возможно, фосфатов) в клетки, препятствуя их выведению в процессе диализа.
5. Уровень кальция в диализирующем растворе. Для пациентов, принимающих современные, не содержащие кальция фосфат-биндеры, концентрация кальция в растворе для диализа, возможно, должна быть увеличена - во избежание дисбаланса ионизированного кальция в организме. По той же причине у пациентов, принимающих кальций-содержащие фосфат-биндеры, некоторые специалисты настаивают на использовании диализных растворов с концентрацией кальция ниже 1,25 ммоль (2,5 мЭкв/л). Однако низкие концентрации кальция в диализате, как показали исследования, повышают риск внезапной остановки сердца (Pun, 2013).
6. Уровень магния в диализирующем растворе. Обычная концентрация магния в диализных концентратах - 0,25-0,5 ммоль (0,5-1,0 моль-экв/л). У пациентов, не страдающих гипомагниемией, выживаемость выше. Распространенное в наши дни употребление ингибиторов протонной помпы может привести к снижению усвоения магния, поступающего с пищей и добавками, а значит, увеличить риск развития гипомагниемии (Alhosaini, 2014). Таким образом, использование концентратов с содержанием магния 0,5 ммоль (1,0 мЭкв/л), то есть на верхней границе нормы - современная тенденция.
С. Температура диализирующего раствора. Температура диализирующего раствора должна быть на наиболее низком уровне, не вызывающем еще дискомфорта у пациента - обычно в диапазоне 34,5-36,5 °C. Как обсуждается в главе 12, температура диализирующего раствора, устанавливаемая на полградуса ниже, чем температура барабанной перепонки пациента, может снизить риск развития интрадиализной гипотензии, предотвратить ощущение холода и озноба на процедуре и ускорить восстановление после диализа. Индивидуальный подход к установлению температуры диализирующего раствора также снижает вероятность негативных воздействий на миокард и связанных с диализом ишемических повреждений белого вещества мозга. В одном из исследований в Китае постоянное применение диализирующих растворов с пониженной температурой привело к снижению сердечно-сосудистой заболеваемости и смертности среди пациентов (Hsu, 2012).
XII. ПРИМЕНЕНИЕ АНТИКОАГУЛЯНТОВ ПРИ ДИАЛИЗЕ
См. главу 14.
XIII. НАЗНАЧЕНИЕ ПРИ ОСЛОЖНЕНИЯХ ДИАЛИЗА. Осложнения на диализе подробно обсуждаются в главе 12. Часто встречающиеся осложнения - такие как гипотензия, судороги, синдром беспокойных ног, тошнота, рвота, зуд и боль за грудиной, - могут регулироваться на диализе стандартными мероприятиями. Однако симптомы, появляющиеся во время диализа, могут указывать и на наличие более серьезных патологических процессов, требующих немедленного установления диагноза и соответствующего лечения.
XIV. МОНИТОРИНГ СОСТОЯНИЯ ПАЦИЕНТА
А. До и во время диализа
1. Перед процедурой
a. Вес. Преддиализный вес пациента следует сравнивать с весом после предыдущего диализа и с оптимальным для пациента весом с целью получения представления о динамике набора веса между процедурами. Значительная междиализная прибавка веса, особенно сопровождающаяся одышкой, требует проведения обследования сердечно-сосудистой системы и пересмотра оптимального постдиализного веса (скорее всего, он завышен). Пациентам следует набирать не более 1 кг в сутки, хотя в среднем увеличение междиализного веса у них значительно выше. В таких случаях следует прежде всего рекомендовать пациенту ограничить употребление жидкости, и что очень важно, поваренной соли, т. к. избыточное потребление воды происходит именно после приема соли. Повышенная жажда может быть также следствием повышенного содержания натрия в диализирующем растворе. Жалобы на утомление или повторяющиеся мышечные судороги после диализа могут говорить о том, что постдиализный вес пациента слишком мал. Как было сказано ранее, время восстановления после диализа можно сократить, если понизить температуру диализирующего раствора.
b. Артериальное давление. Уровень оптимального артериального давления при его мониторинге - вопрос спорный. Как среднее давление на протяжении процедуры, так и давление после диализа, возможно, лучше указывают на наличие перегрузки жидкостью, чем преддиализное давление (см. главу 33). У некоторых пациентов давление повышается во время процедуры, несмотря на выведение жидкости. Причины интрадиализной гипертензии не вполне ясны, но она связана с плохой выживаемостью. Пациентам со стойкой к снижению объема жидкости гипертензией иногда помогает дополнительное выведение жидкости, артериальное давление может снизиться лишь спустя несколько месяцев (Fishbane, 1996).
Во избежание интрадиализной гипотензии некоторым пациентам с повышенным давлением обычно рекомендуется не принимать гипотензивные препараты в день процедуры, однако это требование не обязательное, особенно в отношении тех, кто диализируется днем. Как добиться контроля артериального давления, описано в главе 33. Основным условием является ограничение поступления в организм натрия, увеличение суммарной недельной продолжительности диализа и, если есть такая возможность, увеличение количества диализов в неделю. Как показала практика, измерение биоимпеданса тела для контроля выведения лишней жидкости из организма помогает снизить артериальное давление. Приверженность к ограничению максимальной скорости ультрафильтрации (например, до 12 мл/час/кг веса) стимулирует пациентов контролировать набор веса между процедурами, что также способствует снижению артериального давления (Burkart, 2012).
Хотя пациентов с очень высоким уровнем артериального давления необходимо обследовать и, возможно, корректировать давление, очень агрессивные подходы связаны с увеличением эпизодов интрадиализной гипотензии и нарушением функционирования сосудистого доступа (см. главу 33).
c. Температура тела пациента. Температуру тела пациента необходимо контролировать. Повышенная преддиализная температура требует серьезного внимания и обязательного выяснения причины ее повышения. Проявление инфекционного процесса у диализного пациента может быть стертым. С другой стороны, повышение температуры тела на полградуса во время диализа является нормальным и не обязательно является следствием присутствия инфекции или проявлением пирогенной реакции в организме.
d. Сосудистый доступ. Независимо от температуры тела сосудистый доступ следует проверять перед каждой процедурой диализа на наличие признаков инфицирования.
2. Мониторинг во время сеанса. Артериальное давление и пульс, как правило, измеряются каждые 30-60 мин. Любые жалобы на головокружение, слабость могут указывать на гипотензию и требуют немедленного измерения артериального давления. Симптомы гипотензии могут быть невыраженными или вовсе отсутствовать, пока давление не упадет до угрожающих значений.
В. Лабораторные тесты (преддиализные значения)
1. Уровень мочевины крови. Данный параметр должен измеряться ежемесячно в качестве компонента оценки ДСМ (URR). Остается открытым вопрос, измерять ли уровень мочевины крови в тех случаях, когда клиренс диализатора измеряется in vivo путем определения проводимости диализата либо когда Kt/V пациента оценивается по поглощению им УФ-излучения. Однако определение преддиализного уровня азота мочевины актуально, поскольку позволяет вычислить стБВА (стандартизованный белковый эквивалент выведения азота - nPNA).
2. Уровень альбумина крови. Преддиализный уровень альбумина плазмы должен измеряться каждые 3 месяца. Данный параметр является важным индикатором алиментарного статуса пациента. Низкий уровень альбумина плазмы является плохим прогностическим признаком, предиктором смерти диализного пациента. Повышение риска смерти наблюдается при уровне альбумина <4,0 г/дл (40 г/л). Пациенты с уровнем альбумина в крови <3,0 г/дл (30 г/л) находятся в зоне очень высокого риска, поэтому необходимо приложить все усилия для выяснения и устранения гипоальбуминемии.
3. Уровень креатинина крови. Преддиализный уровень креатинина плазмы измеряется ежемесячно. Его обычное среднее значение у пациентов на гемодиализе - около 10 мг/дл (884 мкмоль/л), типичный диапазон - 5-15 мг/дл (440-1330 мкмоль/л). Парадоксально, но у диализных пациентов высокие уровни креатинина ассоциируются с уменьшением риска смерти, вероятно, потому, что являются показателем наличия мышечной массы и хорошего алиментарного статуса.
Уровни мочевины плазмы и креатинина должны измеряться и оцениваться в паре. Если наблюдается их параллельное изменение, следует пересмотреть программу диализа или заподозрить изменение остаточной функции почек. Если уровень креатинина остается постоянным, а уровень азота мочевины заметно меняется, то, вероятнее всего, пациент изменил количество употребляемого белка или изменился уровень катаболизма эндогенных протеинов.
4. Уровень общего холестерина крови. Данный уровень является показателем алиментарного статуса. Преддиализный уровень общего холестерина в 200250 мг/дл (5,2-6,5 ммоль/л) связан с самым низким риском смерти у диализных пациентов. Пониженный уровень общего холестерина, особенно если он ниже 150 мг/дл (3,9 ммоль/л), ассоциируется с повышением риска смерти, возможно потому, что отражает недостаточность питания.
5. Уровень калия крови. Пациенты с преддиализным уровнем калия в сыворотке крови в пределах 5,0-5,5 ммоль/л имеют самый низкий риск смерти. Риск значительно увеличивается при уровнях калия выше 6,5 ммоль/л или ниже 4,0 ммоль/л.
6. Уровень фосфора крови. Измеряется ежемесячно. Преддиализный уровень фосфатов, ассоциирующийся с наименьшей смертностью - ниже 5,5 мг/ дл (1,8 ммоль/л). Риск смерти резко возрастает при уровне фосфатов выше 9,0 мг/дл (2,9 ммоль/л) или ниже 3,0 мг/дл (1,0 ммоль/л). Текущие рекомендации KDIGO ставят целью «снижение уровня фосфора крови к нормальному диапазону». Значения данного показателя, как правило, повышены после трехдневного перерыва в процедурах диализа.
7. Уровень кальция в крови. Измеряется ежемесячно (чаще - при изменении дозы витамина D). Наименьший риск смерти имеет место при уровне кальция 9-12 мг/дл (2,25-3,0 ммоль/л). Риск значительно повышается при уровнях кальция выше 12 мг/дл (3,0 ммоль/л) или ниже 7 мг/дл (1,75 ммоль/л). Следует добиваться уровня кальция в пределах целевого диапазона. Не рекомендуется поддерживать его на верхней границе нормы из-за риска сосудистой кальцификации.
8. Уровень магния в крови. У диализных пациентов данный параметр не контролируется регулярно. Однако у пациентов, принимающих ингибиторы протонной помпы, нередко наблюдается гипомагниемия (Alhosaini, 2014), а это известный риск нарушений ритма сердца и худших сердечно-сосудистых исходов во многих популяциях пациентов. Соотношение цена/эффективность регулярного контроля уровня магния в крови пока не изучалось.
9. Уровень щелочной фосфатазы крови. Измеряется каждые 3 месяца. Высокие значения данного показателя являются признаком гиперпаратиреоза или болезней печени. Высокий уровень щелочной фосфатазы связан с повышенным риском смерти.
10. Уровень бикарбоната крови. Измеряется ежемесячно. Наименьший риск смерти - при уровне бикарбоната 20-22,5 ммоль/л. Смертность возрастает как при повышении, так и при понижении указанных пределов. Значительное увеличение смертности наблюдается при преддиализных значениях бикарбоната ниже 15 ммоль/л. Преддиализный ацидоз может быть корригирован щелочным питанием в междиализный период.
11. Уровень гемоглобина. Проверяется как минимум раз в месяц, а во многих случаях - каждые две недели. Становится популярным аппаратный способ измерения уровня гемоглобина с помощью оптических датчиков. Вопросы оптимальной коррекции анемии, связанной с хронической болезнью почек, рассматриваются в главе 34. Высокий уровень гемоглобина без лечения ЭСП может быть признаком поликистоза, приобретенного кистоза почек, гидронефроза или нефрокарциномы. Уровень ферритина и железа в плазме, а также ее железосвязывающая способность и индексы эритроцитов должны проверяться каждые 3 месяца.
12. Уровень аминотрансфераз в крови. Обычно проверяется 1 раз в месяц. Показатели, находящиеся на верхней границе нормы или превышающие их, могут свидетельствовать о бессимптомном течении какого-либо процесса в печени, особенно гепатита или гемосидероза. Кровь должна быть проверена на наличие поверхностного антигена гепатита В и на гепатит С (см. главу 35).
13. Уровни паратиреоидного гормона в плазме должны проверяться каждые 3-6 месяцев - подробно об этом в главе 36.
Ссылки и рекомендованная литература<>
/bAlhosaini М, et al. Hypomagnesemia in hemodialysis patients: role of proton pump inhibitors. Am J Nephrol. 2014; 39:204-209.
Cheung AK, et al. Effects of high-flux hemodialysis on clinical outcomes: results of the HEMO study. J Am Soc Nephrol. 2003; 14: 3251-3263.
Daugirdas JT. Dialysis time, survival, and dose-targeting bias. Kidney Int. 2013; 83: 9-13.
Daugirdas JT. Dialysis dosing for chronic hemodialysis: beyond Kt/V. Semin Dial. 2014; Tit 98-107.
Daugirdas JT, et al. Relationship between apparent (single-pool) and true (double-pool) urea distribution volume. Kidney Int. 1999; 56: 1928-1933.
Daugirdas JT. Second generation logarithmic estimates of single-pool variable volume Kt/V: an analysis of error. I Am Soc Nep hrol. 1993; 4: 1205-1213.
Depner T, et al. Dialysis dose and the effect of gender and body size on outcome in the HEMO Study. Kidney Int. 2004; 65: 1386-1394.
Di Iorio B, et al. Dialysate bath and QTc interval in patients on chronic maintenance hemodialysis: pilot study of single dialysis effects. I Nephrol. 2012; 25: 653-660.
Eknoyan G, et al. Effect of dialysis dose and membrane flux in maintenance hemodialysis. N Engl I Med. 2002; 347: 2010-2019.
European Best Practice Guidelines Expert Group. Haemodialysis. Nephrol Dial Transplant. 2002; 17 (suppl 7): S16-S31.
FHN Trial Group. In-center hemodialysis six times per week versus three times per week. N Engl I Med. 2010; 363:2287-2300.
Fishbane S, et al. Role volume overload in dialysis-refractory hypertension. Am I Kidney Dis. 1996; 28:257-261. Foley RN, et al. Long inter di alytic interval and mortality among patients receiving hemodialysis. N Engl I Med. 2011; 365: 1099-1107.
Hanson JA, et al. Prescription of twice-weekly hemodialysis in the USA. Am I Nephrol. 1999; 19: 625-633.
Hecking M, et al. Predialysis serum sodium level, dialysate sodium, and mortality in maintenance hemodialysis patients: the Dialysis Outcomes and Practice Patterns Study (DOPPS). Am I Kidney Dis. 2012; 59:238-248.
Hecking M, et al. Significance of interdialytic weight gain vs. chronic volume overload: consensus opinion. Am I Nephrol. 2013; 38:78-90.
Hsu HJ, et al. Association between cold dialysis and cardiovascular survival in hemodialysis patients. Nephrol Dial Transplant. 2012; Tit 2457-2464.
Jadoul M, et al. Modifiable practices associated with sudden death among hemodialysis patients in the Dialysis Outcomes and Practice Patterns Study. Clin I Am Soc Nephrol. 2012; 7:765-774.
Kalantar-Zadeh K, et al. Twice-weekly and incremental hemodialysis treatment for initiation of kidney replacement therapy. A m I Kidney Dis. 2014; 64: 181-186.
Karnik JA, et al. Cardiac arrest and sudden death in dialysis units. Kidney Int. 2001; 60: 350-357.
Keen М, Janson S, Gotch F. Plasma sodium (CpNa) “set point”: relationship to interdialytic weight gain (IWG) and mean arterial pressure (MAP) in hemodialysis patients (HDP) [Abstract]. J Am Soc Nephrol. 1997; 8: 241A.
Lacson, Jr, et al. Body size and gender dependent differences in mortality risks associated with ultrafiltration rates [Abstract]. J Am Soc Nephrol. 2013; 25.
Lafrance J, et al. Predictors and outcome of cardiopulmonary resuscitation (CPR) calls in a large haemodialysis unit over a seven-year period. Nephrol Dial Transplant. 2006; 21: 1006-1012.
Locatelli F, et al. Membrane Permeability Outcome (MPO) Study Group. Effect of membrane permeability on survival of hemodialysis patients. J Am Soc Nephrol. 2009; 20: 645-654.
Movilli E, et al. Association between high ultrafiltration rates and mortality in uraemic patients on regular haemodialysis: a 5-year prospective observational multicenter study. Nephrol Dial Transplant. 2007; 22: 3547-3552.
NKF-KDOQI clinical practice guidelines; update 2006. Am J Kidney Dis. 2006; 48 (suppl 1): S2-S90.
Pirkle JL, et al. Effect of limiting maximum ultrafiltration rate in an in-center hemodialysis population [Abstract]. J Aw Soc Nephrol. 2012; 23: 6A.
Pun PH, et al. Dialysate calcium concentration and the risk of sudden cardiac arrest in hemodialysis patients. Clin J Am Soc Nephrol. 2013; 8: 797-803.
Saran R, et al. Longer treatment time and slower ultrafiltration in hemodialysis: associations with reduced mortality in the DOPPS. Kidney Int. 2006; 69: 1222-1228.
Tentori F, et al. Association of dialysate bicarbonate concentration with mortality in the Dialysis Outcomes and Practice Patterns Study (DOPPS). Am J Kidney Dis. 2013; 62: 738-746.
Tentori F, et al. Longer dialysis session length is associated with better intermediate outcomes and survival among patients on in-center three times per week hemodialysis: results from the Dialysis Outcomes and Practice Patterns Study (DOPPS). Nephrol Dial Transplant. 2012; Tit 4180-4188.
Termorshuizen F, et al for the NECOSAD Study Group. Relative contribution of residual renal function and different measures of adequacy to survival in hemodialysis patients: an analysis of the Netherlands Cooperative Study on the Adequacy of Dialysis (NECOSAD)-2. J Am Soc Nephrol. 2004; 15: 1061-1070.
Twardowski ZJ. Safety of high venous and arterial line pressures during hemodialysis. Semin Dial. 2000; 13: 336-337.
Ward RA, et al. Dialysate flow rate and delivered Kt/Vurea for dialyzers with enhanced dialysate flow distribution. Clin I Am Soc Nephrol. 2011; 6: 2235-2239.
Интернет-ссылки
HDCN adequacy channel: http://www.hdcn.com/ch/adeq/.
NKF KDOQI guidelines for hemodialysis adequacy: http://www.kidney.org.
Urea kinetics calculators: http://www.ureakinetics.org.
