- Диализному врачу
- 1. Ведение пациентов с ХБП 4-5-й стадии.
- 2. Подготовка к трансплантации, диализу или к консервативной терапии
- 3. Физиологические принципы и моделирование кинетики мочевины
- 4. Оборудование для гемодиализа и расходные материалы
- 5. Вода для диализа и диализирующий раствор
- 6. Артериовенозные фистулы и протезы. Основные положения
- 7. Центральный венозный катетер в качестве доступа: основы
- 8. Мониторинг артериовенозного доступа и осложнений
- 9. Инфекции и другие осложнения центральных венозных катетеров
- 10. Назначение острого гемодиализа
- 11. Назначение хронического гемодиализа
- 12. Осложнения в ходе процедуры гемодиализа
- 13. Повторное использование диализаторов
- 14. Антикоагуляция
- 15. Продленная заместительная почечная терапия
- 16. Гемодиафильтрация
- 17. Терапевтический аферез
- 18. Актуальность сорбционных технологий сегодня
- 19. Руководство по диализу
Терапевтический аферез
Терапевтическим аферезом (ТА) называется группа методов экстракорпорального очищения крови, при которых из русла выводятся аномально измененные клетки крови и/или компоненты плазмы. Термины «плазмаферез», «лейкаферез», «эритроци-таферез» и «тробоцитаферез» образованы от названий компонентов крови, которые выводятся при этих процедурах. При плазмаферезе (ПА), или терапевтическом плаз-мообмене (ТПО), из системного кровообращения удаляются большие объемы плазмы и замещаются свежезамороженной плазмой (СЗП) или альбумином и физраствором.
I. ЛОГИЧЕСКОЕ ОБОСНОВАНИЕ ПЛАЗМАФЕРЕЗА. Существует несколько механизмов, благодаря которым плазмаферез оказывает терапевтический эффект (табл. 18.1). Основным механизмом его действия является быстрое снижение концентрации в крови специфичных, связанных с болезнью факторов. Другим эффектом является возможность выведения ряда высокомолекулярных белков, которые могут вносить свой вклад в процесс воспаления (интактные компоненты системы комплемента СЗ, С4, активированные компоненты системы комплемента, фибриноген и цитокины). Предположительно существуют другие механизмы влияния ПА на иммунитет, включая иммуномодулирующее действие, например, изменение баланса идиотипических и антиидиотипических антител или сдвиг соотношения концентраций антител и антигенов, приводящий к образованию более растворимых форм иммунных комплексов (что упрощает их удаление), а также стимуляция клонов лимфоцитов, повышающая эффективность цитотоксической терапии. ПА позволяет использовать нормальную плазму для восполнения тех ее составляющих, которые находятся в дефиците в организме пациента - это, возможно, принципиальный механизм действия ПА при лечении тромботической тромбоцитопенической пурпуры (ТТП).
Таблица 18.1 Возможные механизмы действия терапевтического плазмообмена

А. Принципы лечения
1. Использование сопутствующей иммуносупрессии. Из-за иммунологической природы большинства заболеваний, для лечения которых используется плазмаферез, практически всегда требуется сопутствующее применение иммуносупрессоров. Протоколы иммуносупрессии обычно включают введение повышенных доз кортикостероидов, цитотоксических средств, а также биологических агентов. Назначения этих препаратов предназначены для снижения уровня ресинтеза патогенных антител и для дальнейшего модулирования клеточного иммунитета, оказывая влияние на большинство иммунных нарушений.
2. Раннее начало лечения. Если болезнь отвечает на лечение ПА, терапию лучше начинать на ранних стадиях, чтобы минимизировать воспалительную реакцию, которая зачастую вносит свой вклад в течение заболевания. Например, плазмаферез при гломерулонефрите, вызванном наличием антител к гломерулярной базальной мембране (ГБМ), наиболее эффективен, если терапию начинают при концентрации креатинина <5 мг/дл (440 мкмоль/л).
II. ФАРМАКОКИНЕТИКА ВЫВЕДЕНИЯ ИММУНОГЛОБУЛИНОВ (lg)
A. Периоды полувыведения веществ из плазмы. Иммуноглобулины имеют относительно большие периоды полувыведения - примерно 21 сутки для IgG и 5 суток для IgM, поэтому от иммуносупрессоров, подавляющих их образование, не следует ожидать снижения концентрации патогенных аутоантител в плазме, по крайней мере, в течение первых нескольких недель, даже если образование иммуноглобулинов полностью блокировано. Это является основной предпосылкой для выведения таких антител экстракорпоральными методами.
B. Внесосудистое распределение и скорость выравнивания концентраций 1д. Иммуноглобулины имеют значительное экстраваскулярное распределение (табл. 18.2). Соотношение внутрисосудистого и внесосудистого распределения иммуноглобулинов определяет эффективность их выведения в рамках одного сеанса ПА. Скорость уравновешивания интраваскулярного распределения в сторону экстраваску-лярного - примерно 1-2% в час; в обратном направлении - несколько быстрее, поскольку тогда оно управляется скоростью тока лимфы, но все-таки недостаточно быстрое, поэтому кинетика выведения иммуноглобулинов при плазмо-обмене может рассчитываться с применением уравнений, описывающих кинетику первого порядка при выведении веществ из одного компартмента (в данном случае - внутрисосудистого пространства).
Таблица 18.2 Объемы распределения иммуноглобулинов
C. Процент снижения макромолекул и V^Vp.
В главе 3 описывается взаимоотношение процента снижения концентрации мочевины (URR) и Kt/V. Похожее взаимоотношение имеет место при выведении иммуноглобулинов при ТПО.Кинетика их выведения подчиняется следующей экспоненциальной зависимости:
С, = Coe-ve/vf
где Со - начальная концентрация макромолекул вещества в плазме, Ct - концентрация в момент времени t, Ve - объем плазмы, подвергнутый обмену к этому моменту, и Vp - виртуальный объем плазмы, который хоть и меньше объема распределения макромолекул большинства из этих веществ, но выступает в роли объема, из которого они выводятся, и может использоваться благодаря низкой скорости эквилибрации концентраций между экстраваскулярным и интраваскулярным пространствами.
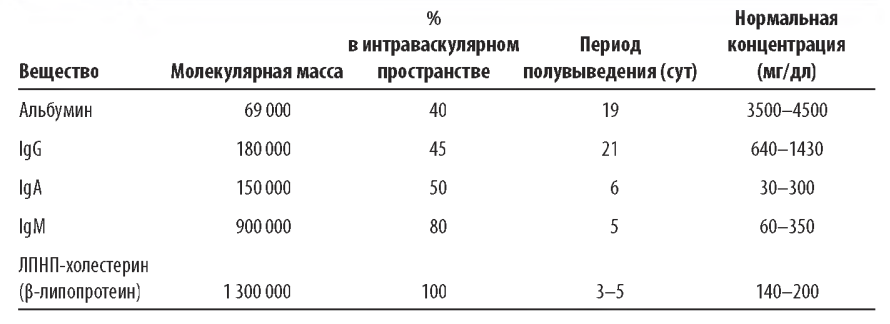
Процент снижения макромолекул (MRR2) равен 100 х (1 - С,/Со), поэтому MRR = 100 х (1 - e~Ve'vp). Если подставить сюда значения для Ve от 1400 до 8400 мл (табл. 18.3) и предположить, что Vp пациента равен 2800 мл, то соотношение Ve/Vp будет в пределах от 0,5 до 3,0. ТПО с использованием этих величин будет выражаться в значениях MRR (табл. 18.3) в диапазоне от 39% (при Ve/Vp = 0,5) до 95% (при Ve/Vp = 3,0). Стоит отметить, что при Ve/Vp = 1,0, MRR = 63%. Наибольшее снижение концентрации макромолекул происходит при выведении первой порции плазмы; выведение последующих порций во время той же процедуры становится все менее эффективным в плане уменьшения концентраций выводимого вещества. Эффективность процедуры после первой порции плазмы уменьшается из-за дилюции выводимого вещества замещающей жидкостью. По этой причине за одну процедуру плазмафереза обычно производится обмен 1,0-1,5 эквивалентных объема плазмы (Ve/Vp).
D. Реаккумуляция. Вслед за выведением макромолекул какого-либо вещества происходит их реаккумуляция в сосудистом русле вследствие двух процессов - перераспределения и продолжающегося синтеза. Перераспределение из экстравас-кулярного пространства происходит посредством дренажа лимфы, а также путем диффузии макромолекул через капилляры из межклеточного пространства в интраваскулярное. Эндогенный синтез встречается при синдроме Гудпасчера, при котором концентрацию антител к ГБМ удается гарантированно снизить путем применения ПА, однако увеличение их концентрации в плазме в промежутках между процедурами происходит слишком быстро, чтобы его можно было объяснить простым уравновешиванием концентраций с внесосудистым пространством.
Таблица 18.3 Соотношение между выводимым объемом плазмы и концентрациями содержащихся в ней веществ
Е. Фармакокинетические основы назначения ТПО. С учетом на перечисленных концепций, рациональный подход к ПА заключается в плазмообмене одного объема плазмы ежедневно или через день, в зависимости от течения болезни, чтобы дать макромолекулам время для адекватного перераспределения посредством дренажа лимфы в пространство крови. Скорость аккумуляции и частота ТПО специфичны для макромолекул конкретного патогена, подлежащего выведению, поэтому следует изучить данные о нем (если они имеются). Например, если нужно вывести IgM, то может быть целесообразным более продолжительный ПА, так как ожидаемая скорость эндогенного синтеза IgM выше, чем у IgG. Кроме того, распределение IgM преимущественно интраваскулярное, в то время как IgG распределяется главным образом в экстраваскулярном пространстве. Поэтому при выведении IgM антител или парапротеинов предписывается ежедневный ПА. А пациенты, у которых предполагается наличие аутоантител к IgG, должны получать процедуры через день, чтобы дать антителам время для перераспределения из внесосудистого пространства во внутрисосудистое. Если концентрации веществ, подлежащих выведению (например, уровень специфических аутоантител в плазме), могут быть измерены надежными количественными методами, то лечение следует выстроить так, чтобы обеспечить значительное уменьшение концентраций данных веществ, основываясь на кинетических принципах. Если терапия проводится без идентификации патогенного агента, то врачу остается использовать эмпирический подход при составлении плана лечения.
F. Оценка объема циркулирующей плазмы. Для назначения адекватного плазмафереза требуется оценить объем циркулирующей плазмы. Для этой цели существует ряд номограмм и уравнений, использующих рост, вес и гематокрит (Het) пациента. Данные методы расчета применяются и в современных аппаратах для плазмафереза. Принято считать, что объем плазмы составляет 35-40 мл на 1 кг тощей массы тела, и значение 35 мл/кг берется для пациентов с нормальным гематокритом, а 40 мл/кг - для пациентов с субнормальным гематокритом.
Например, для пациента 70 кг с нормальным гематокритом (45%) объем плазмы (Vp) будет 70 х 40 = 2800 мл. Уравнения для расчета объема крови были выведены из графиков взаимосвязи действительных объемов крови, измеренных с помощью альбумина, помеченного радиоактивным изотопом (йод-131), и параметров тела - роста (в см) и массы (в кг): Vp = (1 - Het) (b + cW), где W - тощая (безжировая) масса тела; константа b = 1530 для мужчин и 864 для женщин; и константа с = 41 для мужчин и 47,2 для женщин. Следует помнить, что данные расчеты основываются на тощей массе тела, и для пациентов с ожирением должна браться именно она - во избежание ненужного и опасного повышенного объема плазмообмена.
III. ТЕХНИЧЕСКИЕ ОСОБЕННОСТИ ПЛАЗМАФЕРЕЗА. ТИО может производиться с применением центрифуг для сепарирования клеток крови либо с помощью мембранной плазмо-сепарации (MPS3). Центрифужные аппараты обычно используются для заготовки донорской крови в банках крови, поскольку помимо плазмафереза могут производить селективное сепарирование клеток крови - цитаферез. При MPS используются высокопроницаемые половолоконные мембраны - наподобие тех, которые применяются в диализаторах, но с большим размером пор, а также диализное оборудование, модифицированное соответствующим образом. Преимущества и недостатки каждой из техник перечислены в табл. 18.4.
А. Аферез с центрифужной плазмосепарацией. В центрифуге кровяные клетки сепарируются под действием гравитации благодаря различной плотности компонентов крови. Применяется два типа центрифугирования для сепарации клеток крови: непрерывно-поточное и прерывисто-поточное. При вращении центрифуги эритроциты перемещаются к внешней стенке емкости, содержащей кровь, в то время как плазма, более легкий компонент, располагается ближе к внутренней стенке емкости. Тромбоциты и лейкоциты располагаются между слоями плазмы и эритроцитов. Любые из этих компонентов могут быть отделены, собраны, удалены или возвращены в систему кровообращения (рис. 18.1).
В установках с прерывисто-поточным центрифугированием промежуточные порции крови (аликвоты) отбираются из устройства, обрабатываются и возвращаются пациенту. При непрерывно-поточном центрифугировании кровь забирается из организма, сепарируется в центрифуге, и необходимый компонент крови отделяется и возвращается пациенту в непрерывном режиме, с использованием кольцевидного разделительного ротора с особым образом расположенными портами для сбора плазмы, эритроцитов, лейкоцитов и тромбоцитов (рис. 18.1). Аферез прерывисто-поточным методом производится через одноигольный сосудистый доступ, в то время как при непрерывно-поточном методе требуется применение двухпросветных катетеров, похожих на диализные. В настоящее время установки для прерывисто-поточного центрифугирования крови (производства «Гемонетикс»4, США) редко применяются для терапевтического афереза. Для терапевтических процедур предпочтительнее использование непрерывно-поточного центрифугирования - из-за небольшого объема экстракорпорального контура, значительно меньшей продолжительности процедур и сниженной потребности в антикоагуляции. Наиболее широко применяемые сепараторы на основе центрифуг для терапевтического афереза производятся компаниями «Терумо»5 (США) и «Фрезениус Каби»6 (Германия).
Таблица 18.4 Сравнение мембранной плазмосепарации и центрифужного афереза

В. Аферез с мембранной плазмосепарацией (MPS). Плазмофильтрация. Действие мембранных сепараторов плазмы основано на тех же принципах, которые используются в диализе. Половолоконные фильтры таких сепараторов очень похожи на фильтры диализаторов. Напрашивается простая смена диализатора в диализной установке на фильтр-сепаратор для MPS с последующей процедурой гемофильтрации без диализирующего раствора. Однако сепарирование плазмы физиологически отличается от ультрафильтрации: когда вода выводится из интраваскулярного пространства, жидкость из экстраваскулярного пространства стремится компенсировать данное выведение посредством диффузии; когда плазма выводится из интраваскулярного пространства, скорость ее восполнения значительно ниже, поэтому возрастает риск сердечно-сосудистых осложнений в ходе плазмообмена. Для обеспечения безопасности пациента следует использовать только специальное оборудование для мембранной плазмосепарации.
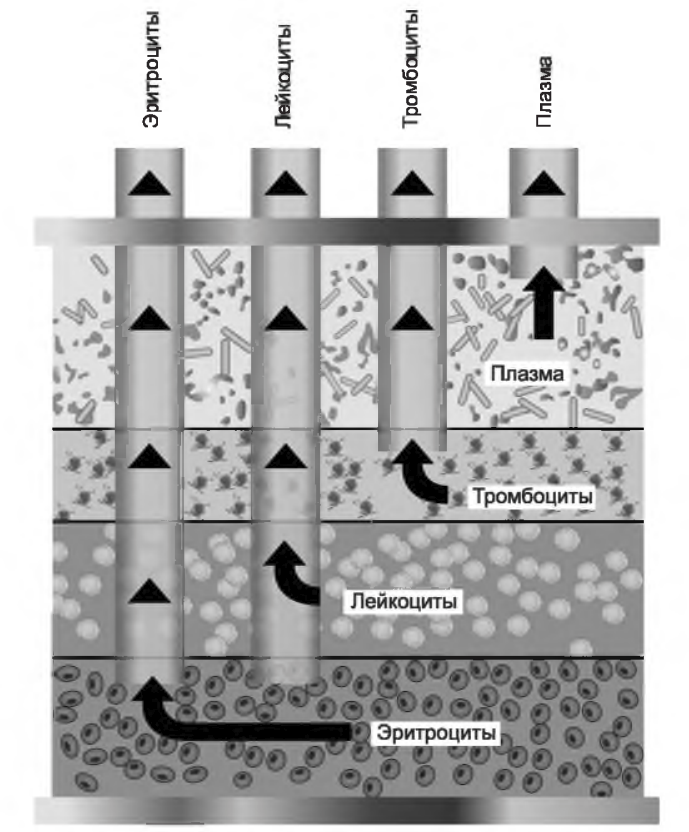
РИСУНОК 18.1. При центрифужном аферезе плазма и клетки крови специфически сепарируются под действием гравитации, в зависимости от их плотности. Каждый из полученных слоев может быть выведен отдельно, в зависимости от проводимой процедуры, типа замещающей жидкости и/или необходимости одновременного обмена клеток (Courtesy оf Dobri Kiprov, MD. Reprinted from Linz W, et al. Principles o f Apheresis Technology. 5th ed. American Society for Apheresis; 2014. www.apheresis.org.)
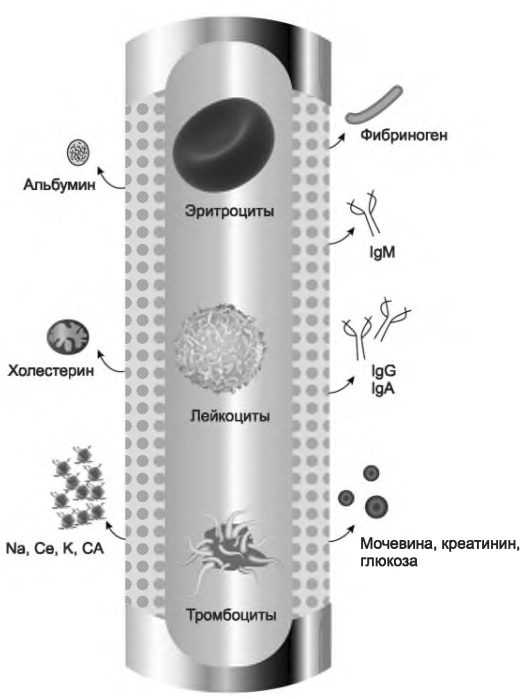
Для MPS применяются мембраны с отсечкой молекул с молекулярной массой выше 3 млн Да, что достаточно для прохождения через них иммунных комплексов (молекулярная масса которых около 1 млн Да). Фильтры для MPS могут производиться на основе половолоконных мембран либо в плоскопараллельной конфигурации. Примером половолоконного сепаратора может служить плаз-мофильтр «Плазма-Фло»7 производства «Асахи»8. Мембрана пропускает только плазму, поскольку ее поры достаточно малы, чтобы через них проникали компоненты крови. Мембрана имеет коэффициент просеивания 0,8-0,9 для альбумина, IgG, IgA, IgM, СЗ, С4, фибриногена, холестерина и триглицеридов (при скорости потока крови 100 мл/мин и трансмембранном давлении 40 мм рт. ст.) (рис. 18.2). Ряд производителей предлагает либо модифицированное оборудование для CRRT, либо специальные аппараты для мембранного плазмафереза.
Мембранная плазмосепарация должна производиться при низком трансмембранном давлении (<500 мм рт. ст.) - во избежание гемолиза. При использовании половолоконных фильтров скорость потока крови должна быть больше 50 мл/мин - для предотвращения тромбообразования. Идеальная скорость потока крови (Qb), как правило, равна 100-150 мл/мин. Если Qb = 100 мл/ мин, можно ожидать скорости плазмофильтрации на уровне 30-50 мл/мин. Таким образом, среднее время, необходимое для проведения стандартного мембранного плазмафереза (при Ve = 2800 мл) - менее 2 часов (40 мл/мин х 60 мин = 2400 мл/час).
РИСУНОК 18.2. При мембранной плазмосепарации через фильтр не проникают клетки крови, а только вещества, содержащиеся в плазме (Courtesy of Dobri Kiprov, MD. Reprinted from Linz W, et al. Principles ofApheresis Technology. 5th ed. American Society for Apheresis; 2014. www.apheresis.org.)
С. Сравнение устройств для мембранной и центрифужной плазмосепарации (табл. 18.4). В США для терапевтического афереза предпочтитают использовать сепараторы компонентов крови на основе центрифуг. Помимо плазмафереза они способны производить цитаферез (лейкаферез, эритроцитаферез и тромбоцитаферез). К тому же такие устройства используют более низкие потоки цельной крови и плазмы (Qb в диапазоне 40-50 мл/мин). MPS позволяет производить плазмаферез быстрее. Однако он не подходит для лечения пациентов с синдромом повышенной вязкости крови вследствие парапротеинемии (как правило, мак-роглуболинемии Вальденстрема) или пациентов с криоглобулинемией, так как доступные устройства не предназначены для выведения очень больших макромолекул. Обычно MPS производится с использованием гепарина в качестве антикоагулянта, а при лечении заболеваний, сопровождающихся кровотечениями, таких как ТТП, вместо гепарина применяется цитратная антикоагуляция.
IV. СОСУДИСТЫЙ ДОСТУП. Как уже было отмечено ранее, при центрифужном аферезе достаточно потока крови в 40-50 мл/мин. Иногда такие потоки могут обеспечиваться сосудистым доступом через крупные периферические вены (например, локтевую вену). При MPS, напротив, необходим центральный венозный доступ, так как для успешной фильтрации требуется поток крови в 100-150 мл/мин. Для MPS лучше использовать двухпросветный катетер с большим диаметром - похожий на те, что применяются при диализе и которые специально спроектированы для плазмафереза. Большинство устройств для сосудистого доступа, предназначенных для целей, не связанных с диализом, таких как катетеры Свана-Ганса и трехпросветные катетеры, почти никогда не могут обеспечить адекватный поток крови для проведения плазмафереза, хотя они могут подойти для возврата крови.
Инфузии цитрата (см. далее) приводят к резкому снижению концентрации ионизированного кальция в плазме (даже при нормальном общем уровне кальция), что может вызвать локальное нарушение сердечной проводимости с последующей аритмией и угрозой для жизни - особенно если кровь возвращается через центральный венозный доступ, когда кончик катетера располагается в непосредственной близости от атриовентрикулярного узла. Следует контролировать сердечный ритм, а также использовать устройства для подогрева крови, особенно если возврат крови производится посредством центрального доступа.
Когда терапия заболевания требует применения хронического ТПО (например, при гиперхолестеринемии или криоглобулинемии), предпочтительна организация постоянного сосудистого доступа. Пациентам могут устанавливаться центральные катетеры на длительный срок, либо формируется артериовенозная фистула или фторопластовые сосудистые протезы (сосудистые протезы из PTFE9).
V. АНТИКОАГУЛЯЦИЯ. Для процедур терапевтического афереза антикоагуляция обязательна, как при мембранной, так и при центрифужной плазмосепарации. Как правило, в первом случае используют гепарин, а во втором - цитрат.
A. Гепарин.
Чувствительность к гепарину и период его полувыведения у разных пациентов могут сильно отличаться, поэтому необходим индивидуальный подбор дозы. Доза гепарина может быть увеличена для пациентов с низким гематокритом (повышенным объемом распределения) и при высокой скорости сепарации плазмы (которая приводит к повышенному выведению гепарина, коэффициент просеивания для которого - 1,0).B. Цитрат. В большинстве процедур ТПО используется цитратно-глюкозный раствор для антикоагуляции (ACD10). Цитрат образует хелатные комплексы с кальцием, являющимся необходимым кофактором в каскаде реакций коагуляции и вносящим, таким образом, существенный вклад в процессы тромбообразования и агрегации тромбоцитов. ACD поставляется в двух стандартных составах: формула A (ACD-A) содержит 2,2 г/дл цитрата натрия и 0,73 г/дл лимонной кислоты; формула В (ACD-В) содержит 1,32 г/дл цитрата натрия и 0,44 г/дл лимонной кислоты. ACD-A применяется для всех устройств с непрерывно-поточным центрифугированием. Хотя кровотечения при цитратной антикоагуляции происходят не часто, снижение уровня ионизированного кальция - типичное явление. Поэтому следует тщательно следить за появлением у пациентов симптомов и признаков гипокальциемии (парестезия вокруг рта и/или кончиков пальцев; у некоторых пациентов может наблюдаться дрожь, головокружение, судороги, тремор и редко продолжительные мышечные сокращения, переходящие в непроизвольный спазм запястья).
Если уровень ионизированного кальция падает значительно, симптомы могут перерасти в выраженную тетанию, со спазмами других групп мышц, включая угрожающий жизни ларингоспазм. Также сообщается о случаях тонико-клонических судорог (grand mat). Данные симптомы и признаки могут усугубляться наличием алкалоза вследствие гипервентиляции. Снижение уровня ионизированного кальция в плазме также удлиняет фазу плато деполяризации миокарда, что проявляется на ЭКГ в виде удлинения интервала QT. Очень высокие концентрации цитрата в сочетании с пониженным уровнем ионизированного кальция приводят к подавлению сократительной функции миокарда, что, хотя и очень редко, может провоцировать фатальные аритмии у пациентов, получающих лечебный ПА.
1. Предотвращение снижения уровня ионизированного кальция при цитратной антикоагуляции. В качестве профилактики следует рассматривать следующие меры.
а. Снижение скорости инфузии цитрата пациенту - объем поступающего цитрата не должен перекрывать возможности его метаболизма в организме в зависимости от индивидуальных особенностей больного. Поскольку скорость инфузии цитрата пропорциональна скорости потока крови, следует избегать больших скоростей. В большинстве установок для плазмафереза на основе центрифуг объем крови пациента оценивается по номограмме, после чего скорость потока крови устанавливается автоматически, задавая предел скорости инфузии цитрата.
У пациентов с печеночной и почечной недостаточностью метаболизм цитрата может быть ухудшен, и цитратная антикоагуляция для них должна производиться с большой осторожностью. Свежезамороженная плазма содержит до 14% цитрата от объема. В случаях, когда такая плазма вместо альбумина используется в качестве возмещения, общий объем инфузии цитрата в организм должен рассчитываться с учетом этого содержания.
Ь. Дополнительное назначение кальция при ПА. Кальций назначается перорально либо внутривенно. Можно, например, давать пациенту таблетки 500 мг (5 ммоль) карбоната кальция каждые 30 минут. Другим способом является постоянное внутривенное введение 10% раствора глюконата кальция (10 мл на 1 литр замещающей жидкости) (Weinstein, 1996). В дополнение к этим мерам могут вводиться внутривенные болюсы препаратов кальция при появлении симптомов гипокальциемии.
2. Алкалоз при введении цитрата. Существует опасность развития метаболического алкалоза (хотя и крайне редкая) - из-за того, что цитрат натрия превращается в организме в бикарбонат. Для пациентов с поражением печени и возможными нарушениями метаболизма цитрата необходим тщательный мониторинг кислотно-основного состояния крови во время проведения плазмафереза с цитратной антикоагуляцией.
VI. ТИПЫ ЗАМЕЩАЮЩЕЙ ЖИДКОСТИ. Выбор типа и количества замещающей жидкости -важный момент при назначении ПА и ТПО. Разнообразие заболеваний и состояний пациентов усложняет разработку стандартных рекомендаций по выбору замещающей жидкости. Тем не менее будет полезно привести здесь некоторые советы, касающиеся такого выбора, а приведенные рекомендации могут быть модифицированы в соответствии с конкретными условиями.
При большинстве процедур ПА для поддержания гемодинамической стабильности требуется обмен плазмы коллоидными растворами. На практике выбор ограничен изонатриевым 5% раствором альбумина и свежезамороженной плазмой. Преимущества и недостатки каждого из субституатов приведены в табл. 18.5.
А. Свежезамороженная плазма (СЗП). СЗП схожа по составу с фильтратом, выводимым в процессе плазмафереза, но ассоциируется с появлением побочных эффектов, таких как аллергические реакции. Часто наблюдается кожная сыпь по типу крапивницы, которая может быть выраженной. В редких случаях анафилактические реакции проявляются в форме некардиогенного отека легких, вызванного пассивной трансфузией лейкоагглютининов. Еще одной причиной анафилактических реакций может стать инфузия СЗП, содержащей иммуноглобулин А (IgA), пациентам с селективным дефицитом IgA. Поскольку СЗП может содержать существенные количества анти-А и анти-В изоагглютининов, необходима АВО-совместимость крови донора и реципиента. Как уже было сказано ранее, такая плазма содержит цитрат, и ее использование повышает риск реакций организма на снижение уровня ионизированного кальция в ответ на поступление цитрата. К тому же существует небольшая, но имеющая статистику вероятность передачи через СЗП гепатита В (0,0005% на учреждение), гепатита С (0,03% на учреждение) и ВИЧ (0,0004% на учреждение). Хотя риск такого инфицирования сильно снижен благодаря внедрению тестирования до и после сдачи крови, тем не менее, следует помнить, что при каждой процедуре плазмафереза при обмене 3 л плазмы на СЗП 3 л СЗП готовятся из 10-15 единиц плазмы, взятой у такого же количества доноров. Ряд производителей предлагает СЗП, обработанную детергентом.
Таблица 18.5 Выбор замещающей жидкости

Использование СЗП в качестве замещающей жидкости усложняет оценку эффективности плазмафереза для некоторых пациентов (например, при такой оценке нельзя просто опираться на итоговый уровень IgG и других иммуноглобулинов). Также СЗП может привнести с собой ряд факторов, удаляемых в процессе плазмафереза и способных вносить свой вклад в процесс воспаления.
В настоящее время частичное или полное замещение плазмы СЗП при плазмообмене специфически назначается: а) при тромботической тромбоцитопенической пурпуре и гемолитико-уремическом синдроме (ТТП/ГУС); б) при имеющемся дефекте гемостаза и/или при низком уровне фибриногена в плазме до начала лечения (<125 мг/дл); в) пациентам с риском кровотечений - например, тем, кому предстоит хирургическое вмешательство, или тем, кто недавно его перенес.
Что касается ТТП/ГУС, то имеются предпосылки для использования СЗП в качестве единственной замещающей жидкости, поскольку сама инфузия СЗП может иметь терапевтический эффект и поскольку при тромбоцитопении риск кровотечений может быть велик даже при небольших изменениях баланса факторов коагуляции. В связи с тем, что при ПА среди прочего удаляются и факторы коагуляции, как правило, замещение только альбумином в сочетании с кристаллоидными растворами не позволяет восполнить запасы этих факторов и ведет к риску появления кровотечений. Однако такое развитие событий маловероятно после одной-двух процедур плазмообмена - особенно если он производится через день, поскольку период полувыведения большинства факторов коагуляции лежит в диапазоне 24-36 ч.
В. Альбумин. Из-за особенностей применения СЗП, перечисленных выше, мы рекомендуем использовать альбумин в качестве субституата выбора. Выводимая из организма плазма может замещаться эквивалентным объемом кристаллоидного раствора, содержащим 5% альбумина (5 г/дл [50 г/л]) и 130-160 ммоль/л хлорида натрия. Однако поскольку значительная часть альбумина, вводимая в начале процедуры плазмафереза, выводится в результате плазмообмена, более экономичным подходом (при котором объем обмена альбумина эквивалентен объему плазмы, при отсутствии гипоальбуминемии) является замещение первых 20-30% объема выводимой плазмы кристаллоидным раствором, например 0,9% физраствором, с последующим выравниванием баланса упомянутым выше 5% раствором альбумина. В итоге применения данного метода будет получена концентрация альбумина в сосудистом русле на уровне 3,5 г/дл (35 г/л) -достаточная для поддержания онкотического давления крови и для предупреждения гипотензии. Данный подход не должен применяться для пациентов с гипервязкостью крови, с неврологическими заболеваниями, а также для пациентов с эпизодами гипотензии, не связанными с терапией плазмаферезом.
Очищенные растворы для инфузий альбумина сыворотки человека не могут быть источниками вирусных инфекций, поскольку при обработке подвергаются длительному воздействию повышенных температур, поэтому при ТПО предпочитают использовать в качестве замещающей жидкости именно их. Побочные реакции любого рода наблюдаются примерно в одном случае на 6600 инфузий. Тяжелые и потенциально опасные для жизни реакции встречаются примерно в одном случае на 30 000 инфузий. При приготовлении 5% раствора альбумина из более концентрированных растворов в качестве разбавителя следует использовать 0,9% физраствор; применение в качестве разбавителя воды приводило к тяжелой гипонатриемии и гемолизу (Steinmuller, 1998).
Требуемое количество замещающей жидкости зависит от объема излишней жидкости в организме. Количество замещающей жидкости может корректироваться вручную либо автоматически и составлять от 100 до 85% от объема замещаемой плазмы. Использование меньших количеств замещающей жидкости обычно не рекомендуется, поскольку это может уменьшить интраваскулярный объем плазмы и стать причиной гемодинамической нестабильности.
VII. ОСЛОЖНЕНИЯ ПРИ ПЛАЗМООБМЕНЕ. Побочные эффекты при плазмообмене обычно не тяжелые и при выявлении могут быть легко купированы. Основные из них перечислены в табл. 18.6.
Частота проявления осложнений колеблется от 4 до 25%, а средняя частота -10%. Незначительные реакции встречаются примерно при 5% ПА и характеризуются крапивницей, парестезиями, тошнотой, головокружением, а также судорогами ног. Реакции умеренной тяжести (5-10% случаев) включают гипотензию, боль в груди и желудочковую эктопию. Все реакции обычно быстропроходящие и без последствий. Тяжелые побочные эффекты наблюдались менее чем в 3% случаев, и главным образом это были анафилактоидные реакции, связанные с применением СЗП. Ориентировочный уровень смертности, ассоциирующейся с плазмаферезом, - 3-6 случаев на 10 000 процедур. Основными причинами смерти являются: анафилаксия, связанная с применением СЗП, легочная эмболия, а также перфорация сосудов. Наиболее значимые осложнения перечислены в табл. 18.6. Стратегии предотвращения и коррекции осложнений ПА приведены в табл. 18.7.
A. Цитрат. Наиболее частым осложнением терапевтического афереза с применением центрифужной плазмосепарации является интоксикация цитратом, описанная выше, в разделе «Антикоагуляция».
B. Гемодинамические осложнения. Гипотензия (при 2% всех процедур) в основном происходит по причине уменьшения объема плазмы, находящейся в интраваскулярном пространстве, за счет значительного (250-375 мл) перераспределения крови из сосудистого русла в экстракорпоральный контур. В качестве других причин могут выступать вазовагальные реакции, использование гипоонкоти-ческой замещающей жидкости, замедленный или неадекватный плазмообмен, анафилаксия, аритмия и острая сердечно-сосудистая недостаточность.
C. Гематологические осложнения. Геморрагические эпизоды редки. Упоминаются кровотечения после установки бедренного катетера, кровотечения в месте предыдущей установки катетера, гематемезис (кровавая рвота) и эпитаксис (носовое кровотечение).
Таблица 18.6 Осложнения при плазмаферезе

После единичной процедуры плазмообмена уровень фибриногена в плазме обычно падает на 80%, а уровни протромбина и многих других факторов свертывания также уменьшаются на 50-70%. Частичное тромбопластиновое время при этом обычно увеличивается на 100%. Восстановление уровней этих факторов в плазме происходит в два этапа: в первые 4 часа после процедуры плазмафереза оно происходит быстро, а затем медленнее - в течение 4-24 часов. Через сутки после плазмообмена уровень фибриногена достигает значения 50%, а уровень антитромбина III - 85% от их первоначальных значений; для полного восстановления данных уровней требуется от 48 до 72 ч. Через сутки после процедуры содержание протромбина - 75%, а фактора X - 30% от начального уровня; к этому времени уровни всех остальных факторов свертывания возвращаются к нормальным значениям. Когда за короткий период производится несколько процедур плазмафереза подряд, снижение уровней данных факторов еще более выражено и может потребовать нескольких суток спонтанного восстановления. Как уже было сказано, при проведении нескольких процедур с небольшими временными промежутками между ними рекомендуется обмен двух единиц СЗП в конце каждой процедуры. Сообщается также о тромбоцитопении, индуцированной использованием конкретного оборудования для ТПО, что особенно сбивает с толку, когда ТПО применяется для лечения ТТП (Perdue, 2001).
Таблица 18.7 Стратегии предотвращения осложнений при плазмаферезе

D. Ингибиторы ангеотензин-превращающего фермента (АСЕ). Сообщается об анафилактических или атипичных анафилактоидных реакциях у пациентов, принимающих иАПФ во время терапии гемодиализом, при ПА ЛПНП и других видах афереза с применением колонок для селективной плазмофильтрации. Данные реакции связывают с отрицательным зарядом мембран плазмофильтров. Существует экспериментальное подтверждение того, что причиной таких реакций является не только экстракорпоральный контур. Есть мнение, что присутствующий в человеческом альбумине фактор - активатор прекалликреина вызывает эндогенный выброс брадикинина. Тяжесть реакций зависит от различных факторов, включая тип иАПФ и самого альбумина (в котором может быть различное содержание активатора прекалликреина). Поэтому в идеале следует прекратить прием ингибиторов АСЕ с коротким периодом действия за сутки, а пролонгированных иАПФ - за двое суток до плазмообмена с использованием мембран.
E. Инфекции. Истинная частота инфекций при ТПО неизвестна. В исследованиях не выявлено явного повышения числа случаев заражения оппортунистическими инфекциями среди пациентов, получавших иммуносупрессоры вместе с ТПО, по сравнению с теми, кто подвергался только иммуносупрессивной терапии. Однако если в период, непосредственно следующий за плазмообменом, у пациента развивается серьезная инфекция, разумным подходом в данном случае будет разовая инфузия иммуноглобулинов (100-400 мг/кг внутривенно).
F. Выведение электролитов, витаминов и лекарственных препаратов
1. Гипокалиемия. Если в качестве замещающей жидкости используется раствор альбумина, сразу после процедуры плазмафереза будет наблюдаться 25% снижение уровня калия в плазме. Риск гипокалиемии может быть уменьшен добавлением 4 ммоль калия к каждому литру замещающей жидкости.
2. Метаболический алкалоз. Может быть следствием инфузии больших количеств цитрата натрия.
3. Лекарственные препараты. Как правило, при плазмообмене наиболее активно выводятся препараты, имеющие небольшой объем распределения и хорошо связывающиеся с белками крови. Данные клинической практики показывают, что после плазмообмена не требуется дополнительных доз преднизолона, дигоксина, циклоспорина, цефтриаксона, цефтазидима, вальпроевой кислоты и фенобарбитала. Но необходимы дополнительные дозы салицилатов, азатиоприна и тобрамицина. Во многих отчетах, касающихся клиренса фенитоина, содержатся противоречивые данные, поэтому необходим тщательный мониторинг концентраций не связанного с белками препарата. Мы обычно рекомендуем давать все назначенные пациенту препараты сразу после ПА.
VIII. ПОКАЗАНИЯ ДЛЯ ПЛАЗМАФЕРЕЗА. Наиболее подробные рекомендации по использованию терапевтического афереза содержатся в материалах, опубликованных Американским обществом афереза (ASFA). ASFA присваивает заболеваниям категории на основании доказательного подхода и после систематического изучения специализированных публикаций по теме афереза. Более того, классифицируется и качество приводимых доказательств. Категория I включает нарушения, для которых аферез рассматривается в качестве терапии выбора. Категория II обозначает заболевания, для которых аферез применяется в качестве дополнительной терапии (обычно после неудачного применения других методов). К категории III относятся состояния, для которых оптимальная роль терапии аферезом не установлена и требуется принятие индивидуального решения в каждом клиническом случае. Категория IV включает заболевания, при которых применение афереза, согласно имеющимся данным, является неэффективным или вредным. В табл. 18.8 приведен список заболеваний, при которых аферез применяется в качестве терапии первой линии, как изолированно, так и в сочетании с другими терапевтическими модальностями. При этих заболеваниях аферез должен применяться как можно скорее - для достижения оптимальных результатов. Ниже приведены примеры и итоги использования афереза при лечении заболеваний почек.
А. Гломерулонефрит, вызванный антителами к гломерулярной базальной мембране (ГБМ). Существуют подтверждения патогенетической роли антител к ГБМ в развитии данного заболевания, которое, как показывает история, может быстро привести к летальному исходу при отсутствии лечения. Настоятельно рекомендуется раннее начало лечения плазмаферезом, поскольку прогноз улучшается при относительно малых концентрациях креатинина в плазме (<500 мкмоль/л, или 5,7 мг/дл). В самом большом длительном исследовании плазмафереза в сочетании с иммуносупрессорами почти у всех пациентов с уровнем креатинина <500 мкмоль/л (5,7 мг/дл) функция почек была восстановлена - по сравнению с 8% тех пациентов, кто уже был на диализе.
Таблица 18.8 Показания для проведения срочного плазмафереза и цитафереза

У диализных пациентов с олигурией, особенно имеющих большое количество гломерулярных полулуний в биоптате почек, плазмаферез, возможно, целесообразно применять только при легочном кровотечении, поскольку функцию почек вряд ли удастся восстановить. Частота плазмафереза должна быть достаточно высокой для быстрого уменьшения содержания циркулирующих антител к ГБМ. В исследовании, упомянутом выше, пациенты подвергались плазмообмену на уровне 50 мл/кг (примерно Г,5 единицы плазмы) в течение Г4 дней подряд или до достижения неопределяемого уровня антител к ГБМ. Другие авторы рекомендуют обмен двух объемов плазмы ежедневно, в течение 7 дней, с плазмаферезом через день в течение следующей недели. Хотя для подтверждения диагноза рекомендуется проведение биопсии почек, при наличии серьезных клинических подозрений и при положительных результатах соответствующих анализов на антитела к ГБМ лечение должно быть начато незамедлительно. Если биопсия все же необходима, она может быть произведена после первых двух-трех процедур плазмообмена, с последующей отсрочкой плазмафереза на 24 часа. Там, где это возможно, после биопсии почек и при легочном кровотечении предпочтительнее цитратная антикоагуляция. Возможно, потребуется продление терапии плазмаферезом на вторую неделю - в зависимости от клинического ответа на терапию и уровня антител к ГБМ.
Как правило, плазма замещается 5% раствором альбумина, однако рекомендуется использование СЗП в качестве завершающего литра субституата для пациентов после биопсии почек либо легочного кровотечения. Если у пациента наблюдается большой излишек жидкости, количество раствора альбумина может быть снижено до 85% (но не ниже) от удаляемого объема плазмы.
В. ТТП и ГУС. И ТТП, и ГУС приводят к тромботической микроангиопатии (ТМА), которая при ГУС поражает главным образом почки, а при ТТП зачастую поражает ЦНС. ГУС подразделяется на ассоциированный с диареей - (D+) и не связанный с диареей (спорадический или атипичный) - (D-). ГУС-(П-) может ассоциироваться с генетическими дефектами регуляторов активности системы комплемента или с аутоантителами к этим белкам (атипичный ГУС - аГУС). При ТТП может наблюдаться генетически обусловленная недостаточность протеазы ADAMTS13, расщепляющей фактор фон Виллебранда, или присутствие антител к ней. При плазмаферезе замещаются нормальные компоненты плазмы, независимо от их этиологии, включая аутоантитела.
При тяжелой ТТП терапия плазмаферезом должна начинаться как можно скорее. Требуются ежедневные процедуры с обменом, как минимум одного объема плазмы, обычно в течение 7-10 дней. Некоторые специалисты предлагают использование 1,5 объема плазмы в первые три процедуры - для достижения быстрого терапевтического эффекта. Процедуры продолжаются, пока число тромбоцитов не нормализуется, а гемолиз в основном не прекратится (и уровень лактатдегидрогеназы не станет ниже 400 МЕ/л). Поскольку за прекращением терапии плазмаферезом сразу может последовать рецидив проявлений болезни, функциональное состояние сосудистого доступа должно поддерживаться до стабилизации числа тромбоцитов. Для пациентов, у которых число тромбоцитов падает до значений <100 000/мм3, рекомендуется проведение плазмафереза по графику через день - до тех пор, пока число тромбоцитов не стабилизируется. На настоящий момент проведено два контролируемых исследования, демонстрирующих эффективность плазмафереза с применением СЗП по сравнению с простыми инфузиями СЗП, плюс недавний метаанализ контролируемых исследований показал, что плазмаферез с применением СЗП является наиболее эффективным методом лечения ТТП.
ГУС, ассоциированный с диареей (ГУС-(П+)) у детей - зачастую саморегулирующееся состояние, улучшающееся при применении поддерживающей терапии. Рандомизированные исследования плазмафереза не проводились, однако имеются недавние отчеты об успехе применения плазмафереза для взрослых пациентов с тяжелой ГУС-(П+) в острой форме. Также не проводились контролируемые исследования атипичного, (D—), ГУС, однако имеются единичные клинические случаи успешного применении плазмообмена с использованием СЗП при лечении тяжелобольных пациентов. Несмотря на недостаточность данных, пробное назначение плазмафереза при тяжелой ТТП (ТМА) во время беременности может оказаться небезосновательным. Плазмаферез также может быть полезным при других, вторичных причинах ТТП, хотя перфузия плазмы через колонки со стафилококковым протеином A (SPA) оказалась более эффективной для лечения митомицин-индуцированной ТТП. При лечении ГУС-(П-) применяется экулизумаб (моноклональное антитело, связывающееся с белком С5 комплемента человека и подавляющее активацию комплементо-посредованного лизиса клеток) с обнадеживающими результатами. При недавней эпидемии в Европе, ГУС-(1) I) хорошо поддавался лечению как экулизума-бом (Delmas, 2014), так и плазмаферезом.
С. Криоглобулинемия. Плазмаферез используется для лечения криоглобулинемии вот уже 20 лет - благодаря положительному эффекту от выведения больших иммунных комплексов, ответственных за клинические проявления болезни. Хотя контролируемые исследования такого лечения не проводились, существует большое количество отчетов, демонстрирующих эффективность плазмообмена при терапии васкулитов и криоглобулинемии с вовлечением почек. Следует также рассматривать плазмаферез в качестве средства при лечении синдрома гипервязкости крови или если пациенту предстоит операция в условиях гипотермии. В тяжелых случаях применяются также иммуносупрессоры в сочетании с противовирусной терапией для пациентов с гепатитом С.
Как правило, рекомендуется обмен одной единицы плазмы в течение 7 дней и как альтернатива плазмаферез через день в течение 2-3 недель. В качестве замещающей жидкости следует использовать 5% раствор альбумина подогретого - во избежание осаждения циркулирующих криоглобулинов. Для лучшего контроля симптоматики у ряда пациентов требуется проведение процедур один раз в неделю на протяжении продолжительного периода. Часто предпочтительнее использовать установки с центрифугами - из-за вероятности засорения мембран криоглобулинами при их остывании и осаждении. Альтернативные техники, такие как двойная каскадная фильтрация и криофильтрация, являются довольно дорогими и технически сложными, поэтому широко не применяются.
D. Разновидность васкулитов, при которых в крови определяются антинейтрофильные цитоплазматические антитела (АНЦА). АНЦА-ассоциированный васкулит. У пациентов с данным заболеванием наблюдается васкулит мелких сосудов, зачастую поражающий почки, с быстропрогрессирующим малоиммунным гломерулонефритом. Данная группа заболеваний включает гранулематоз с полиангиитом (ранее - гранулематоз Вегенера), микроскопический полиангиит и эозинофильный гранулематоз с полиангиитом (ранее - синдром Чарга-Стросса). Объем данных, подтверждающих патогенетическую роль АНЦА при указанных заболеваниях, растет. Хотя в предыдыдущих исследованиях не было получено однозначных результатов, Pusey (1991) продемонстрировал успех применения плазмообмена в сочетании с иммуносупрессорами для пациентов, которым уже требовался диализ. Большое многоцентровое европейское исследование (МЕРЕХ) подтвердило эти данные и показало, что для пациентов с уровнем креатинина >500 мкмоль/л (5,7 мг/дл) применение плазмафереза привело к лучшему восстановлению функции почек по сравнению с пациентами, получавшими пульс-терапию метилпреднизолоном. Еще одно небольшое недавнее исследование продемонстрировало успех терапии плазмаферезом пациентов с уровнем креатинина >250 мкмоль/л (2,8 мг/дл). Недавний метаанализ подтвердил пользу от дополнительного лечения плазмаферезом по сравнению со стандартной терапией в предотвращении развития терминальной почечной недостаточности.
На базе исследования МЕРЕХ мы рекомендуем ежедневный обмен 1,5 объема плазмы в течение 7 дней. Однако большое международное контролируемое исследование плазмафереза при АНЦА-ассоциированном васкулите у пациентов со скоростью клубочковой фильтрации <50 мл/мин PEXIVAS не показало никаких преимуществ применения ПА в лечении АНЦА-васкулита, и теперь его рекомендуют только при тяжелом поражении легких. Для пациентов после биопсии почек или легочного кровотечения в качестве последнего литра замещающей жидкости следует использовать СЗП. Некоторым пациентам могут потребоваться более длительные периоды лечения, в зависимости от клинического ответа на него.
E. Множественная миелома. Множественная миелома (ММ) может приводить к повреждению почек посредством целого ряда механизмов, самым типичным из которых является сочетание сжД'-нефропатии и болезни легких цепей у больных с множественной миеломой. Хотя с помощью плазмафереза можно легко удалить парапротеины, ответственные за развитие ММ, ранние исследования в данной области продемонстрировали противоречивые результаты. Более позднему, недавнему большому исследованию не удалось показать преимуществ плазмафереза при лечении пациентов с выявленной <жГ-нефропатией, подтвержденной биопсией почек. В ретроспективном исследовании клиники Мейо показана польза плазмафереза для пациентов с выявленной <жГ-нефропатией с высоким уровнем легких цепей и тяжелым повреждением почек.
Как правило, мы рекомендуем режим из пяти последовательных процедур плазмообмена с 5% раствором альбумина для пациентов с острым почечным повреждением, вследствие болезни легких цепей. В зависимости от клинического ответа на терапию и уровня парапротеинов некоторым пациентам может потребоваться более длительное лечение.
Альтернативой плазмаферезу может быть получивший популярность в последние пять лет подход, который основан на эффективном выведении легких цепей в процессе гемодиализа при помощи специальных диализаторов с мембраной, изготовленной по технологии высокой отсечки. В добавление к стандартной химиотерапии, с бортезомибом или без него, проводился интенсивный диализ. В первоначальном исследовании у пациентов с острой почечной недостаточностью вследствие множественной миеломы производился диализ с использованием двух последовательно соединенных диализаторов («Тералайт»39 компании «Гамбро»40) путем ежедневных восьмичасовых процедур в течение первых 5 дней, а затем восьмичасовых процедур через день в течение последующих 12 дней, после чего процедуры производились по 6 часов три раза в неделю. В конце каждой продленной процедуры пациенту давалось по 4 г бессолевого альбумина, магний внутривенно и кальций перорально, если их преддиализные уровни были низкими (Hutchison, 2009). Уровень свободных легких цепей оценивался путем иммуноанализа. Клинический ответ был обнадеживающим - в виде заметного снижения уровня свободных легких цепей в плазме и большого числа пациентов с восстановлением функции почек. Сейчас в Европе готовятся два контролируемых исследования на базе ряда медицинских учреждений (EULITE и MYRE) для изучения данного метода.
F. Системная красная волчанка (СКВ). Плазмаферез широко применяется при лечении СКВ для выведения циркулирующих аутоантител и иммунных комплексов. Е(есмотря на бытующее мнение о положительном эффекте плазмафереза, одно из рандомизированных исследований не выявило преимуществ добавления плазмафереза к иммуносупрессивной терапии для пациентов с волчаночным нефритом, применявшейся на протяжении 3 лет. Правда, в исследовании не участвовали пациенты с серповидным нефритом и те, которым требовался диализ, но вряд ли кратковременная терапия, такая как плазмаферез, смогла бы повлиять на успех лечения таких больных. Международное исследование с применением больших доз циклофосфамида совместно с плазмаферезом было приостановлено из-за большого числа побочных эффектов, поэтому данный подход не может быть рекомендован. Наш опыт и непроверенная информация говорят о том, что плазмаферез должен применяться у пациентов с проявлениями системного волчаночного эритематоза, угрожающими жизни - например, для людей с серповидным нефритом, легочным кровотечением, волчанкой мозга или катастрофическим антифосфолипидным синдромом. Сообщается также о применении иммуносорбции с использованием колонок с протеином А для пациентов с тяжелым течением заболевания, не поддающимся лечению другими методами.
Мы бы рекомендовали первичный курс из семи процедур обмена 1-1,5 объема плазмы с использованием 5% раствора альбумина для пациентов с угрожающим жизни течением заболевания. В качестве завершающего литра замещающей жидкости для пациентов после биопсии почек или легочного кровотечения необходимо использовать СЗП.
G. Рецидивирующий фокально-сегментарный гломерулосклероз (ФСГС). Рецидивирующий ФСГС в трансплантированной почке в ряде случаев, похоже, вызывается циркулирующими факторами проницаемости, повышающими проницаемость клубочков. Применение плазмафереза при ФСГС в собственной почке пациента приводит к различным результатам, возможно, потому, что у кого-то из этих пациентов имеются врожденные генетические дефекты протеинов, участвующих в почечном фильтрационном барьере. ФСГС может рецидивировать вскоре после пересадки почки (в 15-55% случаев), и сообщается об успешном применении плазмафереза для таких пациентов.
В отсутствие адекватной информации на данный счет для пациентов с быстрым рецидивом протеинурии после трансплантации почки мы бы рекомендовали обмен 1 объема плазмы 5% раствором альбумина в течение как минимум 5 дней подряд, и возможно, дольше - в зависимости от клинического ответа на терапию.
H. Пурпура Шенлейна-Геноха и IgA-нефропатия (болезнь Берже). У пациентов с HSP и первичной IgA-нефропатией может быстро прогрессировать гломерулонефрит вследствие серповидного нефрита. Гистологическая картина может быть схожей с таковой при АНЦА-ассоциированном васкулите. Сообщается об успешном применении плазмафереза, обычно в сочетании с иммуносупрессорами, для ряда небольших групп пациентов. Мы также наблюдали улучшение функции почек у некоторых пациентов при применении данного подхода.
Целесообразно проведение семи обменов 1-1,5 объема плазмы на 5% раствор альбумина для пациентов с активным серповидным нефритом и ухудшающейся функцией почек, основываясь на практике лечения АНЦА-ассоцииро-ванного васкулита.
I. Синдром гипервязкости крови. Наиболее часто проявляется при макроглобулине-мии Вальденстрема (50% случаев), иногда при миеломе и криоглобулинемии. Гипервязкость ведет к агрегации эритроцитов и ухудшению системного кровотока, приводящего к ишемии ряда органов и систем, включая ЦНС, сетчатку и почки. Хотя контролируемых исследований не проводилось, имеется ряд сообщений об успешном применении плазмафереза в улучшении клинических симптомов и ожидании эффекта в терапии основного заболевания в целом.
В отсутствие адекватной информации по данному вопросу мы бы рекомендовали обмен 1 объема плазмы 5% раствором альбумина в течение 3-5 дней или до нормализации вязкости крови и стабилизации состояния пациента.
J. Трансплантация почки. Вот уже 20 лет плазмаферез применяется для предотвращения отторжения трансплантированной почки, опосредованного антителами, а с недавнего времени - в качестве составной части протокола десенсибилизации для АВО-несовместимых пациентов или пациентов с повышенной чувствительностью. Показания к плазмаферезу для предотвращения отторжения трансплантата все еще окончательно не сформированы, и в ряде исследований сообщается о положительном эффекте его применения для пациентов с кризом отторжения, вызванном антителами, зачастую с сопутствующей внутривенной терапией иммуноглобулинами (IVIG). Однако плазмаферез не дает выраженного эффекта при хроническом отторжении трансплантата. Для удаления из организма предшествующих антител к HLA применяется как плазмаферез, так и иммуносорбция протеином А у пациентов с повышенной сенсибилизацией, с 70% выживаемостью трансплантата в течение одного года после пересадки.
Также сообщается об эффективности применения плазмафереза при пересадке почки АВО-несовместимым пациентам, часто с использованием дополнительного иммуносупрессора - например, ритуксимаба. При остром отторжении, опосредованном антителами, мы бы рекомендовали обмен 1 объема плазмы 5% раствором альбумина, совместно с терапией IVIG. Плазмаферез в качестве составной части протоколов десенсибилизации для пациентов с высоким риском отторжения трансплантата следует проводить только в специализированных центрах.
К. Отравление и передозировка лекарств. Для таких случаев ASFA не предусматривает назначения плазмафереза в качестве терапии первой линии. Однако сообщается о его применении при отравлении бледной поганкой (Amanita phalloides); для улучшения выведения комплексов дигоксин-РаЬ-фрагментов у пациентов с почечной недостаточностью; при укусах змей; при передозировке цисплатина и для выведения введенных моноклональных антител, когда это требуется (Schutt, 2012).
IX. ПРОЦЕДУРЫ СЕЛЕКТИВНОГО АФЕРЕЗА
A. Обоснование. Несмотря на то что с помощью обычного плазмафереза можно выводить целевые элементы плазмы, такие как содержащиеся в ней иммуноглобулины, криопротеины или липиды, такое выведение неспецифично и требует использования донорской плазмы или альбумина, что требует высоких затрат и может стать причиной побочных реакций. Процедуры селективного афереза разработаны для специфического выведения из плазмы конкретных веществ с возвратом всех остальных ее протеинов, при этом позволяют обходиться без замещающих жидкостей и избегать потери ценных компонентов плазмы.
B. Аферез ЛПНП. В США аферез ЛПНП назначается пациентам с гомозиготной семейной гиперхолестеринемией, а также пациентам с уровнем ЛПНП в крови >300 мг/дл (7,8 ммоль/л) или с уровнем ЛПНП >200 мг/дл (5,2 ммол/л) и подтвержденным атеросклерозом коронарных артерий, несмотря на применение максимальных мер медикаментозной терапии. Как правило, данные процедуры проводятся один раз в неделю или в две недели, в зависимости от уровня ЛПНП, хотя интервалы между процедурами могут быть увеличены, если пациент нормально переносит гиполипидемическую терапию. Аферез ЛПНП должен рассматриваться в качестве пожизненной терапии, поэтому в качестве сосудистого доступа предпочтительно применение периферических внутривенных доступов или артериовенозных фистул, а не туннельных диализных катетеров. Существует множество техник для селективного выведения ЛПВП, применяемых по всему миру. В США FDA одобрила лишь две системы для этой цели: «Липосорбер»41 (Kaneka Corporation, Япония) и H.E.L.P. (гепарин-инду-цированная экстракорпоральная преципитация производства Б. Браун, США). В системе «Липосорбер» кровь проходит через мембранный сепаратор плазмы перед тем, как попасть в две иммуносорбционные колонки LA-15 на основе декстран сульфата в установке МА-03. Декстран сульфат - вещество с отрицательно заряженными молекулами с низкой токсичностью, селективно связывающими положительно заряженные Аро-В-содержащие липопротеины (ЛПНП, ЛПОНП и Lp[а]), с высокой степенью аффинности, выводя их, таким образом, из циркуляции. Для антикоагуляции используется гепарин. Целевой объем обрабатываемой плазмы - 1,5 объема, с уменьшением содержания ЛПНП на 73-83% по итогам одной процедуры.
Отрицательно заряженная поверхность адсорберов провоцирует выброс брадикинина, поэтому пациентам, получающим данную терапию, противопоказаны ингибиторы АПФ, но вместо них можно использовать блокаторы рецепторов ангиотензина. В системе H.E.L.P. цельная кровь проходит через сепаратор плазмы, липопротеины и фибриноген селективно осаждаются буферным раствором гепарина с pH 5,12. Полученный осадок удаляется из плазмы с помощью поликарбонатной мембраны, а гепарин - посредством соответствующего адсорбера, после чего плазме возвращается естественный уровень pH путем бикарбонатного диализа. Данный метод позволяет снижать уровень ЛПНП на 45-67% по итогам одной процедуры. При его применении происходит повышенное выведение компонентов системы комплемента СЗ и С4, плазминогена, фактора VIII и фибриногена. Выведение фибриногена положительно сказывается на гемореологии и используется при лечении внезапной потери слуха -нарушения, характеризующегося заметным повышением уровня фибриногена, агрегацией эритроцитов и повышением вязкости плазмы (хотя данный метод пока не был одобрен FDA). При этих методах, применяемых в США, для антикоагуляции используют гепарин. При применении системы H.E.L.P. прием ингибиторов АПФ не противопоказан.
Существует ряд других техник для селективного выведения ЛПНП. В Европе для лечения гиперлипидемии доступны иммуносорбционные колонки на основе анти-апопротеина ВЮО-антител «Терасорб»42. Из-за их высокой стоимости эти колонки обычно регенерируются и хранятся, что не слишком удобно. Существуют две системы обработки цельной крови, не требующие сепарации плазмы: ДАЛИ43 и версия системы «Липосорбер Д» для цельной крови44. В России есть аппарат для иммуносорбции (колонка «Липопак», НПФ «Покард») для выведения липопротеина(а) как независимого фактора риска атеросклероза коронарных артерий.
С. Иммуносорбционные колонки. В мире производится множество моделей колонок, предназначенных для селективного связывания целевых молекул и их выведения из циркулирующей плазмы (рис. 18.3). Колонки, доступные на настоящий момент, содержат либо SPA - специфический пептид или синтетический антиген, либо иммобилизованные антитела, ковалентно связанные с инертной и нерастворимой матрицей (например, с целлюлозой), заполненью гелевыми гранулами. SPA имеют высокую аффинность к Fc-фрагментам IgGl, IgG2 и IgG4 и выводят из плазмы аутоантитела к IgG или циркулирующие иммунные комплексы, содержащие IgG. Существуют SPA-колонки «Иммуносорба»45 для терапии отторжения почечного трансплантата, опосредованного антителами, дилатационной кардиомиопатии, системной красной волчанки, обыкновенной пузырчатки и антител к фактору VIII. Иммуносорбционные колонки, использующие иммобилизованные антитела, включают колонки на основе анти-апопротеина В («Терасорб»), применяемые для лечения аутоимунных заболеваний, таких как СКВ, миастения, дилатационная кардиомиопатия, и при АВО-несов-местимой трансплантации почки. Кроме того, разработан ряд иммуносорб-ционных колонок, содержащих иммобилизованные антигены или пептиды, предназначенные для связывания специфических циркулирующих антител или молекул. Пример такой колонки - «Гликосорб»46 АВО, которая содержит терминальные фрагменты трисахаридов антигенов групп крови А или В, иммобилизованных на сефарозе, связывающие циркулирующие анти-А и анти-В антитела, и предназначена такая колонка, в частности, для вспомогательной терапии при трансплантации АВО-несовместимых органов.
РИСУНОК 18.3. Иммуноадсорбционная колонка задерживает патогены, связывая их с элементами фильтра (Courtesy of Dobri Kiprov, MD. Reprinted from Linz W, et al. Principles ofApheresis Technology. 5th ed. American Society for Apheresis; 2014. http://www. apheresis.org.)

DFPP, или «каскадной плазмофильтра-цией», называется процесс, при котором используется мембранный сепаратор плазмы, за которым следует фильтр для выведения целевых растворенных веществ, в зависимости от их размера и молекулярной массы. Данные системы применяются для лечения гиперхолестеринемии, криоглобулинемии, мак-роглобулинемии Вальденстрема и нарушений микроциркуляции. Существует целый ряд фильтров с разными размерами пор - для разных молекул. Данный метод гораздо более селективен по отношению к выводимым веществам, чем обычный плазмаферез, однако ценные протеины, такие как IgM, могут задерживаться фильтром, и возможности системы ограничены емкостью фильтра по отношению к продуктам выведения.
E. Криофильтрация. Криоглобулины могут выводиться путем обычного плазмафереза, DFPP или методом, называемым криофильтрацией. В первом случае плазма сепарируется в системе на основе центрифуги или мембраны, пропускается со скоростью 20-30 мл/мин через охлаждающую систему при температуре 4 °C, а затем через криофильтр (Versapor, Pall Medical) для сбора осажденных криопротеинов/криоглобулинов. После этого плазма, освобожденная от крио-глобулинов, нагревается до 37 °C, смешивается с клетками и возвращается пациенту. Другая техника криофильтрации основана на удалении криогеля. Криогель - это осажденный фибриноген, экстра-домен А фибронектин, продукт расщепления фибрина и фибронектина. При данной технике применяется гепаринизация (болюс 2000 ед. с последующей инфузией 1000-2000 ед/ч) - для формирования основы криогеля, вокруг которой собираются другие протеины. Затем криогель отфильтровывается из циркулирующей плазмы.
X. ДРУГИЕ ПРОЦЕДУРЫ АФЕРЕЗА
ЕСР - онлайн способ обработки плазмы, изначально разработанный для лечения Т-клеточной лимфомы кожи (синдрома Сезари). Он также используется для терапии некоторых пациентов с клеточноопосредованными аллоиммунными нарушениями, такими как реакция «трансплантат против хозяина» (ТПХ) и клеточное отторжение трансплантированного сердца или легкого. При данной процедуре используется центрифугирование - для сбора лейкоцитов. Затем к ним добавляется 8-метоксипсорален (8-МОР49), и полученная смесь подвергается дозированному воздействию ультрафиолетового-А излучения (УФ-А), после чего возвращается пациенту. УФ-А излучение активирует 8-МОР, приводя к появлению перекрестных связей ДНК, гибели Т-лимфоцитов и модифицированию дендритных клеток. Считается, что это вызывает клон-специфические изменения в последующем иммунном ответе, включая образование Т-регулирующих лимфоцитов, повышающих иммунологическую толерантность организма. Существуют две такие системы, разработанные компанией «Теракос»50 - UVAR XTS и CELLEX. В качестве антикоагулянта в них используется гепарин; сосудистый доступ, как правило, периферический внутривенный доступ или катетер Вотеке 51. Обычно процедуры проводятся парами, два дня подряд, и повторяются каждые 2 недели (или реже); клиническая картина улучшается постепенно.
XI. ТРАНСПЛАНТАЦИЯ СТВОЛОВЫХ КЛЕТОК И ДРУГИЕ ВИДЫ КЛЕТОЧНОЙ ТЕРАПИИ. Гемопоэтические стволовые клетки (ГСК) собираются у больного методом лейкоцитафереза и используются для лечения неопластических заболеваний кроветворной и лимфатической ткани, в регенеративной медицине и других областях.
ГСК могут быть получены либо напрямую из костного мозга, либо из периферического кровотока. ГСК, доставленные в периферический кровоток, имеют незначительные включения эритроцитов и являются более выраженными предшественниками лимфоцитов и других одноядерных клеток. Обогащенные ГСК популяции клеток способствуют лучшему приживлению трансплантата и иммунной реконституции. Данные преимущества и лучшие показатели заболеваемости и смертности сделали аферез аутологичных ГСК из периферического кровотока наиболее популярным методом получения таких клеток.
Виды клеточной терапии, такие как аутологичные вакцины против рака (например, Provenge, Dendreon, США), и появляющиеся генно-клеточные технологии также используют аферез для получения моноядерных клеток из периферического кровотока.
Ссылки и рекомендуемая литература
Braun N, et al. Immunoadsorption onto protein A induces remission in severe systemiclupus erythematosus. Nephrol Dial Transplant. 2000; 15: 1367-1372.
Cataland SR, Wu HM. Diagnosis and management of complement mediated thrombotic microangiopathies. Blood Rev. 2014;28:67-74.
Clark WF, et al. Plasma exchange when myeloma presents as acute renal failure: a randomized, Controlled trial. Ann Intern Med. 2005; 143: 777-784.
Colic Е, et al. Management of an acute outbreak of diarrhoea-associated haemolyticuraemic syndrome with early plasma exchange in adults from southern Denmark: an observational study. Lancet. 2011; 378: 1089— 1093.
Delmas Y, et al. Outbreak of Escherichia coli O104:H4 haemolytic uraemic syndrome in France: outcome with eculizumab. Nephrol Dial Transplant. 2014; 29: 565-572.
Hattori M, et al. Plasmapheresis as the sole therapy for rapidly progressive Henoch-SchOnlein purpura nephritis in children. Aw J Kidney Dis. 1999; 33: 427-433.
Hutchison CA, et al. Treatment of acute renal failure secondary to multiple myelomawith chemotherapy and extended high cut-off hemodialysis. Clin J Am Soc Nephrol. 2009; 4:745-754.
Hutchison C, Sanders PW. Evolving strategies in the diagnosis, treatment, and monitoring of myeloma kidney. Adv Chronic Kidney Dis. 2012; 19: 279-281.
Kale-Pradhan PB, Woo MH. A review of the effects of plasmapheresis on drug clearance. Pharmacotherapy. 1997; 17: 684-695.
Kiprov DD, et al. Adverse reactions associated with mobile therapeutic apheresis: analysis of 17,940 procedures. J ClinApher. 2001; 16: 130-133.
Kiprov DD, Hofmann J. Plasmapheresis in immunologically mediated olyneuropathies. Ther Apher Dial. 2003; 7: 189-196.
Klemmer PJ, et al. Plasmapheresis therapy for diffuse alveolar hemorrhage in patientswith small-vessel vasculitis. Am J Kidney Dis. 2003; 42: 1149-1154.
Lev)7' JB, et al. Long-term outcome of anti-glomerular basement membrane antibodydisease treated with plasma exchange and immunosuppression. Ани Intern Med. 2001; 134: 1033-1042.
Linz W, et al. Principles of Apheresis Technology. 5th ed. American Society for Apheresis; Vancouver, BC, Canada; 2014. http://www.apheresis.org.
Maggioni S, et al. How to implement immunoadsorption in a polyvalent dialysis unit: a review. J Ren Care. 2014; 40: 164-71.
Matsuzaki M, et al. Outcome of plasma exchange therapy in thrombotic microangiopathy after renal transplantation. Aw J Transplant. 2003; 3: 1289-1294.
McLeod BC, et al. Apheresis: Principles and Practice. 3rd ed. Bethesda, MD: AABB Press; 2010.
Menne J, et al. EHEC-HUS consortium. Validation of treatment strategies for enterohaemorrhagic Escherichia coli O104:H4 induced haemolytic uraemic syndrome: case-control study. Br Med J. 2012; 345: e4565.
Montagnino G, et al. Double recurrence of FSGS after two renal transplants with complete regression after plasmapheresis and ACE inhibitors. Transpl Int. 2000; 13: 166-168.
Perdue JJ, et al. Unintentional platelet removal by plasmapheresis. J Clin Apher. 2001; 16: 55-60.
Pusey CD, et al. Plasma exchange in focal necrotizing glomerulonephritis without anti-GBM antibodies. Kidney Int. 1991;40:757-763.
Saddler JE, et al. Recent advances in thrombotic thrombocytopenic purpura. Hematology. 2004: 407-423.
Sanchez AP, Cunard R, Ward DM. The selective therapeutic apheresis procedures.I ClinApher. 2013; 28:20-29.
Schutt RC, et al. The role of therapeutic plasma exchange in poisonings and ntoxications. Semin Dial. 2012; 25:201-206.
Schwartz J, et al. Guidelines on the use of therapeutic apheresis in clinical racticeevidence-based approach from the Writing Committee of the American Society for Apheresis: the sixth special issue. J Clin Apher. 2013; 28: 145-284.
Siami GA, Siami FS. Current topics on cryofiltration technologies. Ther Apher. 2001; 5: 283-286.
Stegmayr B, et al. Plasma exchange as rescue therapy in multiple organ failure including acute renal failure. Crit Care Med. 2003; 31: 1730-1736.
Steinmuller DR, et al. A dangerous error in the dilution of 25 percent albumin [letter]. V Engl I Med. 1998; 38: 1226-1227.
Strauss RG. Mechanisms of adverse effects during hemapheresis. I Clin Apher. 1996; 11: 160-164.
United States Centers for Disease Control. Renal insufficiency and failure associated with IGIV therapy. Morb Mortal WklyRep. 1999;48:518-521.
Ward DM. Extracorporeal photopheresis: how, when, and why. J ClinApher. 2011; 26 (5): 276-285.
Weinstein R. Prevention of citrate reactions during therapeutic plasma exchange by constant infusion of calcium gluconate with the return fluid. J Clin Apher. 1996; 11: 204-210.
Williams ME, Balogun RA. Therapeutic plasma exchange, principles of separation: indications and therapeutic targets for plasma exchange. Clin I Am Soc Nephrol. 2014; 9: 181-189.
Winters JL. Lipid apheresis, indications, and principles. I ClinApher. 2011; 26: 269-275.
Wolf J, et al. Predictors for success of plasmapheresis on the long-term outcome of renal transplant patients with recurrent FSGS [Abstract]. J Aw Soc Nephrol. 2005; SA-FC026.
Zucchelli P, et al. Controlled plasma exchange trial in acute renal failure due to multiple myeloma. Kidney Int. 1988; 33: 1175-1180.
