- Диализному врачу
- 1. Ведение пациентов с ХБП 4-5-й стадии.
- 2. Подготовка к трансплантации, диализу или к консервативной терапии
- 3. Физиологические принципы и моделирование кинетики мочевины
- 4. Оборудование для гемодиализа и расходные материалы
- 5. Вода для диализа и диализирующий раствор
- 6. Артериовенозные фистулы и протезы. Основные положения
- 7. Центральный венозный катетер в качестве доступа: основы
- 8. Мониторинг артериовенозного доступа и осложнений
- 9. Инфекции и другие осложнения центральных венозных катетеров
- 10. Назначение острого гемодиализа
- 11. Назначение хронического гемодиализа
- 12. Осложнения в ходе процедуры гемодиализа
- 13. Повторное использование диализаторов
- 14. Антикоагуляция
- 15. Продленная заместительная почечная терапия
- 16. Гемодиафильтрация
- 17. Терапевтический аферез
- 18. Актуальность сорбционных технологий сегодня
- 19. Руководство по диализу
Физиологические принципы и моделирование кинетики мочевины
Диализ - это процесс, при котором состав раствора А изменяется в результате экспозиции второму раствору Б через полупроницаемую мембрану. В принципе эту мембрану можно рассматривать как лист, перфорированный отверстиями или порами. Молекулы воды и низкомолекулярных веществ из двух растворов могут перемещаться через мембрану, но более крупные молекулы (такие как белки) не могут проходить через полупроницаемый барьер, и количество растворенных высокомолекулярных веществ с обеих сторон мембраны остается неизменным.
I. МЕХАНИЗМ ТРАНСПОРТА РАСТВОРЕННЫХ ВЕЩЕСТВ. Растворенные вещества могут проходить через мембрану по двум различным механизмам: диффузия и ультрафильтрация (конвекция).
A. Диффузия. Движение растворенных веществ за счет диффузии является результатом беспорядочного движения молекул. Чем больше молекулярный вес вещества, тем ниже будет скорость его транспорта через полупроницаемую мембрану. Небольшие молекулы, движущиеся с высокой скоростью, будут сталкиваться с мембраной чаще, и их диффузионный транспорт через мембрану будет выше. Более крупные молекулы, даже если они могут легко проникать через поры мембраны, будут диффундировать медленнее, поскольку они движутся с меньшей скоростью и сталкиваются с мембраной реже (рис. 3.1).
B. Ультрафильтрация. Вторым механизмом транспорта растворенных веществ через полупроницаемую мембрану является ультрафильтрация (конвекционный транспорт). Молекулы воды исключительно малы и легко проходят через полупроницаемую мембрану. Ультрафильтрация происходит, когда вода перемещается через мембрану под действием гидростатических или осмотических сил (рис. 3.1). Растворенные вещества подхватываются водой и проникают через мембрану (solvent drag). Вода переносит через мембрану растворенные вещества в концентрациях, близких к исходным. Процесс можно сравнить с ветром, подхватывающим листья и пыль, или океанским течением, несущим мелкую и крупную рыбу. Крупные вещества, превышающие размер пор, задерживаются. Для них мембрана служит ситом.
1. Гидростатическая ультрафильтрация.
а) Трансмембранное давление. Во время гемодиализа вода (вместе с низкомолекулярными веществами) движется из крови в диализат в результате гидростатического градиента между секторами крови и диализата. Скорость ультрафильтрации будет зависеть от общей разности давления с двух сторон мембраны (рассчитанной как разница в давлении между сектором крови и сектором диализата).
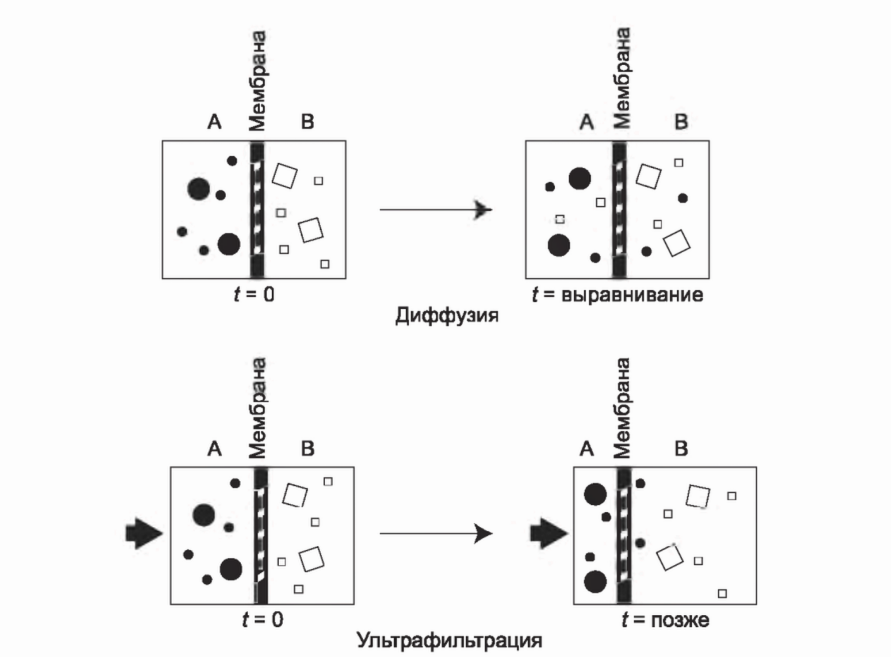
РИСУНОК 3.1. Процесс диффузии (сверху) и ультрафильтрации (снизу). В ходе обоих процессов низкомолекулярные вещества могут проникать через полупроницаемую мембрану, тогда как крупные молекулы задерживаются
B) Коэффициент ультрафильтрации (KUF). Проницаемость мембраны диализатора для воды хоть и высока, но может существенно различаться и зависеть от толщины мембраны и размера пор. Она определяется Кир KUF рассчитывается как число миллилитров жидкости, проходящей через мембрану в течение часа при градиенте давления в 1 мм рт. ст.
2. Осмотическая ультрафильтрация. Осмотическая ультрафильтрация описана в главе 21.
3. Цель ультрафильтрации. Ультрафильтрация в ходе диализа проводится с целью удаления жидкости, накопленной в организме в результате питания и метаболизма поступивших веществ за междиализный промежуток. Как правило, при трехразовом диализе пациент за междиализный промежуток увеличивает вес на 1-4 кг - главным образом за счет воды; ее необходимо удалить в течение 3-4-часового сеанса диализа. Пациентам с острой перегрузкой жидкостью может потребоваться выведение жидкости с большей скоростью. Таким образом, клиническая потребность в ультрафильтрации обычно колеблется от 0,5 до 1,2 л/ч.
4. Использование ультрафильтрации для увеличения выведения растворенных веществ.
а) Гемофильтрация и гемодиафильтрация. В то время как диффузионное удаление веществ зависит от размера молекул, все ультрафильтруемые вещества с размером меньше пор удаляются примерно с одинаковой скоростью. Этот принцип лег в основу техники, названной гемофильтрацией, при которой большие объемы ультрафильтрата (больше чем требуется для удаления жидкости) сопровождаются инфузией замещающей жидкости с целью удаления растворенных веществ. Хотя гемодиализ и ультрафильтрация часто демонстрируют сопоставимое удаление низкомолекулярных веществ, таких как мочевина (МВ 60), гемофильтрация приводит к значительно большему удалению крупных, часто плохо диффундирующих веществ, таких как инулин (МВ 5200). Иногда гемодиализ и гемофильтрация сочетаются. Процедура названа гемодиафильтрацией.
С. Удаление веществ, связанных с белками. В норме почки выводят органические кислоты и основания, связанные с белками. Будучи связаны с белками, они фильтруются только в очень незначительной доле и проходят мимо клубочка (Sirich, 2013). Однако в перитубулярной капиллярной сети эти вещества удаляются с альбумина и переносятся в клетки проксимальных канальцев. Затем они секретируются в просвет канальца, чтобы удалиться с мочой. Другие связанные с белками вещества (с альбумином или с меньшими белками) фильтруются в клубочках вместе с несущими их белками. В проксимальных канальцах профильтрованные белки катаболизируются вместе со связанными с ними веществами.
Плазменные концентрации таких связанных с белками веществ существенно повышены у диализных пациентов (Sirich, 2013), но связь между их высокими концентрациями в крови и летальностью не вполне ясна (Melamed, 2013). Удаление связанных с белками веществ на гемодиализе зависит от процента «свободной» фракции (доступной для диализа). Удаление также зависит от того, насколько быстро «свободная» фракция восполняется из связанного с белками пула. Вещества с низкой «свободной» фракцией, которые плотно связаны с белками, обычным диализом удаляются в незначительной степени.
II. УДАЛЕНИЕ РАСТВОРЕННЫХ ВЕЩЕСТВ: ВЗГЛЯД НА ДИАЛИЗАТОР. На практике емкость, содержащая два раствора (рис. 3.1), становится диализатором, содержащим кровь и диализирующий раствор. Последний состоит из высокоочищенной воды, в которую добавлены натрий, калий, кальций, магний, хлориды, бикарбонат и глюкоза. Низкомолекулярные вещества, которые накапливаются в уремической крови, отсутствуют в диализном растворе. Когда происходит экспозиция уремической крови диализному раствору, поток растворенных токсинов из крови в диализат вначале существенно выше, чем обратный поток из диализата в кровь. В конечном счете, если кровь и диализат остаются в статичном контакте через мембрану, концентрация способных к проникновению токсинов в крови и в диализате сравняется, и дальнейшее удаление токсинов происходить не будет. Перемещение токсинов через мембрану в обе стороны будет продолжаться, но скорость будет равна. На практике во время диализа выравнивание концентраций предотвращают, и концентрационный градиент поддерживается на максимальном значении за счет постоянного замещения диализата свежим диализным раствором и замены диализированной крови на недиализированную. Как правило, направление потока диализирующего раствора и крови противоположно (рис. 3.2). Целью «противотока» является максимизация разницы в концентрациях между кровью и диализатом на всем протяжении диализатора.
А. Доля выведения. Рис. 3.3 схематично показывает диализатор и его эффект на концентрацию мочевины в крови, входящей и покидающей диализатор. Доля выведения представляет собой процент снижения концентрации мочевины или любого другого растворенного вещества при прохождении через диализатор. В представленном примере скорость кровотока (QB) составляет 400 мл/мин, концентрация мочевины на входе 35 ммоль/л, а на выходе - 14 ммоль/л. Следовательно, доля выведения составляет 60% (35 - 14)/35. Доля выведения не зависит от входящей концентрации мочевины. В тех же условиях, если концентрация мочевины на входе составит 70 ммоль/л, то на выходе - 28 ммоль/л. А при входном уровне 3,5 ммоль/л концентрация на выходе составит 1,4 ммоль/л.
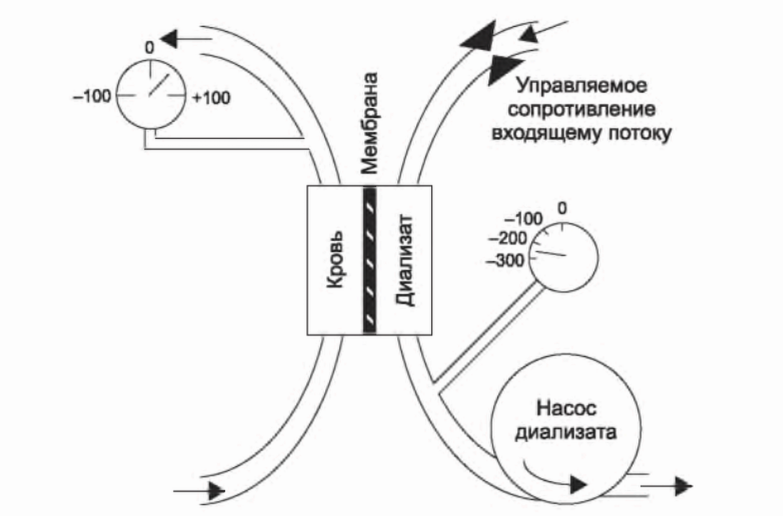
РИСУНОК 3.2. Диализатор с потоками крови и диализирующего раствора, текущими в противоположных направлениях. Гидростатическое давление на мембране (и ультрафильтрация) управляется изменением сопротивления входящему потоку диализирующего раствора
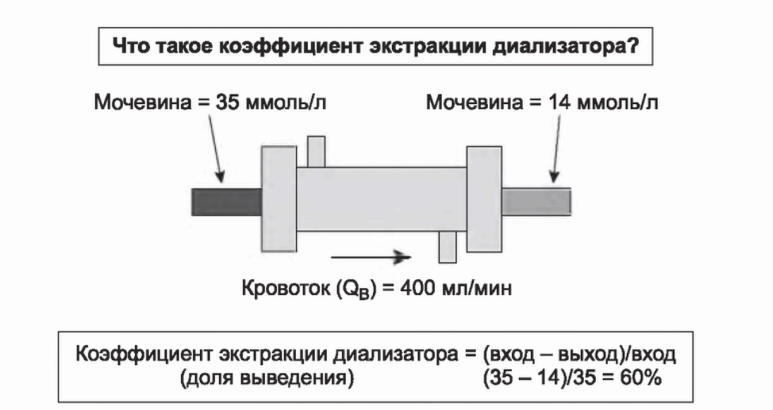
РИСУНОК 3.3. Доля выведения мочевины (коэффициент экстракции) как функция концентрации мочевины на входе и выходе диализатора
Доля выведения зависит от скорости кровотока по диализатору (рис. 3.4). Если снизить скорость кровотока с 400 до 200 мл/мин, то концентрация мочевины на выходе составит не 14, а 4 ммоль/л. Если скорость кровотока снизить до 1 мл/мин, концентрация мочевины на выходе будет очень низкой, примерно 0,01 ммоль/л. А при скорости кровотока в 20 л/мин концентрация мочевины на выходе составит 34,5 ммоль/л. Чем быстрее кровь проходит через диализатор, тем меньше времени она проводит в фильтре. Объем сектора крови в диализаторе примерно 100 мл, соответственно, при кровотоке 400 мл/мин кровь остается в диализаторе 15 секунд. Уменьшение кровотока вдвое удваивает время прохождения крови до 30 секунд, и кровь имеет больше времени, чтобы быть очищенной от мочевины, выходя из диализатора с концентрацией мочевины только 4 ммоль/л. Снижение скорости кровотока до 1 мл в минуту будет увеличивать время прохождения крови до 100 минут, за которые концентрация понизится до ничтожных величин. С другой стороны, при очень большой скорости кровотока (намного больше, чем можно достичь на практике, допустим, 20 000 мл/мин), кровь проведет в диализаторе только 0,3 с. Тем не менее мочевина на выходе будет ниже и составит примерно 34,5 ммоль/л. Фактически диализатор - это стиральная машина, и чем меньше времени проводит кровь в машине, тем от меньшей доли загрязняющих продуктов освободится заданный объем крови.
В. Концепция клиренса. Как показано на рис. 3.5, выходящую из диализатора кровь можно рассматривать двояко. Можно представить ее как единый объем с процентным снижением концентрации растворенного вещества в этом объеме, или как два потока: в первом концентрация вещества будет равной входящей, а во втором вся мочевина будет удалена. Долю выведения можно представить как снижение концентрации на 60% или как величину выходящего «чистого» потока в 60% от входящего. Если мы смешаем оба потока, общая концентрация снизится на 60% от исходной. Таким образом, можно рассчитать, какую долю потока можно оставить неочищенной, чтобы достичь баланса. В данном случае очищенный поток составляет 60% от общего входного потока. Если входной поток равен 400 мл/мин, скорость очищенного потока составляет 0,6 х 400 = 240 мл/мин, а скорость неочищенного потока будет равна 160 мл/мин. Таким образом, доля выведения в 60% транслируется в клиренс диализатора в 0,6 х QB, или 240 мл/мин. В качестве сокращения для клиренса используется К или KD, а для потока Q (QB - для крови, QD - для диализирующего раствора).
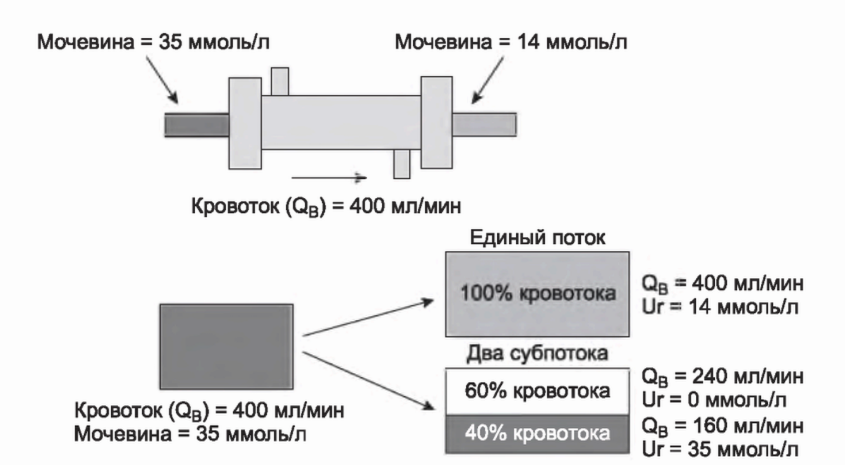
РИСУНОК 3.5. Концепция клиренса диализатора. Кровоток на выходе диализатора можно условно разделить на два потока: вместо единого потока со снижением Ur на 60% представим один поток с неизменным уровнем мочевины, а другой поток - полностью свободным от мочевины. Второй поток представляет собой клиренс диализатора; он равен коэффициенту экстракции диализатора, умноженному на общую скорость кровотока
1. Влияние скорости кровотока по диализатору на клиренс. Рассмотрим теперь влияние скорости кровотока (QB) на клиренс диализатора (KD). Из табл. 3.1 мы видим, что при очень низком кровотоке, 50 мл/мин, кровь в диализаторе очищается очень хорошо вследствие длительного пребывания в нем, и уровень мочевины на выходе составляет только 0,3 ммоль/л с долей выведения в 99%.
Таблица 3.1 Эффект скорости кровотока на долю выведения (коэффициент экстракции диализатора) и клиренс (Ur на входе - 35 ммоль/л)
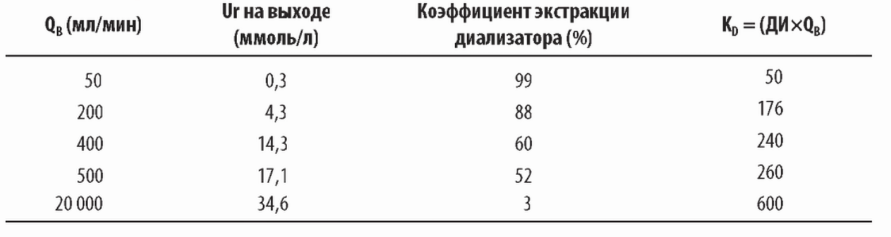
Однако количество очищенной крови будет мало из-за скорости кровотока 50 мл/мин. Хотя кровь очищается на 99%, но 99% от 50 мл/мин - очень небольшая величина. Когда скорость кровотока увеличивается, кровь очищается от мочевины только частично из-за меньшего времени пребывания в диализаторе, но даже при снижении доли выведения объем очищенной крови растет с увеличением скорости кровотока. В конце концов, когда скорость кровотока очень высокая (20 л в минуту), клиренс в этом особом случае составляет 600 мл/мин, хотя только 3% от входящей мочевины удаляется.
2. КД коэффициент массы переноса. Если доля выведения остается постоянной на уровне 60%, удвоение кровотока вдвое увеличивает клиренс. Однако эффективность удаления снижается на очень высоких кровотоках, так что клиренс не возрастает вместе с QB в соотношении 1:1. При очень высоких кровотоках клиренс выходит на плато. Максимальный теоретический клиренс диализатора (для данного вещества) при неограниченно большом кровотоке и потоке диализата обозначается как К0А, единица измерения - мл/мин. Для диализатора в табл. 3.1 К0А близок к 600 мл/мин. К0А имеет также физическую интерпретацию. Это произведение двух величин: Ко, коэффициента проницаемости диализной мембраны для данного вещества, и А - общей эффективной площади поверхности мембраны диализатора. Удвоение площади поверхности примерно удваивает К0А. Два диализатора с одинаковой площадью необязательно имеют равный К0А, поскольку Ко для них может существенно различаться. Увеличить Ко можно, делая мембрану тоньше, увеличивая пористость и оптимизируя ток диализата с помощью специальных волокон или других возможностей.
Рис. 3.6 показывает взаимоотношения между скоростью кровотока на горизонтальной оси и ожидаемым клиренсом диализатора на вертикальной. Каждая изолиния представляет различную эффективность диализатора, которая выражается в К0А. Величина К0А на рис. 3.6 представлена в диапазоне от 300 до 1600 мл/мин. Большинство диализаторов, использующихся в настоящее время у взрослых, имеют величины К0А от 800 до 1600 мл/мин. Графики показывают, что при увеличении кровотока клиренс возрастает, но с тенденцией к ограничению роста. Можно видеть, что при низком QB, примерно 200 мл/мин, диализаторы с К0А в диапазоне 800-1600 мл/мин имеют близкие клиренсы. Это объясняется тем, что при низком кровотоке в каждом из них происходит почти полное удаление мочевины в диализаторе. Преимущество высокоэффективных диализаторов (с высоким К0А) становится заметным при высоких кровотоках. Диализаторы большего размера с более тонкой и эффективной мембраной способны поддерживать высокую долю выведения с увеличением кровотока, максимально увеличивая клиренс диализатора.
3. Расчет скорости удаления растворенного вещества. В ситуации, когда однородный раствор протекает по диализатору, можно рассчитать скорость удаления конкретного вещества (в мг/мин или в ммоль/мин). Например, если уровень мочевины на входе 35 ммоль/л и мы очищаем от мочевины 240 мл крови в минуту, то удаление составит 8,4 ммоль/мин мочевины.
4. Эффект эритроцитов. В концепции клиренса, описанной выше, кровь рассматривается как простой раствор, однако это не так. При гематокрите в 30% кровоток в 400 мл/мин соответствует току плазмы в 280 мл/мин; остальной поток в 120 мл/мин является движением эритроцитов. На входе и выходе из диализатора мы измеряем уровень определенного вещества в плазме. Для мочевины присутствие эритроцитов не изменяет ситуации, поскольку мочевина быстро диффундирует в диализатор и из него. Например, если мочевина плазмы на выходе составляет 14 ммоль/л, ее концентрация в эритроцитах снижается до той же величины. Для креатинина, фосфатов и многих других веществ проблема сложнее, поскольку их концентрация в эритроцитах не выравнивается так же быстро. Действительно, очень небольшое количество креатинина или фосфатов удаляется из эритроцитов за время прохождения крови по диализатору. При расчете удаления креатинина или фосфатов следует использовать скорость тока плазмы вместо скорости кровотока.
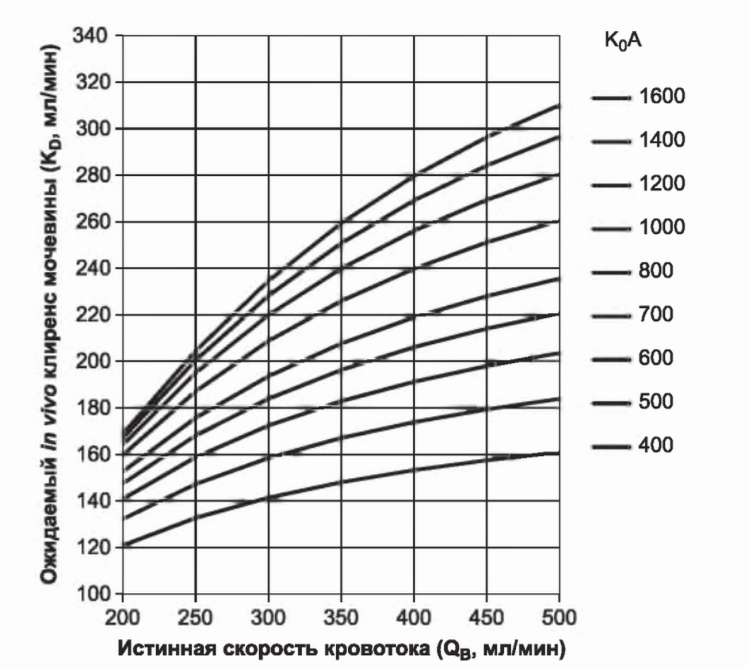
РИСУНОК 3.6. Соотношение между скоростью кровотока (QJ и клиренсом воды крови по мочевине в диализаторе (К) в зависимости от эффективности диализатора (К^А). Каждая кривая представляет разные диализаторы с различным (К0А). Для использования номограммы найдите скорость кровотока на горизонтальной оси, двигайтесь вертикально вверх до пересечения с кривой с соответствующим К.А, затем считайте значение клиренса на вертикальной оси. Теоретические клиренсы скорректированы для лучшего отражения ожидаемой величины клиренса in vivo
5. Эффект воды крови. Как отмечено выше, мочевина растворена в эритроцитах и воде плазмы и удаляется из обоих пространств при прохождении через диализатор. Примерно 93% плазмы является водой (в зависимости от концентрации белков), и вода составляет примерно 72% объема эритроцитов. Некоторая доля мочевины связана с неводной частью эритроцитов. В среднем мочевина растворена в объеме, который составляет 86% объема крови. Коррекция на воду крови становится важной при использовании клиренса диализатора для расчета удаленной мочевины за сеанс.
Для растворов, подобных креатинину и фосфатам, которые удаляются только из сектора плазмы при прохождении через диализатор, доля удаления составляет 93% от тока плазмы. При повышении гематокрита (например, от 20 до 40%), вызывающем только незначительное снижение клиренса воды крови по мочевине, произойдет значимое снижение клиренса креатинина или фосфатов из-за эффекта величины гематокрита на скорость тока плазмы.
6. Эффект скорости потока диализного раствора. Клиренс диализатора по мочевине (и другим веществам) также зависит от скорости потока диализного раствора. Увеличение скорости потока увеличивает эффективность диффузии мочевины из крови в диализат, хотя этот эффект обычно умеренный. Обычно скорость диализного раствора составляет 500 мл/мин. Увеличение потока до 800 мл/мин повысит клиренс мочевины на 5-8% при использовании высокоэффективных диализаторов и при скорости потока больше 350 мл/мин. С другой стороны, в некоторых методиках (ежедневный, ночной диализ, продолжительный диализ в отделениях интенсивной терапии) используется значительно меньший поток диализата. Такое снижение потока может вызвать существенное уменьшение клиренса диализатора. Оптимальный поток диализного раствора превышает скорость кровотока в 1,5-2 раза. Выше этой величины эффект увеличения потока незначительный, особенно в новых диализаторах, где поток диализирующего раствора оптимизирован.
7. Эффект молекулярного веса на диффузионный клиренс. Поскольку вещества более высокой молекулярной массы перемещаются по раствору медленнее, их диффузия через мембрану хуже. Как результат доля выведения для таких молекул будет ниже таковой для мочевины. Кроме того, при расчете клиренсов более низкая доля выведения умножается на скорость тока плазмы, а не на скорость кровотока.
8. Очень крупные молекулы. Очень крупные молекулы, такие как|32-микроглобулин (МВ 11 800), совсем не могут проникать через поры стандартных (низкопоточных) диализных мембран. Таким образом, клиренс этих диализаторов по р2-микроглобулину будет равен нулю. Высокопоточные мембраны имеют поры достаточного размера для прохождения крупных молекул. Кроме того, некоторые мембраны удаляют |32-микроглобулин адсорбцией.
9. Диализатор: эффективность к поток. Когда мы говорим об эффективности диализатора, мы в первую очередь имеем в виду его способность удалять малые вещества. Эффективность диализатора лучше всего описывается Q0A по мочевине. Такая характеристика, как поток диализатора, относится к его способности удалять крупные молекулы, такие как |32-микроглобулин. Не существует общепринятой меры оценки потока диализатора, хотя может быть использована его проницаемость для воды (KUF). Обычно высокопоточные диализаторы имеют проницаемость для воды выше 15-20 мл/ч/ мм рт. ст. Диализатор может быть маленьким, низкоэффективным (Q0A = 400 мл/мин), например, для детей, но быть высокопоточным, или высокоэффективный диализатор (Q0A = 1200 мл/мин) может быть низкопоточным, то есть хорошо удалять мочевину, но не удалять |32-микроглобулин.
III. УДАЛЕНИЕ РАСТВОРЕННЫХ ВЕЩЕСТВ ИЗ ОРГАНИЗМА ПАЦИЕНТА
А. Значение мочевины. Измерение удаления растворенных веществ на диализе фокусируется на мочевине. Мочевина образуется печенью из азота аминокислот с промежуточным образованием аммиака и является главным путем удаления азотистых шлаков из организма. Мочевина - это малая молекула с молекулярным весом 60 Да. Она лишь незначительно токсична. Генерация мочевины пропорциональна разрушению белков и отражается в величине БВА1 - белкового эквивалента выведения мочевины. У стабильных пациентов БВА пропорционально потреблению белков. Используя математическую модель, известную как кинетика мочевины, можно рассчитать как скорость удаления, так и темп продукции мочевины. Удаление мочевины дает нам меру адекватности диализа, а генерация мочевины дает оценку количества потребляемого белка.
B. Недельный профиль мочевины сыворотки крови. В результате сеанса диализа пред-диализный уровень мочевины, как правило, снижается на 70%, таким образом, уровень мочевины после диализа составляет 30% от додиализного. В течение последующего междиализного периода (при трехразовом диализе) мочевина поднимется примерно до того же уровня, что и при первом сеансе. Недельный график мочевины является пилообразным. Средневременной уровень мочевины time-averaged (ТАС) можно рассчитать математически делением площади под кривой на время. Преддиализный уровень мочевины и ТАС - оба отражают баланс между генерацией и удалением мочевины. Для заданного уровня диализа как уровень преддиализной мочевины, так и ТАС будут увеличиваться при росте генерации мочевины (g) и падать, если g будет снижаться. Также для заданного уровня генерации мочевины преддиализный уровень мочевины и ТАС будут расти при снижении интенсивности диализа и снижаться при ее увеличении.
C. Логические ловушки в установлении целевых значений преддиализного и средневременного уровней мочевины (ТАС3 4). Ранние попытки моделирования адекватности диализа фокусировались на преддиализной мочевине и ТАС. Диализ считался адекватным, если эти показатели были низкими. Однако их низкие значения оказались связанными с высокой летальностью; чаще они отражали неадекватное потребление белка, а не адекватный диализ.
D. Показатели удаления мочевины
1. Доля снижения мочевины - ДСМ5. В настоящее время основным критерием адекватности диализа является ДСМ за сеанс. Она рассчитывается следующим образом. Предположим, мочевина до диализа была 21 ммоль/л, а после диализа - 6 ммоль/л. Относительное снижение мочевины составило (21 -6,4)/21 = 14,6/21 = 0,70. По умолчанию ДСМ выражается в процентах, то есть в этом примере составит 70%.
2. Kt/V по мочевине. Показатель Kt/V был популяризирован Gotch и Sargent в повторном анализе National Cooperative Dialysis Study (1985). В этом исследовании величина Kt/V меньше 0,8 была связана с высокой вероятностью морбидности и/или летальности, тогда как Kt/V больше 1,0 ассоциировался с хорошими исходами. Главным образом на основании этого исследования была рекомендована минимальная величина Kt/V в 1,2 для гемодиализных пациентов, получающих лечение три раза в неделю.
Kt/V - это безразмерное отношение, представляющее объем очищенной от мочевины плазмы (Kt), разделенное на объем распределения мочевины (V). К - это клиренс воды крови по мочевине (л/ч), t - длительность сеанса диализа (ч), V - объем распределения мочевины (л), который близок к общему объему воды тела.

Если обеспеченный Kt/V составляет 1,0, то К х 1, или общий объем очищенной крови за сеанс диализа = V - объем распределения мочевины.
3. Как ДСМ соотносится с Kt/V. Чтобы лучше понять это, рассмотрим рисунки от 3.7 до 3.14. На условной модели аквариума (рис. 3.7) мы забираем рыбу из 40-литрового бака, сливаем половину воды - 20 литров и замещаем 20 литрами чистой воды; замещаемый объем воды можно рассматривать как Kt. Объем бака 40 л, таким образом, Kt/V составляет 20/40, или 0,5. Доля снижения уровня загрязнения составит 50% после смешивания 20 литров чистой воды с 20 литрами неочищенной. В этой ситуации Kt/V = доле снижения загрязнения = 0,5.
На рис. 3.8 мы очищаем бак более полно. Достанем рыбу из бака, сольем все 40 литров загрязненной воды и заменим ее чистой водой. Вернем рыбу обратно. В этом случае объем очищения = 40 л, V = 40 л, Kt/V = 40/40 = 1,0. Доля снижения загрязнения составит 100%. В этой модели Kt/V в 1,0 представляет идеальный диализ или очищение, его невозможно улучшить.
Существенно другая ситуация представлена на рис. 3.9. В этом случае очищение происходит без удаления рыбы из бака. Литровой кружкой мы удаляем 1 л грязной воды и замещаем ее 1 л чистой воды. При удалении только небольшого объема из бака мы позволяем рыбе благополучно оставаться в баке во время очищения. Если мы сделаем так 40 раз, то 40 литров раствора будет очищено (40 х 1 л), a Kt будет равно 40. Поскольку V также равно 40,
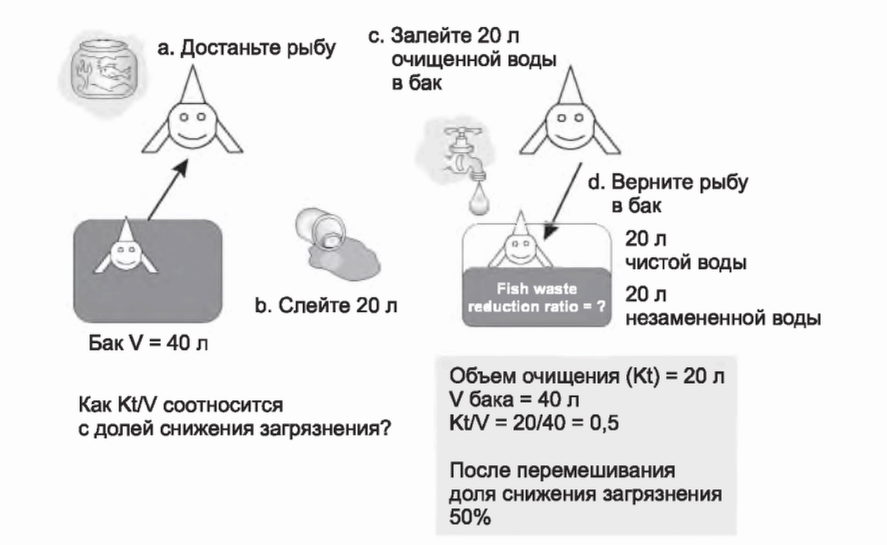
РИСУНОК 3.7. Фракционный клиренс в 50% (Kt/V = 0,5) в модели с рыбой в аквариуме, если удалить рыбу на время очистки. При этом ДСМ равна 0,5 и равна Kt/V
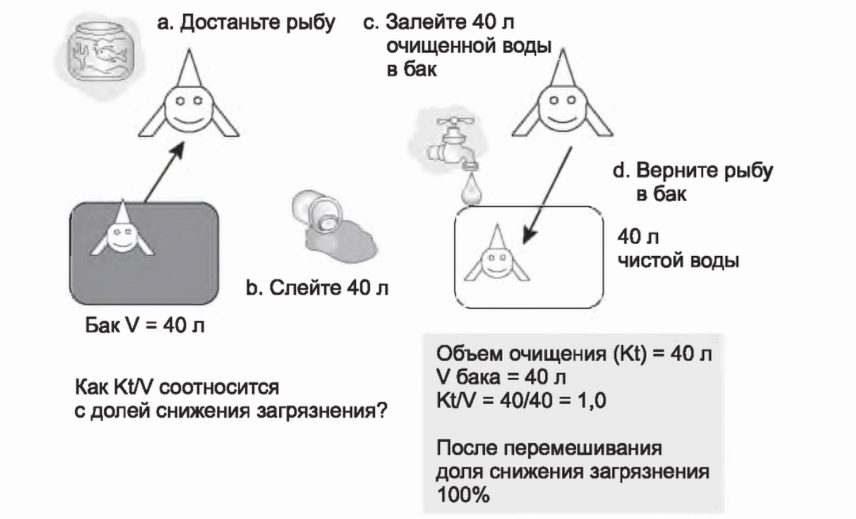
РИСУНОК 3.8. Фракционный клиренс в 100% (Kt/V = 1,0) в модели с рыбой, удаляемой на время очистки. Доля снижения загрязнения -100%, что соответствует Kt/V = 1,0
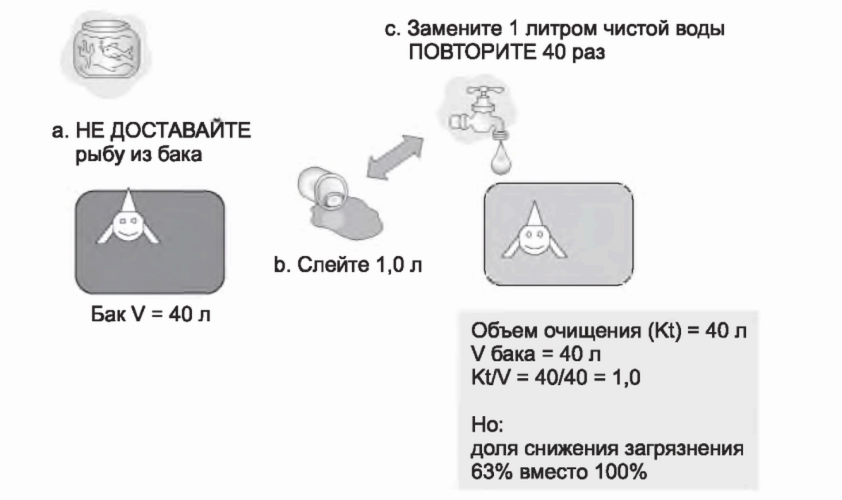
РИСУНОК 3.9. Фракционный клиренс в 100% (Kt/V = 1,0) в модели с рыбой, остающейся в баке на время очистки.
Но в этой ситуации доля снижения загрязнения - только 63% мы вновь получаем Kt/V 40/40 = 1,0. Однако в этой ситуации доля снижения загрязнения составит только 63% вместо 100. Почему? С каждым циклом удаления/восполнения одного литра каждый последующий цикл удаляет меньше продуктов загрязнения, чем предыдущий. Нарастающее разведение продуктов загрязнения в баке в ходе очищения снижает эффективность этого процесса, и теперь Kt/V в 1,0 уже не является идеальным очищением, и значимая доля загрязнения остается в баке после завершения процесса.
Рис. 3.10 и 3.11 демонстрируют это в более строгой форме. На рис. 3.10 мы показали ситуацию, аналогичную рис. 3.7, когда рыба удаляется из бака во время очищения. Здесь мы рассматриваем исходный бак объемом 40 л и идеальный диализатор, такой, что на выходе из него содержание мочевины равно нулю. Начальная концентрация мочевины в баке составляет 35 ммоль/л. На рис. 3.10 процесс очищения непрерывный. Очищенная жидкость собирается в отдельном баке, и концентрация мочевины в ней равна нулю. Если через диализатор пройдет 20 литров, то Kt составит 20, и вернув очищенную жидкость в исходный бак, мы получим ДСМ в 50%. Если через идеальный диализатор пройдет 40 литров, Kt составит 40, и вернув эту полностью очищенную жидкость в исходный бак, мы получим ДСМ в 100%. Нижняя панель рис. 3.10 показывает график взаимоотношений между ДСМ и Kt/V, и в этом случае ДСМ просто равен Kt/V. Средняя панель показывает концентрацию мочевины в жидкости, входящей в диализатор из исходного бака. Уровень мочевины на входе остается постоянным в 35 ммоль/л на протяжении всего сеанса, что делает процесс исключительно эффективным.
На рис. 3.11 показанная ситуация аналогична той, когда рыба остается в баке. В этой ситуации уровень мочевины в жидкости, выходящей из диализатора, остается равной нулю, но выходящая жидкость возвращается в исходный бак. Это приводит к постепенному разведению мочевины в исходном баке, и уровень мочевины на входе в диализатор со временем снижается, что показано на средней панели. Система с постоянным возвратом жидкости в исходный бак значительно менее эффективна, чем когда очищенная жидкость накапливается в отдельном баке до окончания диализа. В этих новых обстоятельствах даже после того как 40 литров раствора пройдет через идеальный диализатор (Kt/V = 1), несмотря на то что уровень мочевины на выходе из диализатора будет оставаться равным нулю, к концу диализа в баке еще останется мочевина. Нижняя панель рис. 3.11 демонстрирует соотношение между ДСМ и Kt/V. Подобно модели с аквариумом при Kt/V 1,0 ДСМ составила 0,63. Даже если мы проведем через диализатор 40 литров второй раз (Kt/V = 2,0) и третий раз (Kt/V = 3,0), уровень мочевины не станет равным нулю и ДСМ не достигнет 100%. Из-за фактора разведения длительные сеансы диализа становятся все менее эффективными в удалении низкомолекулярных веществ по мере продолжения сеанса.
4. Эффект генерации мочевины. На рис. 3.12 мы возвращаемся к модели аквариума. Если удалить 40 л по одному литру 40 раз и сделать это быстро, доля снижения загрязнения составит 63%, как мы обсудили ранее. Однако если очищать бак медленно, рыба будет продолжать генерировать продукты жизнедеятельности. Если «диализ» или очистка бака занимает 2 часа, мы, ожидая долю снижения загрязнения в 63%, вместо этого получим величину 61,5% вследствие дополнительного поступления загрязнения за 2-часовой период очистки. Аналогично, если очистка длится 4 или 8 часов, при Kt/V 1,0 мы получим долю снижения загрязнения только 60 или 57% соответственно. Наконец, если объем в 40 литров будет заменен в течение 24 часов, мы получим модель продолжительной заместительной почечной терапии, где Kt/V в 1,0 за сутки приводит к доле снижения загрязнения, близкой к 0%. Таким образом, хотя ДСМ и Kt/V математически связаны, следует принимать во внимание длительность сеанса диализа.
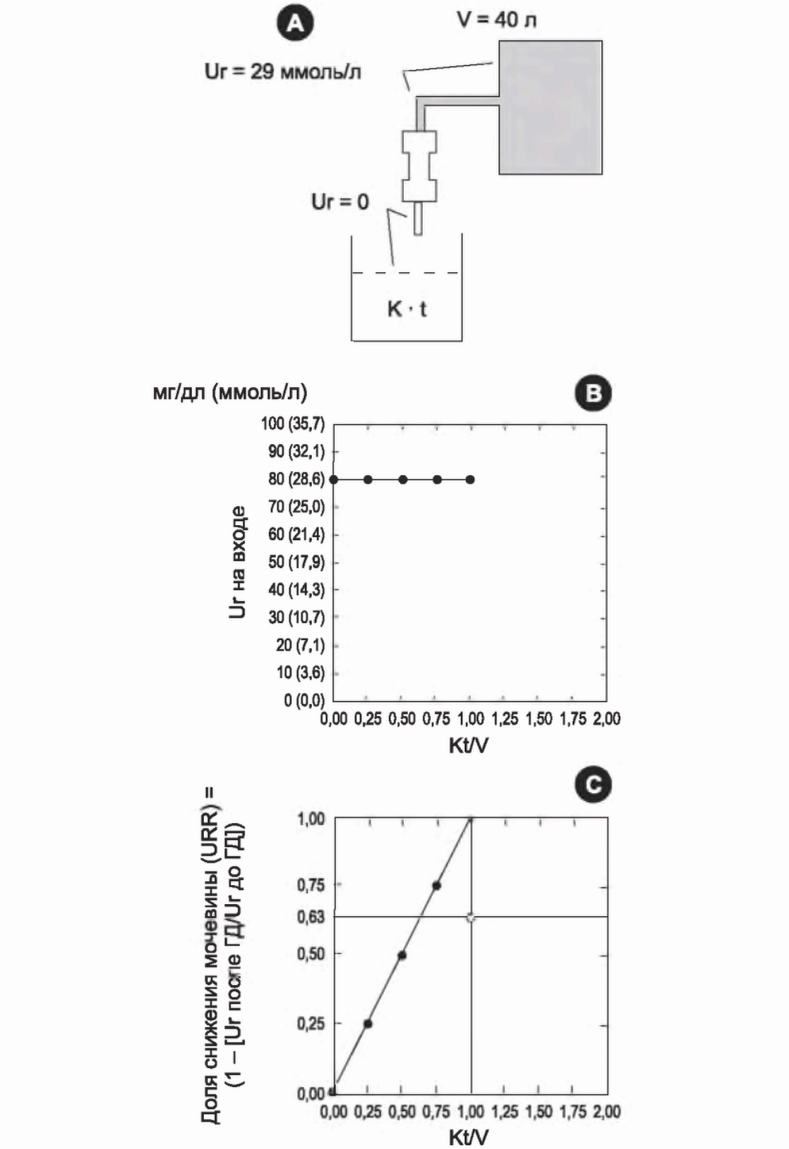
РИСУНОК 3.10. А: Модель удаления мочевины при фиксированном объеме (без генерации мочевины), в которой жидкость из диализатора поступает в исходный бак (тело пациента), но смешивается с его содержимым только в конце диализа. На этой схеме скорость кровотока равна клиренсудиализатора, поскольку мы используем идеальный диализатор. В: Уровень мочевины на входе остается постоянным в течение всего диализа (например, 29 ммоль/л). С: В модели Kt/V = URR и Kt/V = 1,0 представляет идеальный диализ (все токсины удаляются). Воспроизведено из: Daugirdas JT. Urea kinetic modeling tutorial. Hypertens Dial Clin Nephrol. Available at: http://www.hdcn.com
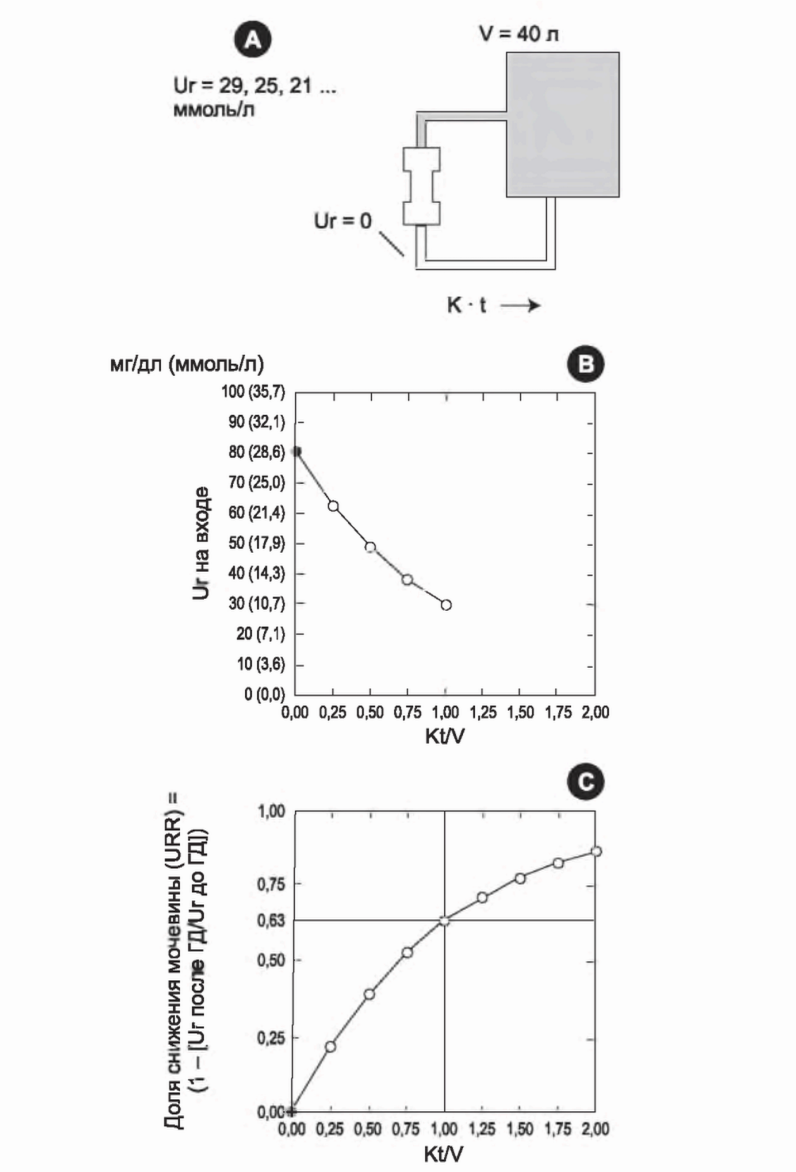
РИСУНОК 3.11. А: Другая модель с фиксированным объемом (без генерации мочевины), но в ней жидкость из диализатора возвращается в исходный бак в течение всего диализа. Как показано в секции В, уровень мочевины на входе экспоненциально снижается, уменьшая эффективность диализатора. С: При непрерывном возвращении оттекающего из диализатора раствора в бак URR достигает только уровня 0,63, когда полный объем бака проходит через диализатор, обеспечивая Kt/V = 1,0. Воспроизведено из: Daugirdas JT. Urea kinetic modeling tutorial. Hypertens Dial Clin Nephrol. Available at: http://www.hdcn.com

РИСУНОК 3.12. Эффект продолжительности сеанса диализа на соотношение Kt/V и URR. В результате продолжающейся продукции загрязнения (например, мочевины) в ходе процесса очищения URR при любом заданном Kt/V уменьшается с увеличением продолжительности сеанса
5. Дополнительный Kt/V, связанный с уменьшением объема. Kt/V обычно рассчитывается по величине V после диализа. В ходе диализа обычно удаляется определенное количество жидкости, так что V после диализа будет на несколько литров ниже стартовой величины. Вместе с уменьшением объема будет удаляться некоторое количество веществ, и это удаление не будет отражаться в изменении концентраций. Чтобы понять это лучше, рассмотрим крайний случай на рис. 3.13. Мы начинаем с бака объемом 80 литров. Просто сливаем 40 литров и не замещаем этот объем. Мы «очистили» (Kt) 40 литров, и объем бака после диализа составляет 40 литров, таким образом, что Kt/V = 40/40 = 1,0. Но доля снижения загрязнения равна нулю. Таким образом, в ходе уменьшения объема мы всегда получаем дополнительный Kt/V, который не отражается в доле снижения загрязнения.
6. Количественная оценка эффекта генерации мочевины и удаления объема. Рис. 3.14 представляет номограммы взаимоотношения между Kt/V и ДСМ, скорректированного на генерацию мочевины и удаления объема. Пунктирная линия на рис. 3.14 соответствует линии на рис. З.ПС. Помним, что Kt/V в 1,0 соответствовал ДСМ в 63%. За 3,5-4-часовой сеанс диализа ДСМ в результате генерации мочевины уменьшается на 0,03, поэтому Kt/V в 1,0, как правило, отражает ДСМ в 60% (а не в 63%). Дополнительные линии справа и ниже первой сплошной кривой отражают отношение ДСМ и Kt/V при удалении определенного количества жидкости. Жирная линия показывает взаимоотношения при удалении жидкости в размере 3% от веса тела, остальные две линии - при удалении 6 и 9% соответственно. Удаление в 3% (2,1 кг у пациента весом 70 кг) можно считать типичным. Мы можем считать ДСМ, соответствующую Kt/V в 1,2, движением вверх от точки 1,2 на горизонтальной оси до жирной линии и затем движением влево по вертикальной оси. Пересечение этой линии с кривой 0,03 соответствует ДСМ 65%. Именно поэтому клинические рекомендации, предлагающие минимум Kt/V в 1,2, также устанавливают минимальную ДСМ в 65% . Однако взаимоотношения между Kt/V и ДСМ не фиксированы строго. При удалении 9% жидкости от веса тела ДСМ в 65% соответствуют Kt/V в 1,4, где дополнительные 0,2 единицы Kt/V получены за счет удаления мочевины, не связанного с изменением концентрации. Аналогично Kt/V в 1,2 при удалении жидкости в 9% от веса тела можно достичь уже при ДСМ всего в 58%. П редставлены такж е уровни Kt/V, соответствующие ДС М в 75% при удалении жидкости в 0, 3, 6 или 9% веса тела соответственно: величины составят 1,5; 1,6; 1,7; 1,8.
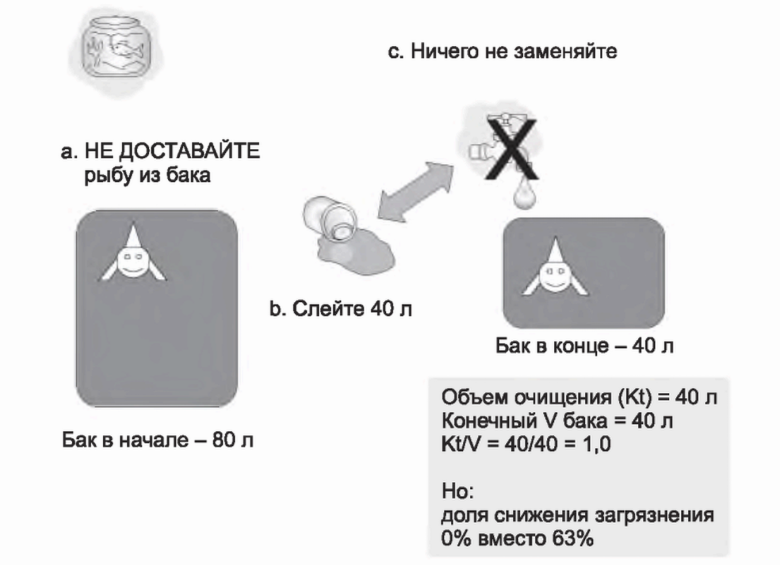
РИСУНОК 3.13. Эффект уменьшения объема на соотношение Kt/V и URR. Мочевина (или загрязнения), удаляемые в процессе сокращения объема, не будут отражаться в URR. Kt/V рассчитан на основе величины V после диализа устанавливают минимальную ДСМ в 65%. Однако взаимоотношения между Kt/V и ДСМ не фиксированы строго. При удалении 9% жидкости от веса тела ДСМ в 65% соответствуют Kt/V в 1,4, где дополнительные 0,2 единицы Kt/V получены за счет удаления мочевины, не связанного с изменением концентрации. Аналогично Kt/V в 1,2 при удалении жидкости в 9% от веса тела можно достичь уже при ДСМ всего в 58%. Представлены также уровни Kt/V, соответствующие ДСМ в 75% при удалении жидкости в 0, 3, 6 или 9% веса тела соответственно: величины составят 1,5; 1,6; 1,7; 1,8.
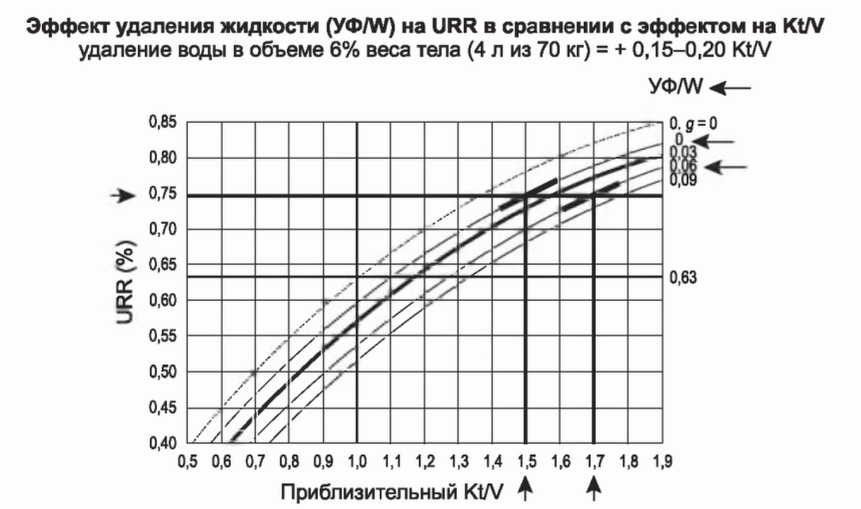
РИСУНОК 3.14. Фактическое соотношение Kt/V и URR, учитывающее генерацию мочевины и эффект сокращения объема. Мы видим в этом случае, что Kt/V в 1,0 соответствует URR 0,60, а не 0,63. Kt/V в 1,0 может достигаться при URR от 0,52 или при средней величине URR в 0,57 (жирная линия на графике, отражающая типичное отношение УФ/W в 3%). URR в 75% может соответствовать Kt/V в 1,5 у пациентов без удаления жидкости или Kt/V в 1,7 у пациентов с удалением жидкости в 6% веса тела. Воспроизведено из: Daugirdas JT. Urea kinetic modeling. Hypertens Dial Clin Nephrol, доступно на: http://www.hdcn.com
Разработаны формулы для преобразования ДСМ в Kt/V коррекцией по продолжительности сеанса (генерация мочевины) и фракционному удалению объема. Одна из них (Daugirdas, 1995) представлена ниже.
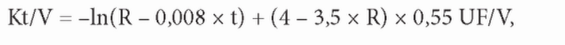
где In - натуральный логарифм, R - отношение постдиализного к преддиа-лизному уровню мочевины, t - продолжительность сеанса (ч), UF - объем удаленной жидкости (л), V - постдиализный объем распределения мочевины (л). Выражение 0,008 х t корректирует отношение мочевины после и до диализа на генерацию мочевины и является функцией длительности сеанса диализа. Величину в 0,008, корректирующую R по генерации мочевины, можно оптимизировать для нестандартных диализных схем или времени забора образцов крови (Daugirdas, 2013). Второй корректирующий фактор учитывает добавочный Kt/V вследствие снижения постдиализного V. Если V неизвестно, можно использовать антропометрическую оценку, примерно 55% от веса после диализа. Тогда выражение упрощается.
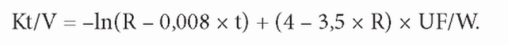
Именно эта формула была использована для генерации кривых на рис. 13.14. Таким образом, ДСМ и Kt/Vматематически связаны, и оба рассчитываются в основном по уровням мочевины до и после диализа. Однако Kt/V принимает также во внимание ультрафильтрацию и генерацию мочевины. Ни одна из этих величин не имеет преимущества перед другой, как предиктор исходов.
7. Многопудовые модели: задержка (inbound) и отскок (rebound) мочевины. Модель, показанная на рис. 3.11, предполагает, что мочевина содержится в едином секторе тела. Это предположение реализуется в моноэкспоненциальном снижении мочевины в ходе как диализа, так и всего диализного цикла (рис. 3.11В) и в отсутствии минимального отскока (rebound) мочевины после диализа. В действительности профиль мочевины отличается от представленного на рис. 3.11В и оказывается ниже ожидаемого (рис. 3.15). Непосредственно после сеанса диализа происходит отскок уровня мочевины, который нельзя объяснить генерацией мочевины. Эти наблюдения предполагают, что мочевина секвестрируется в ходе диализа в каких-то пространствах. Поскольку в начале диализа мочевина удаляется из меньшего кажущегося пространства, ее концентрация падает быстрее, чем ожидается. Мы обозначили это неожиданно быстрое снижение мочевины на ранних стадиях диализа как задержка (inbound). К концу диализа, когда образуется концентрационный градиент между секвестрированными и доступными для диализа пространствами (секторами) тела, падение уровня мочевины замедляется. Когда диализ заканчивается, продолжающееся движение мочевины из секвестрированных пространств вызывает эффект постдиализного отскока (rebound) мочевины (рис. 3.15).
a) Региональные модели кровотока. Секвестрация мочевины в ходе диализа первоначально объяснялась затруднением при перемещении мочевины из клетки. В настоящее время показано, что мочевина секвестрируется в тканях, прежде всего мышечных, которые содержат высокий процент воды, и следовательно мочевины, но получают малый процент сердечного выброса. Из-за низкого отношения кровотока по этим тканям к содержанию мочевины в них перемещение мочевины центральной системой кровообращения из тканей к диализатору оказывается медленным, что вызывает секвестрацию.
b) Влияние задержки (inbound) и отскока (rebound) мочевины на меру адекватности. Количество мочевины, удаляемой за время сеанса диализа, зависит от средневременной концентрации мочевины на входе в диализатор в течение сеанса. При наличии секвестраций средневременная концентрация будет ниже, чем можно было ожидать по уровню мочевины до и после диализа в однопуловой модели. Как результат однопуловая модель завышает оценку выведения мочевины.
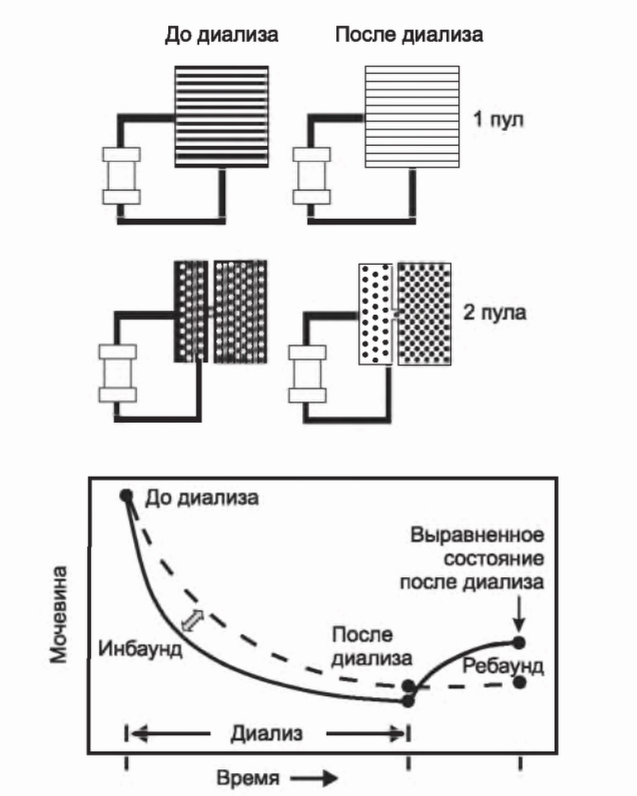
РИСУНОК 3.15. Эффект секвестрации мочевины на ее снижение в ходе диализа (инбаунд) и последиализное возрастание уровня мочевины (ребаунд). При наличии секвестрации мочевина снижается быстрее, чем ожидалось (инбаунд), из-за начального удаления из меньшего кажущегося пространства. Однако после завершения диализа продолжающееся поступление мочевины из секвестрированного пространства вызывает эффект ребаунда (отскока) мочевины. Воспроизведено из: Daugirdas JT. Urea kinetic modeling tutorial. Hypertens Dial Clin Nephrol. Доступно: http://www.hdcn.com
с) Концепция выравненного Kt/V. После диализа мочевина диффундирует из секвестрированных секторов в кровь, вызывая постдиализный отскок, который в основном завершается за 30-60 минут. В это время можно измерить уровень мочевины и рассчитать «истинную», или выравненную ДСМ, которая окажется ниже ДСМ, рассчитанной по образцам крови, полученной непосредственно после сеанса. Выравненную ДСМ можно преобразовать в выравненный Kt/V
Величина отскока мочевины зависит от интенсивности диализа -мощности диализа по отношению к размеру тела. Мощность диализа может быть выражена как Kt/V, обеспеченный за 1 час (Kt/V, деленное на t в часах). На основе моделирования мочевины можно использовать формулу, предложенную Tattersail (1996) для предсказания отскока мочевины исходя из мощности диализа:
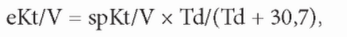
где eKt/V и spKt/V - это выравненный и однопуловый Kt/V, a Td - длительность сеанса в минутах. Временную константу 30,7 мы рекомендуем на основании данных из НЕМО Study (Daugirdas, 2009,2013), она несколько ниже, чем величина в 35 минут, предложенная Tattersall. Используя эту формулу, можно рассчитать eKt/V, соответствующее spKt/V, обеспеченному за 6, 3 или 2 часа.

Как видно из таблицы, eKt/V может быть значительно ниже spKt/V, особенно при коротком диализе. Возможно, по этой причине Европейские рекомендации по наилучшей практике установили минимальный рекомендуемый Kt/V в 1,2 в терминах выравненного, а не однопулового Kt/V
IV. РЕЦИРКУЛЯЦИЯ ПО СОСУДИСТОМУ ДОСТУПУ. Обычно кровоток по артериовенозному доступу составляет около 1 литра в минуту. Насос по крови, который обеспечивает поток крови по диализатору, обычно установлен на скорость потока 350-500 мл/ мин. Поскольку ток крови по доступу обычно не превышает скорости кровотока по контуру, как правило, в контур поступает только кровь из дистальной иглы. Концентрация мочевины в крови, поступающей в диализатор, та же, что и в крови, текущей по доступу вверх, а рециркуляция по доступу отсутствует (предполагая, конечно, что иглы не расположены слишком близко одна от другой, и артериальная и венозная иглы расположены правильно по отношению к направлению кровотока). В фистуле или протезе с прогрессивно ухудшающейся функцией скорость кровотока может значимо снизиться - до величины 350-500 мл/мин и ниже. В этих обстоятельствах часть крови, прошедшей по диализатору, течет в обратном направлении к точке забора крови и вновь попадает в диализатор. При этом кровь на входе в диализатор оказывается «разведенной» кровью, поступившей из диализатора. Этот феномен называется рециркуляцией по доступу.
A. Влияние рециркуляции по доступу на адекватность диализа. При наличии рециркуляции концентрация мочевины в крови, поступающей в диализатор, может быть снижена на 5-40% или более. Количество удаляемой мочевины равно объему прошедшей крови, умноженной на концентрацию мочевины на входе в диализатор. Хотя клиренс диализатора остается неизменным, количество удаляемой мочевины снижается, поскольку снижается концентрация мочевины в крови, поступающей в диализатор. У пациентов с рециркуляцией в конце диализа концентрация мочевины в артериальной магистрали будет ниже, чем в крови, текущей вверх по сосудистому доступу, поскольку кажущийся постдиализный уровень мочевины будет искусственно занижен, ДСМ, и следовательно, spKt/V окажутся завышенными.
B. Избежать влияния рециркуляции на ДСМ и spKt/V можно замедлением кровотока по диализатору или остановкой потока диализата в конце сеанса перед забором крови. Для того чтобы убедиться, что кровь в образце отражает состав крови пациента, необходимо на 20-30 секунд замедлить скорость кровотока по диализатору до уровня, который, безусловно, ниже скорости кровотока по сосудистому доступу (например, до 100 мл/мин). Замедление кровотока по контуру исключит обратный ток крови от выхода из контура ко входу, и теперь вся кровь, поступающая в артериальную иглу, происходит из восходящего потока по фистуле. Необходимая длительность замедления кровотока зависит от мертвого пространства от кончика артериальной иглы до порта забора (обычно 9 мл для большинства магистралей). Период в 20-10 секунд при кровотоке 100 мл/мин будет достаточным, чтобы неразведенная кровь достигла порта забора на большинстве магистралей. Поэтому забор крови всегда должен осуществляться после короткого периода замедления кровотока. Только остановка насоса по крови до забора образца в конце диализа не предотвращает этой проблемы, поскольку разведенная кровь в артериальной магистрали будет просто «заморожена» на месте. Образец крови из артериальной магистрали после остановки насоса по-прежнему будет отражать разведение крови.
Другим рациональным способом избежать этой проблемы является остановка тока диализата на 3 минуты в конце диализа (или перевод диализата в bypass) при продолжающемся кровотоке по контуру. Через 3 минуты уровень мочевины в крови, покидающей диализатор, будет равен таковому на входе в диализатор. Таким образом, теперь уровень мочевины в образце отражает уровень мочевины во всей крови пациента (см. Рекомендации по адекватности диализа 2006 года National Kidney Foundation’s [NKF] Kidney Disease Outcome Quality Initiative [KDOQI]).
V. СЕРДЕЧНО-ЛЕГОЧНАЯ РЕЦИРКУЛЯЦИЯ. Общее определение рециркуляции состоит в том, что кровь, покидающая диализатор, вновь поступает в него, не проходя через периферические ткани с высоким уровнем мочевины. При рециркуляции по доступу она проходит через короткий сегмент доступа между венозной и артериальной иглами. Сердечно-легочная рециркуляция замыкается через сердце и легкие (которые содержат незначительное количество мочевины), когда диализатор снабжается кровью из артериального кровотока (то есть из артериовенозного доступа). Во время диализа очищенная кровь с выхода из диализатора возвращается в сердце. В аорте очищенная кровь разделяется; большая часть из нее направляется в артерии, не связанные с сосудистым доступом, которые ведут эту кровь к тканям, богатым мочевиной. Однако меньшая доля возвращается непосредственно по артериовенозному доступу к диализатору, не пройдя периферическое капиллярное русло. Когда диализатор снабжается кровью из венозного доступа, сердечно-легочной рециркуляции не происходит, хотя градиент концентрации мочевины все еще сохраняется, вся кровь, покидающая диализатор, должна пройти через периферическое капиллярное русло, прежде чем снова вернуться к диализатору.
А. Влияние сердечно-легочной рециркуляции на адекватность диализа. Во время диализа на артериовенозном или венозном доступе устанавливается градиент концентрации мочевины. При артериовенозном доступе концентрация мочевины на входе в диализатор следует кривой, которая на 5-10% ниже кривой при веновенозном доступе. Следовательно, диализ при артериовенозном доступе будет неизбежно менее эффективным (примерно на 5-10%), чем при венозном доступе. Обычно этот эффект компенсируется более высокой скоростью кровотока, достигаемой при артериовенозном доступе, и исключением рециркуляции.
VI. МОДЕЛИРОВАНИЕ ОБЪЕМА РАСПРЕДЕЛЕНИЯ МОЧЕВИНЫ. Моделирование мочевины можно использовать для определения кажущегося объема ее распределения, V. Это выполняется следующим методом. Если удалить некое количество вещества из определенного объема, можно определить размер этого объема, если знать результирующее изменение концентрации. Например, если удаление 50 условных частиц приводит к изменению концентрации на 50%, мы можем сделать вывод, что исходно в объеме было 100 условных частиц. А если исходной концентрацией было, например, 10 частиц/литр, можно рассчитать, что объем составлял 10 литров. Если удаление 50 частиц изменяет концентрацию только на 5%, то исходное их число в объеме составляло 1000. И при начальной концентрации 10 частиц/литр стартовый объем был равен 100 литрам.
Программа моделирования мочевины вначале оценивает, сколько мочевины удалено. Программа рассчитывает клиренс диализатора (исходя из К0А и скоростей тока крови и диализата) и, учитывая длительность сеанса, вычисляет объем очищенной крови (Kt) за весь сеанс. Затем она рассчитывает кривую концентрации мочевины на протяжении всего сеанса по однопуловой или двухпуловой модели (рис. 3.15). На этом основании можно рассчитать среднюю концентрацию мочевины в ходе сеанса. Количество удаленной мочевины тогда равняется произведению клиренса диализатора на время сеанса и среднюю концентрацию мочевины на входе в диализатор. В программу вводятся определенные в лаборатории значения концентрации мочевины до и после сеанса. По этой информации есть возможность рассчитать исходный размер объема распределения мочевины V
В целом мы знаем, что V примерно соответствует 90% от общего объема воды тела. При применении метода к конкретному пациенту следует всегда оценивать рассчитанный объем, чтобы исключить логические ошибки. Мы знаем, что общий объем воды тела составляет 50-60% от веса тела. Можно также рассчитать объем антропометрически (см. Приложение В - Watson или Hume Weyers). Полученный при моделировании объем не должен отличаться от антропометрического более чем на 25%.
Надежнее использовать моделирование при наблюдении в динамике. Хотя величины V существенно варьируют от сеанса к сеансу, большие изменения могут указывать на ошибки в технике забора крови, на незафиксированные изменения в обеспеченной дозе диализа (Kt) или наличие рециркуляции по доступу.
A. V намного меньше обычного. В этом случае ДСМ и Kt/V выше ожидаемого. Поскольку программа исходит из того, что К и t не меняются, высокий Kt/V побуждает программу сделать заключение о том, что V у пациента резко сократился. Если V резко снизился, вероятно, образец крови был взят из венозной магистрали вместо артериальной.
B. V намного выше обычного. В этом сценарии ДСМ и Kt/V ниже ожидаемого. Программа сделает заключение (при неизменных К и t), что объем распределения мочевины увеличился, чтобы привести к такому снижению Kt/V. Реальной проблемой, по-видимому, является уменьшение К или t ниже зафиксированного. Наиболее частой проблемой является перерыв в диализе (полное диализное время не обеспечено), снижение скорости кровотока из-за технических проблем (К ниже ожидаемого), или неправильное указание клиренса диализатора. Рециркуляция по доступу также может вызвать кажущееся увеличение объема, поскольку эффективный клиренс снижается из-за разведения крови на входе в диализатор. Предостережение. Влияние рециркуляции на объем будет заметно, только если образец крови взят правильно (то есть после периода замедления кровотока). Если кровь в образце после диализа разведена кровью, поступившей из диализатора, ДСМ будет искусственно завышена. Ожидаемого снижения ДСМ в результате рециркуляции по доступу при этом не произойдет, и смоделированный V не изменится.
VII. СКОРОСТЬ ГЕНЕРАЦИИ МОЧЕВИНЫ (д) И стБВА. Одним из преимуществ использования моделирования мочевины является возможность расчета скорости генерации мочевины (g) и стБВА. Схема расчета представлена на рис. 3.16. Из значений уровня мочевины до и после сеанса и другой информации касательно сеанса диализа производится начальная оценка объема распределения мочевины у пациента. Затем программа вводит различные предполагаемые значения скорости генерации мочевины и создает недельные графики уровня мочевины с учетом этих допущений. Большая величина g даст более высокие пилообразные графики. Затем программа находит наилучшее соответствие кривой фактически измеренным преддиализ-ным уровням мочевины. Уровни g и стБВА для конкретного пациента определяются исходя из выбранной кривой.
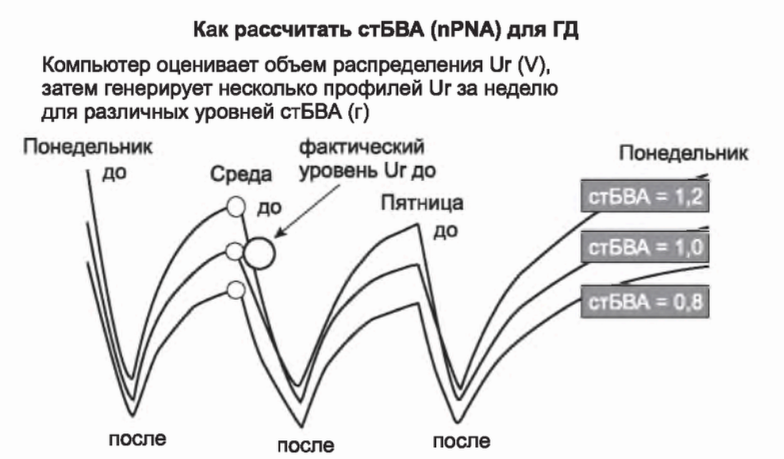
РИСУНОК 3.16. Как программа кинетического моделирования определяет БВА? По до- и последиализным уровням мочевины, длительности сеанса, уменьшению объема распределения и по клиренсу диализатора рассчитывается V для данного пациента. Затем для разных скоростей генерации мочевины (тесно связанных с БВА) создаются пилообразные графики уровней мочевины. За уровень БВА принимается величина, для которой сгенерирована кривая, пик которой в день проведения моделирования совпадает с фактическим уровнем мочевины, полученным лабораторно
Ценность клинического применения g и стБВА иногда ставится под сомнение. стБВА не является надежным предиктором летальности (при коррекции данных на уровень альбумина и креатинина). Как правило, худшие исходы наблюдаются при низком стБВА, поскольку этот показатель отражает низкое потребление белков. Прежде чем сделать вывод о том, что низкий стБВА отражает низкое количество белка в диете, следует убедиться, что в достаточной степени учтены возможные источники потери мочевины, в частности, остаточная функция почек. В редких случаях низкий стБВА будет наблюдаться у быстро улучшающегося клинически пациента, у которого большая часть потребляемого белка уходит на анаболические процессы. В этих счастливых, но редких обстоятельствах мочевина идет на построение белка, а не «выводится» из крови. Высокий стБВА не всегда хороший показатель, поскольку он может отражать разрушение ткани (то есть гиперкатаболизм).
VIII. ОСТАТОЧНАЯ ФУНКЦИЯ ПОЧЕК. Остаточная функция почек обеспечивает значительное улучшение выживаемости пациентов на диализе, а ее значение у пациентов на перитонеальном диализе представляется выше, чем значение перитонеального клиренса.
У пациентов на диализе остаточная функция почек может быть примерно рассчитана как средняя величина между почечными клиренсами по креатинину и мочевине. Клиренс мочевины занижает скорость клубочковой фильтрации вследствие частичной канальцевой реабсорбции мочевины, тогда как клиренс креатинина завышает ее оценку за счет канальцевой секреции. Хорошо установлено, что при наличии остаточной функции почек пациенты с тХПН живут дольше, поэтому важны попытки сохранить остаточную функцию почек и минимизировать возможные негативные эффекты (в частности, избегая нефротоксичных препаратов и минимизируя эпизоды интрадиализной гипотонии).
А. Измерение почечного клиренса по мочевине (Ktu). Для этого необходимо собрать всю мочу за 24-часовой период в междиализный интервал. Обычно пациент собирает мочу за сутки до прихода на сеанс диализа, доставляет контейнер с мочой и сдает образец крови на мочевину. Если пациент получает обычный режим диализа (три раза в неделю) и собирает мочу непосредственно перед диализом, можно предположить, что средняя концентрация мочевины за период сбора составит 86% (для второго сеанса диализа) или 90% (для первого сеанса диализа в неделю) от преддиализного уровня мочевины (Daugirdas, неопубликованные наблюдения). Тогда

Единицы измерения мочевины в крови и в моче не имеют значения, если они одинаковы, поскольку сокращаются. Обычно Кгц составляет 0-8 мл/мин.
Задача. Если диурез составляет 0,33 мл/мин, или 20 мл/ч, за 24 часа пациент соберет 480 мл мочи. Предположим, что уровень мочевины в моче составил 285 ммоль/л (800 мг/дл), что моча собиралась за 24 часа перед первым сеансом в неделю. Преддиализный уровень мочевины в крови составил 20 ммоль/л (56 мг/дл). Рассчитать Кгц.
Решение в единицах СИ. Во-первых, рассчитаем среднюю концентрацию мочевины в крови за 24-часовой интервал. Как обсуждалось ранее, она составляет 90% от уровня мочевины перед диализом, или 0,9 х 20 = 18 ммоль/л. Тогда Кгц = (0,285 ммоль/мл х 0,33 мл/мин)/0,018 ммоль/мл = 5,3 мл/мин.
IX. СТАНДАРТНЫЙ KT/V ПО МОЧЕВИНЕ. Так называемый стандартный Kt/V родился из двух потребностей: 1) получить оценку диализной дозы, не зависимую от числа сеансов в неделю, и 2) определить минимальную дозу гемодиализа, соответствующую минимальной дозе перитонеального диализа.
А. Эквивалентный клиренс мочевины (EKRU) по Casino и Lopez. Рассчитать эквивалентный клиренс мочевины для любого заданного режима диализа можно, используя те же принципы, которые заложены в расчет клиренса креатинина. Креатинин при известной скорости генерации мочевины в минуту (рассчитанной по 24-часовому сбору мочи) и средней концентрации в крови можно рассчитать по отношению:
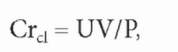
где Crd это клиренс креатинина, UV - диурез, умноженный на концентрацию креатинина в моче, а Р - средняя концентрация креатинина в крови за период сбора. Из сбора мочи за известный период времени можно определить скорость генерации креатинина. И если мы знаем концентрацию креатинина в плазме за период сбора, можно рассчитать, сколько плазмы очищается при удалении генерируемого количества мочевины для поддержания стабильной концентрации.
Эти расчеты были адаптированы для гемодиализа и удаления мочевины Casino Lopez (1996). Как обсуждалось ранее и показано на рис. 3.16, программы моделирования мочевины могут определить величину генерации мочевины для любой диализной схемы в предположении стабильного состояния пациента. Те же программы моделирования могут рассчитать средневременные концентрации мочевины (ТАС) за неделю. При известных g и ТАС эквивалентный клиренс мочевины (EKRU) можно рассчитать для любого диализного режима по аналогии с клиренсом креатинина.
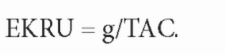
Если рассчитать EKRU для трехразового режима диализа с spKt/V в 1,2, мы получим величину EKRU около 11 мл/мин. Теоретически для любого режима диализа можно рассчитать g и ТАС, используя программы моделирования и затем конвертировать их в EKRU в мл/мин. Эту величину теоретически можно добавлять к измеренному остаточному клиренсу почек по мочевине. Результат можно представить в мл/мин или в л/неделю. В последнем случае EKRU может рассматриваться как величина К х t - объем плазмы, очищаемой в течение недели; при стандартизации на объем V можно рассчитать недельный эквивалент Kt/V по мочевине.
Задача. У пациента V - 35 литров, EKRU - 11 мл/мин. Рассчитать эквивалентный недельный Kt/V по мочевине.
Решение. 11 мл/мин х 10 080 минут в неделю, деленное на 1000 для конвертации миллилитров в литры, дает недельный объем очищенной плазмы ПО литров. Это соответствует выражению К х I. Делением на V = 35 литров мы получаем Kt/V по мочевине 3,14.
В. Стандартный Kt/V по мочевине. Одной из проблем с параметром EKRU было то обстоятельство, что минимальный spKt/V при трехразовом диализе соответствовал недельному эквивалентному Kt/V в 3,14, что было существенно выше, чем недельный Kt/V по мочевине у пациентов на перитонеальном диализе (2,0). Для разрешения этой проблемы Keshaviah и позже Gotch предложили гипотезу пиковых концентраций. Они предположили, что различием между ПД и ГД является наличие пиков для мочевины и других уремических токсинов. Они также обратили внимание, что при трехразовом режиме диализа среднепиковая концентрация мочевины была на треть выше средневременной концентрации. Соответственно, они предложили делить величину g на среднее значение уровня мочевины перед диализом, а не на средневременной уровень (рис. 3.17). Деление на более высокую величину приводит к более низкой мере диализной адекватности примерно на одну треть. Для стандартного трехразового диализа с spKt/V в 1,2 новое значение эквивалентного недельного клиренса составило 7 мл/мин против 11 мл/мин для EKRU, и недельный эквивалент Kt/V в новой мере, обозначенной Gotch как стандартный Kt/V, составил 2,0, что соответствовало таковому для перитонеального диализа.
1. Секвестрированные растворенные вещества и стандартный Kt/V. Как отмечено Depner, стандартный Kt/V можно использовать для моделирования веществ, отличных от мочевины. Растворенные вещества, характеризующие стандартный Kt/V, должны легко удаляться диализом, но могут быть высоко секвестрированы с высоким отскоком после мочевины. Средний преддиализный уровень таких высокосеквестрированных растворов был бы схожим со средневременной величиной. Удаление таких веществ значимо улучшалось бы при увеличении частоты диализа. Если рассмотреть соотношение между стандартным Kt/V и частотой диализа (рис. 3.18), станет ясным, что достичь значения 3,0 можно только с частотой диализа выше трех раз в неделю.
2. Расчет диализного стандартного Kt/V в клинической практике. Расчет можно выполнить, используя программы кинетического моделирования мочевины. Открытая версия программы доступна на сайте http://ureakinetics.org
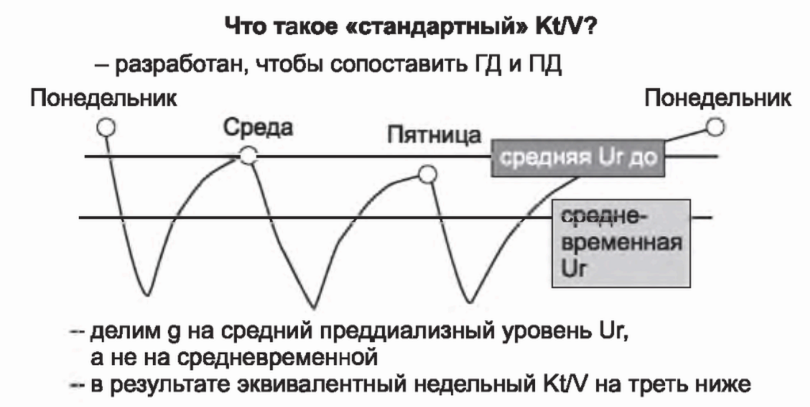
РИСУНОК 3.17. Рассчет стандартного Kt/V. Скорость генерации Ur рассчитывается вместе со стБВА (см. рис. 3.16), после чего эта величина делится на средний преддиализный уровень Ur
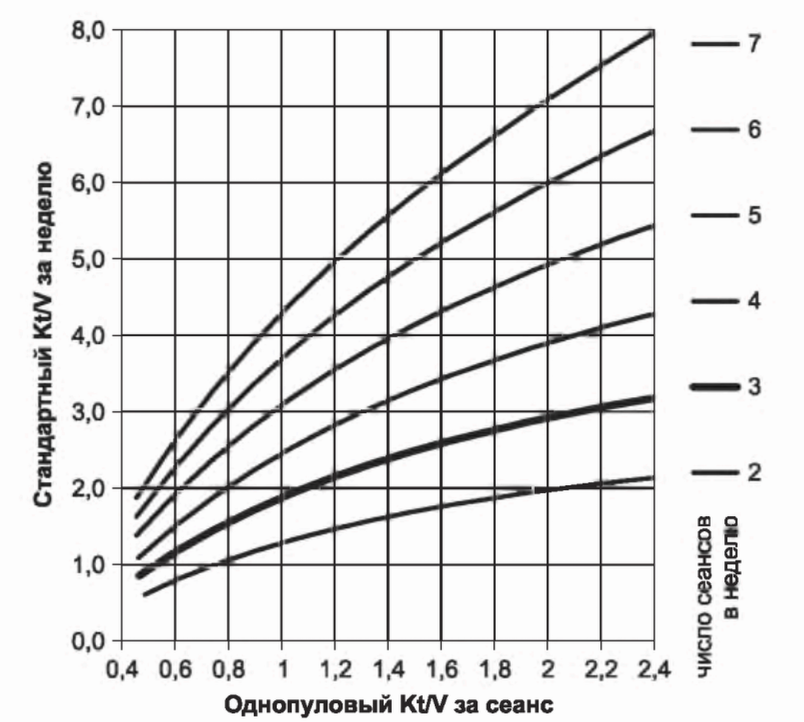
РИСУНОК 3.18. Стандартный Kt/V как функция однопулового Kt/V и числа сеансов в неделю. Смоделированный стандартный Kt/V для клиренса диализатора 220 мл/мин у пациента с V = 40 л. Показано, что трудно достичь стандартного Kt/V выше 3,0 при трехразовом режиме диализа. Диапазон продолжительности диализа - от 30 до 450 минут
(Daugirdas, 2009). Диализный стандартный Kt/V можно также рассчитать, используя упрощенную формулу, разработанную в исследовании FHN (Daugirdas, 2010) - см. Приложение С.
3. Добавление остаточного почечного клиренса по мочевине к стандартному Kt/V. Прямое добавление остаточного клиренса по мочевине к стандартному Kt/V проблематично, поскольку он является искусственной конструкцией. Некоторые исследователи делают это, другие - нет. Следует рассчитать диализный компонент стандартного Kt/V, выразив его в мл/мин, умножая его на V и деля на число минут в неделе. Затем можно прибавить остаточный почечный клиренс по мочевине, после чего конвертировать значение обратно в недельную величину (Daugirdas, 2010).
С. Вопросы, связанные со стандартизацией по V. Стандартизация Kt по V общепринята и осмысленна, поскольку мочевина распределена в общем объеме воды тела и ее генерация пропорциональна V. Однако, поскольку V представляет главным образом мышечные массы, не вполне ясно, нуждается ли пациент с большей на 10% мышечной массой в большем на 10% объеме диализа. Измерение дозы диализа в Kt/V может привести к низким дозам у пациентов небольшого размера, включая женщин и детей (Daugirdas, 2014). Альтернативным подходом является стандартизация К х t по площади поверхности тела. Это даст несколько больше диализа небольшим пациентам, женщинам и детям и относительно меньше диализа - крупным пациентам. Некоторые наблюдательные данные поддерживают использование такого подхода (Lowrie, 2005). Этот способ подсчета детально анализируется в недавнем обзоре (Daugirdas, 2014) - см. Приложение С.
X. АППАРАТНЫЕ МЕТОДЫ ОЦЕНКИ АДЕКВАТНОСТИ ГЕМОДИАЛИЗА
A. Оценка клиренса диализатора путем импульсного изменения уровня натрия в диализирующем растворе с анализом изменения кондуктивности диализата. Измерение адекватности по клиренсу мочевины затратно по времени, требует использования расходных материалов, существенных усилий по обработке и анализу образцов крови, подвергает персонал и пациентов контакту с кровью. Альтернативным подходом является измерение клиренса диализатора онлайн при помощи ступенчатого повышения уровня натрия в диализирующем растворе и последующего измерения кондуктивности диализата на входе и выходе в течение короткого периода времени. Было разрешено несколько технических аспектов, и измеренный на основе кондуктивности клиренс диализаторов хорошо отражает клиренс диализатора по мочевине in vivo. Преимуществом метода является возможность многократно измерять клиренс в течение сеанса диализа. Недостатком является то обстоятельство, что измерение клиренсов диализатора не отражает того, что происходит с пациентом в ходе диализа. Детальное обсуждение см. Gotch (2004) и McIntyre (2003).
B. Поглощение ультрафиолетового излучения в диализате. Другим подходом к аппаратному измерению адекватности диализа является мониторирование поглощения ультрафиолета отработанным диализатом. Поглощение ультрафиолетового излучения на избранных длинах волн соответствует концентрации в диализате мочевой кислоты и других низкомолекулярных веществ. Анализ кривой поглощения ультрафиолетового излучения отработанным диализатом отражает то, что происходит в крови, и отношение поглощения в начале и в конце сеанса диализа отражает соотношение преддиализных и постдиализных уровней мочевины. По этим данным расчет Kt/V может выполняться по ходу сеанса диализа, и эта информация отражает то, что происходит с пациентом (Uhlin, 2006).
Ссылки и рекомендуемая литература
Casino FG, Lopez Т. The equivalent renal urea clearance. A new parameter to assess dialysis dose. Nephrol Dial Transplant. 1996; 11: 1574-1581.
Daugirdas JT. Simplified equations for monitoring Kt/V, PCRn, eKt/V, and ePCRn. Adv Ren Replace Ther. 1995; 2:295-304.
Daugirdas JT. Dialysis dosing for chronic hemodialysis: beyond Kt/V. Semin Dial. 2014; Th 98-107.
Daugirdas JT, Schneditz D. Overestimation of hemodialysis dose depends on dialysis efficiency by regional blood flow but not by conventional two pool urea kinetic analysis. ASAIO J. 1995; 41: M719-M724.
Daugirdas JT, et al; for the Hemodialysis Study Group. Factors that affect postdialysis rebound in serum urea concentration, including the rate of dialysis: results from the HEMO Study. J Am Soc Nephrol. 2004; 15: 194-203.
Daugirdas JT, et al. Solute-solver: a Web-based tool for modeling urea kinetics for a broad range of hemodialysis schedules in multiple patients. Aw J Kidney Dis. 2009; 54:798-809.
Daugirdas JT, et al; Frequent Hemodialysis Network Trial Group. Standard Kt/V urea: a method of calculation that includes effects of fluid removal and residual kidney clearance. Kidney Int. 2010; 77: 637-644.
Daugirdas JT, et al; FHN Trial Group. Improved equation for estimating single-pool Kt/V at higher dialysis frequencies. Nephrol Dial Transplant. 2013; 28: 2156-2160.
Depner TA, Daugirdas JT. Equations for normalized protein catabolic rate based on two-point modeling of hemodialysis urea kinetics. J Aw Soc Nephrol. 1996; 7:780-785.
Depner TA, et al. Dialyzer performance in the HEMO study: in vivo K0A and true blood flow determined from a model of cross-dialyzer urea extraction. ASAIO I. 2004; 50: 85-93.
Gotch FA. Evolution of the single-pool urea kinetic model [abstract]. Semin Dial. 2001; 14 (4): 252-256.
Gotch FA, et al. Mechanisms determining the ratio of conductivity clearance to urea clearance. Kidney Int Suppl. 2004; (89): S3-S24.
Leypoldt JK, Jaber BL, Zimmerman DL. Predicting treatment dose for novel therapies using urea standard Kt/V. Semin Dial. 2004; 17: 142-145.
Leypoldt JK, et al. Hemodialyzer mass transfer-area coefficients for urea increase at high dialysate flow rates. The Hemodialysis (HEMO) study. Kidney Int. 1997; 51: 2013-2017.
Lowrie EG, et al. The online measurement of hemodialysis dose (Kt): clinical outcome as a function of body surface area. Kidney Int. 2005; 68 (3): 1344-1354.
Melamed ML, et al. Retained organic solutes, patient characteristics and all-cause and cardiovascular mortality in hemodialysis: results from the retained organic solutes and clinical outcomes (ROSCO) investigators. BMC Nephrol. 2013; 14: 134.
McIntyre CW, et al. Assessment of haemodialysis adequacy by ionic dialysance: intra-patient variability of delivered treatment. Nephrol Dial Transplant. 2003; 18: 559-563.
Schneditz D, et al. Cardiopulmonary recirculation during dialysis. Kidney Int. 1992; 42: 1450.
Sirich TL, et al. Numerous protein-bound solutes are cleared by the kidney with high efficiency. Kidney Int. 2013;84:585-590.
Tattersall JE, et al. The post-hemodialysis rebound: predicting and quantifying its effect on Kt/V. Kidney Int. 1996;50:2094-2102.
Uhlin F, et al. Dialysis dose (Kt/V) and clearance variation sensitivity using measurement of ultraviolet-absorbance (on-line), blood urea, dialysate urea and ionic dialysance. Nephrol Dial Transplant. 2006; 21: 2225-2231.
Интернет-ссылки
KDOQI Hemodialysis Adequacy guidelines 2006. http://www.kidney.org.
Urea kinetic modeling calculators, http://www.ureakinetics.org.
Urea kinetic modeling channel, http://www.hdcn.com/ch/adeq/.
