- Диализному врачу
- 1. Ведение пациентов с ХБП 4-5-й стадии.
- 2. Подготовка к трансплантации, диализу или к консервативной терапии
- 3. Физиологические принципы и моделирование кинетики мочевины
- 4. Оборудование для гемодиализа и расходные материалы
- 5. Вода для диализа и диализирующий раствор
- 6. Артериовенозные фистулы и протезы. Основные положения
- 7. Центральный венозный катетер в качестве доступа: основы
- 8. Мониторинг артериовенозного доступа и осложнений
- 9. Инфекции и другие осложнения центральных венозных катетеров
- 10. Назначение острого гемодиализа
- 11. Назначение хронического гемодиализа
- 12. Осложнения в ходе процедуры гемодиализа
- 13. Повторное использование диализаторов
- 14. Антикоагуляция
- 15. Продленная заместительная почечная терапия
- 16. Гемодиафильтрация
- 17. Терапевтический аферез
- 18. Актуальность сорбционных технологий сегодня
- 19. Руководство по диализу
Мониторинг артериовенозного доступа и осложнений
В процессе использования артериовенозного (AV) доступа важнейшими факторами, ограничивающими его выживаемость, являются стеноз, тромбоз и инфекция. В целом осложнения чаще происходят при использовании AV-протезов, чем AV-фистул.
I. СТЕНОЗ. Стеноз сосудистого доступа является предшественником тромбоза, снижает кровоток по доступу и может привести к недодиализу. Наиболее частой причиной стеноза при протезах является неоинтимальная гиперплазия, которая развивается на анастомозе или непосредственно после него. Для AV-фистул локализация причины стеноза более разнообразна, хотя его типичным местом является регион вокруг анастомоза. Типичные места стеноза для фистул и протезов показаны на рис. 8.1 и 8.2. Поскольку выживаемость доступа значительно ниже после тромбэктомии, чем после избирательной ангиопластики, текущие рекомендации KDOQI предлагают проспективно отслеживать состояние AV-фистул и протезов на предмет гемодинамически значимого стеноза. Не все рекомендации предлагают рутинный мониторинг, поскольку существуют противоречивые данные в отношении клинических преимуществ программ наблюдения за доступом (Kumbar, 2012; Paulson, 2012). Рандомизированные исследования не всегда подтверждали улучшение исходов при протезах в результате проведения программ наблюдения; в отношении AV-фистул программы наблюдения снижают частоту тромбозов, но не увеличивают выживаемость фистулы в целом.
Существует несколько подходов для выявления стеноза до его прямой визуализации при допплер-УЗИ или для центральных вен - венографии. Эти ранние подходы основаны на непрямой оценке давления кровотока или рециркуляции в ходе сеанса диализа. В идеале программа раннего выявления стенозов должна отличаться для фистул и протезов, а также для предплечий и плеча. Основными принципами являются следующие. А. Рециркуляция по сосудистому доступу не проявляется, пока кровоток по доступу не приближается к кровотоку по экстракорпоральному контуру, тем самым неправильное расположение игл или непреднамеренная их смена не приведут к рециркуляции по доступу, пока кровоток по нему не упадет до 350-500 мл/мин. На этом уровне кровотока протезы находятся под высоким риском тромбоза. Поэтому, если выявляется реальная рециркуляция при использовании протеза, она является экстренным показанием для визуализации протеза и коррекции стеноза. С другой стороны, проходимость AV-фистул сохраняется при кровотоке 350-500 мл/мин, когда уже присутствует рециркуляция. Преимущество скринирования фистул в поисках рециркуляции по доступу относительно невелико в отношении предотвращения тромбозов, но полезно в предотвращении недодиализа. Стеноз доступа между обычными местами пункции не вызывает рециркуляции, но значимо снижает кровоток по доступу до уровней, способствующих тромбозу. Стеноз этой локализации следует заподозрить, когда измеренный кровоток по доступу оказывается ниже, чем скорость вращения насоса, но рециркуляция не выявляется. Б. Как в протезах, так и в фистулах часто развиваются стенозы на пути забора. Поэтому подходы по выявлению таких стенозов полезны для обоих доступов. В. Стенозы на путях возврата намного чаще развиваются при протезах, чем при фистулах на предплечье, где степень неоин-тимальной гиперплазии ниже и где вены на пути оттока часто компенсируют обструкцию главного канала потока. Однако в фистулах на предплечье стеноз на путях оттока не является необычным. Поэтому подходы по выявлению стенозов на путях оттока более полезны при мониторировании функции AV-протеза или фистулы на плече.
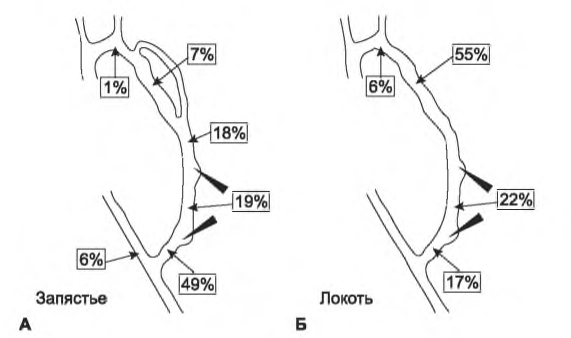
РИСУНОК 8.1. Типичные места стеноза артериовенозной фистулы. Представлены места стеноза для фистул, сформированных на запястье (А), и для фистул, созданных на плече (Б). Воспроизведено с разрешения из: Turmel-Rodrigues I, et al. Treatment of stenosis and thrombosis in haemodialysis fistulas and grafts by interventional radiology. Nephrol Dial Transplant. 2000; 15:2032-2036
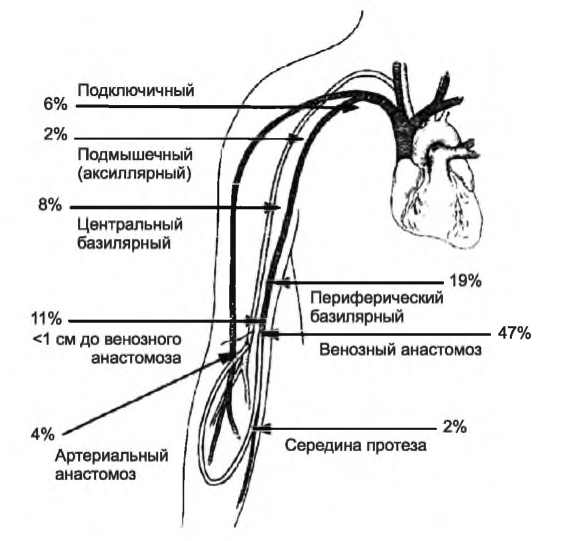
РИСУНОК 8.2. Типичные места стеноза артериовенозного протеза. Воспроизведено с разрешения Elsevier из: Roy-Chaudhury Р, et al. Vascular access in hemodialysis: issues, management, and emerging concepts. Cardiol Clin. 2005; 23: 249-273
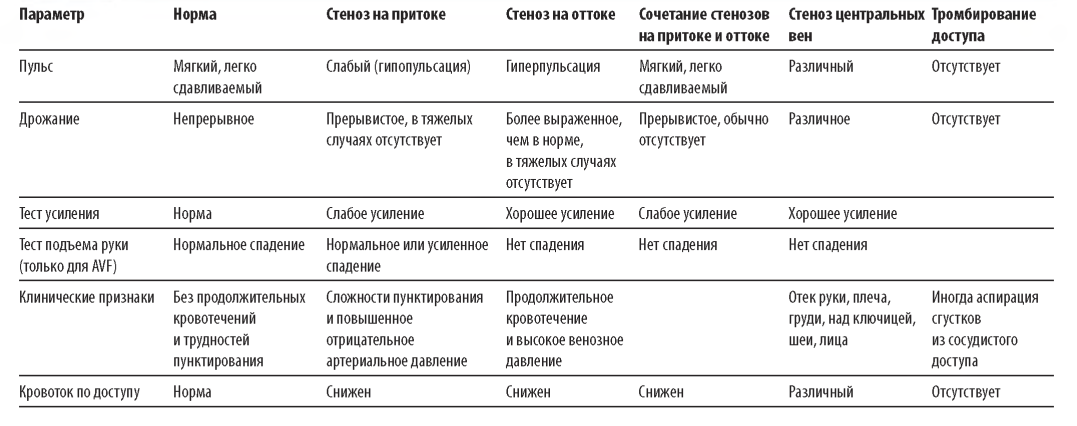
A. Физикальное обследование AV-доступа обсуждено в деталях в главе 6. В табл. 8.1 представлены изменения физикальных данных при типичных осложнениях доступа. Физикальное обследование может быть вполне полезно в выявлении изолированного стеноза на путях притока и оттока, но менее эффективно при комбинированном стенозе. Точность физикального обследования значимо выше у персонала, проходившего специальное обучение (Coentrao, 2012). Диализная сеть Техаса спонсировала ряд обучающих документов и примеров, доступных в Интернете (Beathard, 2012).
B. Наблюдение за доступом по параметрам, доступным в ходе каждого сеанса диализа. Многие аппараты обладают опцией по измерению in vivo ионного диализанса. У всех аппаратов мониторируется венозное давление на возврате крови. Наблюдение за трендами результатов этих измерений помогает выявить стеноз доступа.
1. Тренды ионного диализанса. Ионный диализанс, измеренный по кондуктивнос-ти, включает все компоненты рециркуляции по доступу в случае их наличия. По мере увеличения рециркуляции по доступу ионный диализанс будет снижаться, если сохраняются другие параметры назначения диализа (К0А диализатора, потоки крови и/или диализата, гепаринизация). Диализный аппарат, имеющий функцию измерения ионного диализанса, обеспечивает также измерение клиренса в ходе каждого сеанса (К) для расчета величины Kt (клиренс х время) для данной сессии. В небольшой серии наблюдений из 6 пациентов с фистулами сохраняющееся падение КТ на 20% было связано с рециркуляцией по сосудистому доступу (Fontsere, 2011). Другим подходом является оценка отношения ионного диализанса к кровотоку. В одном из исследований снижение этого отношения менее 0,5 было высокочувствительным и специфичным для рециркуляции по доступу (Mohan, 2010).
2. Тренд венозного давления на возврате. Венозное давление постоянно измеряется в ходе рутинного сеанса гемодиализа. Оно является функцией размера иглы, гематокрита (через эффект на вязкость крови) и скорости кровотока. При прочих равных условиях прогрессирующее увеличение венозного давления (за неделю-месяц) часто связано со стенозом на путях оттока (Zasuwa, 2010). База данных некоторых крупных диализных сетей позволяет отслеживать показатели венозного давления за продолжительное время; компания в США (Vase-Alert, Lafayette, IN) продает программное обеспечение для отслеживания состояния сосудистого доступа по динамике венозного давления. Можно также наблюдать за артериальным давлением до насоса, увеличение которого (в отрицательном направлении) будет свидетельствовать о нарастании стеноза на пути притока.
Таблица 8.1. Физикальные данные при различных формах дисфункции доступа
Чувствительность метода измерения давления в ходе диализа для выявления стеноза доступа можно увеличить, концентрируясь на измерении давления в начале диализа на низком кровотоке (200-225 мл/мин), поскольку при высоких кровотоках большая часть давления обуславливается сопротивлением иглы, а не ограничением сосудистого доступа. Исходное давление следует зафиксировать при первом использовании доступа. Пороговое давление, которое побуждает к дальнейшим исследованиям, зависит от размера иглы, вязкости крови и других факторов. Для иглы 15G стартовым пороговым венозным давлением могла бы быть величина выше 115-120 мм рт. ст., для игл 16G - выше 150 мм рт. ст. Такие пороговые значения должны быть превышены как минимум в ходе трех сеансов диализа, для того чтобы считаться значимыми.
С. Периодическое измерение кровотока по доступу. То, в какой степени низкий кровоток по доступу отражает стеноз и увеличение риска тромбоза, зависит от типа доступа. Кровоток по фистуле на предплечье обычно составляет 500-800 мл/мин, а по протезу - около 1000 мл/мин. Кровоток по фистуле или протезу на плече может быть существенно выше. Фистулы могут сохранять проходимость при кровотоках в 200 мл/мин, в то время как протезы тромбируются при кровотоках между 600 и 800 мл/мин - потоки, которые обеспечивают адекватный диализ, но указывают на предварительные признаки возможного риска тромбоза. Текущие рекомендации KDOQI (2006) предлагают направлять пациентов на визуализацию доступа, если кровотоки по фистуле составляют менее 600 мл/ мин, а по протезу - менее 1000 мл/мин и снизились за прошедшие 4 недели более чем на 25%. Хотя было показано, что регулярные наблюдения за сосудистым доступом на предмет стеноза снижают частоту тромбоза в сравнении с историческим контролем, современные проспективные исследования не показали убедительно, что выявление стеноза и коррекция его при помощи ангиопластики улучшают выживаемость протеза.
1. Прямое измерение кровотока по доступу разведением физраствором. Этот метод измерения кровотока по сосудистому доступу впервые был предложен Krivitski (1995). Требуемое оборудование создано Transonic Systems, Inc. (Ithaca, NY) и состоит из блока управления, двух связанных сенсоров потока/разведения, компьютера и программного обеспечения, а также передвижной стойки, которая легко позволяет перемещать оборудование от одного пациента к другому (рис. 8.3). В исходном положении, представленном на рис. 8.3, иглы находятся в нормальном соотношении. Для измерения скорости кровотока следует преднамеренно поменять артериальную и венозную магистрали, так чтобы кровоток в диализатор поступал из лежащей ниже по кровотоку иглы (рис. 8.4). Степень рециркуляции в такой системе зависит от соотношения кровотока по доступу и скорости кровотока по диализатору. Если процент рециркуляции и скорость кровотока по диализатору известны, можно рассчитать скорость кровотока по доступу.
Чтобы измерить количество (долю) рециркуляции в условиях переставленных магистралей, в кровь, покидающую диализатор, вводится болюс физраствора (рис. 8.4). Доля разведения в выходящей магистрали измеряется расположенным ниже по кровотоку ультразвуковым сенсором. Скорость прохождения звука по крови зависит от содержания протеина в плазме; следовательно, эффект разведения крови в оттекающей магистрали может быть оценен первым сенсором. Некоторое количество разведенной физраствором крови проходит затем по сегменту сосудистого доступа между двумя иглами и поступает во входящую (артериальную) магистраль. Доля разведения крови физраствором зависит от соотношения кровотока по доступу и кровотока по диализатору. Второй ультразвуковой сенсор на магистрали, ведущей к диализатору, используется для того, чтобы оценить эту пропорцию (рис. 8.4). На практике делается дополнительное измерение в условиях, когда магистрали не переставлены, чтобы оценить рециркуляцию в обычных условиях.
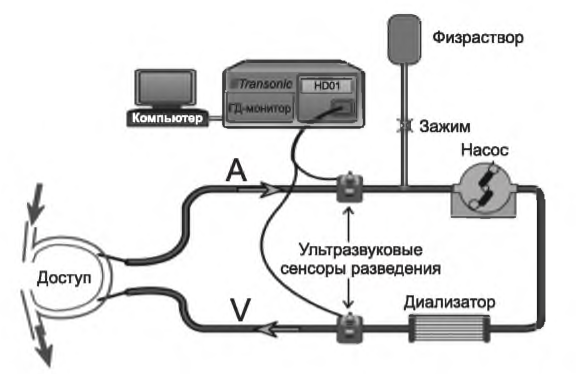
РИСУНОК 8.3. Установка для измерения рециркуляции по доступу по разведению физраствора на ультразвуковых детекторах. Для измерения кровотока по доступу подключение магистралей к иглам нужно поменять местами (не показано). Детали см. в тексте. Воспроизведено с разрешения Transonic Systems, Inc, Ithaca, NY
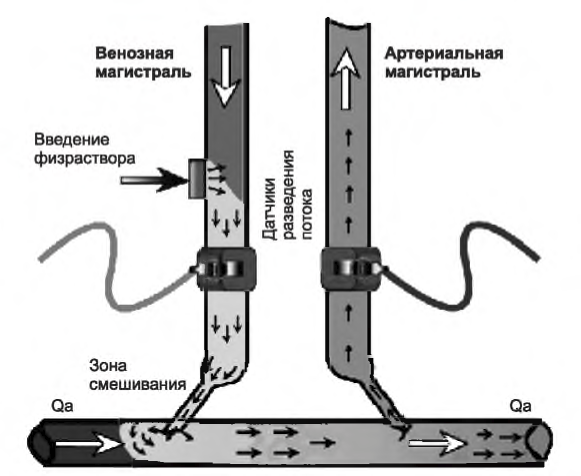
РИСУНОК 8.4. Измерение кровотока по доступу по разведению физраствором; показана перемена местами магистралей и положения датчиков. Детали см. в тексте. Воспроизведено с разрешения Transonic Systems, Inc, Ithaca, NY
2. Альтернативные методы оценки кровотока по изменению температуры, натрия или гемоглобина. Модуль температуры крови в аппарате компании «Фрезениус» имеет возможность на короткое время изменить температуру крови, проходящей через диализатор, а модуль ионной проводимости - на короткое время изменить концентрацию натрия в крови, вытекающей из диализатора. Это делается быстрыми измерениями температуры и проводимости диализирующего раствора и позволяет измерить скорость кровотока аналогично методу разведения физраствора. Магистрали меняются местами, температура оттекающей от диализатора крови или ее проводимость меняются, и рассчитывается мера воздействия этих изменений на кровь, поступающую на вход в диализатор за счет искусственной рециркуляции. Измерение повторяется без смены магистралей, в качестве контроля. Для оценки кровотока аналогичным образом использовалось разведение гемоглобина онлайн (Jiang, 2011; Roca-Tey, 2012). Получено свидетельство, что эти альтернативные методы вполне точны в измерении кровотока по доступу; возможно, температурный метод обеспечивает наилучшие результаты (Badr, 2014). Преимущество использования температуры или ионного диализанса состоит в том, что дополнительный ультразвуковой сенсор и отдельный компьютер не требуются.
D. Допплер-УЗИ для измерения кровотока по доступу. Хотя допплер-УЗИ обычно используется для выявления стеноза непосредственно, его можно также применить для измерения скорости кровотока по диализному доступу. Использовалось большое количество аппаратов и несколько алгоритмов для решения этого вопроса. При использовании некоторых из них происходила системная недо- или переоценка скорости кровотока. Точность измерения кровотока при допплер-УЗИ зависит от точности измерения как скорости, так и размера сосуда. Ее трудно добиться, когда кровоток турбулентный, а диаметр сосуда непостоянный. С учетом этого кровоток лучше измерять на плечевой артерии, где сосуд имеет относительно постоянный размер, а кровоток не турбулентный. Почти весь кровоток плечевой артерии (из примерной величины в 60-80 мл/мин) проходит через сосудистый доступ; кровоток по плечевой артерии коррелирует с кровотоком по доступу очень хорошо.
E. Давление внутри доступа (ДВД) и кровоток по доступу. Поток, давление и сопротивление математически связаны. В протезе ДВД обычно составляет менее 50% от САД (среднее артериальное давление). Наибольшая доля падения давления происходит на артериальном анастомозе, если нет стеноза внутри протеза. Когда развивается стеноз на выходе из протеза (например, в результате неоинтим альной гиперплазии на уровне протез-венозного анастомоза и сразу ниже), ДВД поднимается, и кровоток снижается. Когда ДВД поднимается выше 50% от САД (ДВД/САД>0,5), кровоток по доступу уменьшается до уровня склонности к тромбозу (600-800 мл/мин), что свидетельствует, скорее всего, о наличии стеноза. Детали этого расчета базируются на так называемом эквивалентном ДВД (скорректированном на относительную высоту точки измерения кровотока и датчика давления), они представлены в табл. 8.2. При AV-фистуле кровь возвращается в венозную систему через множество коллатералей, поэтому ДВД (которое обычно ниже, чем таковое при протезе) может не возрастать при наличии стеноза на канале оттока. Следовательно, это измерение менее ценно как инструмент наблюдения. Когда стеноз развивается в середине протеза, между зонами пункции артериальной и венозной иглы, ДВД в венозной игле может оставаться нормальным или даже снижаться, несмотря на нарастающий стеноз. Стеноз на артериальном анастомозе как протезов, так и фистул вызывает снижение ДВД, а широко открытый артериальный анастомоз приводит к высокому ДВД в отсутствие стеноза.

Таблица 8.2 Измерение отношения эквивалентного давления внутри доступа и среднего артериального давления
F. Рециркуляция по доступу. Для измерения рециркуляции использовались как методики, основанные на измерении мочевины, так и другие (например, разведение под контролем УЗИ). Методы, основанные на измерении мочевины, описаны в главе 3. Методы разведения описаны выше и могут использоваться для оценки рециркуляции. Для этого кровопроводящие магистрали не меняются местами, если кровоток, выходящий из диализатора, рециркулирует по доступу и разводит кровоток, входящий в диализатор, то болюс физраствора, введенный в выходную магистраль, вскоре после введения будет выявлен сенсором, расположенным на входной линии. Измерение рециркуляции по доступу при помощи температурного разведения использует температурный модуль, что обеспечивает результат, примерно схожий с методикой разведения под контролем ультразвука. Критическим значением, побуждающим к дальнейшим исследованиям, являются величины рециркуляция в 10% (2-игольный метод, основанный на мочевине), 5% (метод разведения под контролем ультразвука) и 15% (термальное разведение).
II. ВИЗУАЛИЗАЦИЯ СОСУДИСТОГО ДОСТУПА
А. Допплер-УЗИ. Эта неинвазивная методика позволяет непосредственно представить кровоток по протезу или фистулу. Она полезна в выявлении стенозов и картировании аневризм. Измерение скорости кровотока относительно дорого для рутинной практики. Его ключевая роль состоит в оценке кровотока и анатомии доступа среди пациентов, скринированных при помощи других методик.
B. Ангиография. Многие центры направляют пациентов с высокой вероятностью стеноза, выявленного дешевыми методами, непосредственно на ангиографию и баллонную ангиопластику, пропуская допплер-УЗИ. Следует использовать самую низкую из возможных доз контрастных веществ, по возможности - в разведении. Ангиографию можно ограниченно использовать для визуализации артериального дерева.
C. Магнитно-резонансная ангиография (МРА). Европейские рекомендации по наилучшей клинической практике (2007 г.) предлагают МРА для визуализации сосудистого доступа, когда необходимо представить как венозную, так и артериальную часть сосудистого дерева (Tordoir, 2007). Они цитируют несколько исследований, где МРА была успешно применена для визуализации доступа. Частота нефрогенного системного фиброза, связанного с гадолинием, снизилась с введением новых контрастных препаратов (Coca and Perazella, 2011), но кумулятивный риск множественных MPA-процедур у диализных пациентов остается неоцененным.
III. ЧРЕСКОЖНЫЕ ВМЕШАТЕЛЬСТВА ПОСЛЕ ВЫЯВЛЕНИЯ СТЕНОЗА. При выявлении стеноза более 50% следует выполнить чреспросветную ангиопластику или хирургическую ревизию доступа, если присутствуют следующие критерии: а) отклонения при физикальном обследовании, б) тромбозы в анамнезе, в) снижение скорости кровотока, г) повышенное или растущее статичное давление внутри доступа (нормализованное по САД). Опыт каждого центра должен учитываться при выборе процедуры. Если потребовались повторные ангиопластики в течение короткого периода, следует рассмотреть хирургическое вмешательство.
В большинстве центров вмешательства, связанные с сосудистым доступом, проводятся хирургами или интервенционалистами. Большое число центров в США в настоящее время предлагают нефрологам формальный тренинг в технике чрескожной ангиопластики и тромбэктомии. Поскольку нефрологи имеют иной клинический взгляд на пациента и связанные с сосудистым доступом проблемы, прямое их вовлечение во вмешательство может минимизировать отсрочки, снизить госпитализации и стоимость лечения, а также улучшить общую удовлетворенность пациентов.
A. Коррекция ранних дисфункций AV-фистулы. Существенная доля (10-35%) фистул не развивается до удовлетворительного состояния и неспособна поддерживать диализ. Главными виновниками являются стеноз сосудов или наличие заметного побочного венозного сброса (дополнительные венозные ветви отходят от главного ствола и компрометируют фистулу). Из двух этих проблем стеноз обуславливает 70% случаев несозревания фистулы. В большинстве случаев стеноз будет выявлен вблизи анастомоза. Чрескожная баллонная ангиопластика может успешно исправить это нарушение и восстановить большинство фистул, которые в противном случае будут утрачены. В случае задержки созревания из-за побочных венозных сбросов применяется процедура облитерации при помощи трех методик: чрескожное лигирование, оперативное отсечение вен или введение спирали.
B. Измерение кровотока непосредственно после ревизии. Иногда радиографическая коррекция явного стеноза не приводит к увеличению скорости кровотока. В других случаях кровоток первоначально возрастает, но затем падает до исходного уровня в течение 1-2 дней от процедуры. Измерение скорости кровотока немедленно после ревизии или ангиопластики полезно в отношении оценки вероятности того, что доступ останется функционирующим на клинически полезный период.
С. Эндоваскулярные стенты и сосудистый стеноз. Эндоваскулярные стенты занимают важное место в лечении стеноза сосудистого доступа. Стенты используются преимущественно при стенозах протезов, расположенных непосредственно на протез-венозном анастомозе или сразу после него. Стенты также используются в коррекции псевдоаневризм (см. ниже). Стенты протезов - металлические, покрытые изнутри, снаружи или с обеих сторон PTFE. Большое рандомизированное исследование продемонстрировало лучшие исходы лечения стенозов с использованием стентов в сравнении с ангиопластикой (Haskal, 2010). Первичная 6-месячная проходимость стентированных протезов (51%) была лучше, чем при изолированной ангиопластике (23%; р < 0,001). Необычно для диализного доступа сочетание нескольких стенозов, но выигрыш от коррекции главного нарушения может быть ослаблен присутствием дополнительного стеноза, который может потребовать установки дополнительного стента. Дополнительную стоимость эндоваскулярного стентирования необходимо соотнести со стоимостью ангиопластики или первичной хирургической коррекции.
IV. ТРОМБОЗЫ. Тромбозы являются наиболее частым осложнением артериовенозного доступа и обуславливают 80-85% случаев его утраты. Первичная проходимость протеза составляет 40-50% через 1 год и 25% - через 2 года. Причины тромбоза включают в себя стаз кровотока, повреждение эндотелия и нарушение свертываемости, но дополнительными факторами являются артериальный стеноз, сдавление фистулы, образование гематом, гиперволемия, гипотония и состояние гиперкоагуляции. При физикальном исследовании выявляется отсутствие шума и дрожания (табл. 8.1). Как эндоваскулярные методики (механические и/или фармакологические), так и хирургические эффективны в разрешении тромбозов. В случаях повторных тромбозов важно искать причины тромбоза, не связанные со стенозом.
A. Предрасполагающие факторы. Возрастающее число диализных пациентов имеют склонность к усилению гемостаза, включая повышенный уровень фибриногена, сниженные уровни протеина S или С, лейденскую мутацию 5-го фактора, присутствие волчаночного антикоагулянта или повышенный гематокрит в результате терапии эритропоэтином. Данные, связывающие эти факторы с повышенной частотой тромбозов, противоречивы. Использование варфарина проблематично, поскольку в условиях дефицита протеина S или С, или даже без него, использование варфарина способствует возникновению кальцифи-лаксии с некрозами кожи. Использование варфарина трудно мониторировать у пациентов с волчаночным антикоагулянтом, поскольку протромбиновое время является в этом случае ненадежной сферой антикоагуляции.
B. Предотвращение. Терапия антикоагулянтами или антиагрегантами может помочь предотвратить тромбоз доступа, но большинство исследований, опубликованных к настоящему времени, не поддерживают их рутинное использование. Отдельные рандомизированные исследования, как с варфарином в низкой дозе (целевой МНО 1,4-1,9), так и клопидогрелем в сочетании с аспирином против плацебо у пациентов с PTFE-протезами, не смогли продемонстрировать снижение частоты тромбозов или удлинение выживаемости протеза. Оба исследования показали клинически и статистически значимые осложнения в виде кровотечений у леченных пациентов. Однако другое рандомизированное исследование выявило снижение относительного риска тромбозов у пациентов с вновь установленными протезами, леченными дипиридамолом. Метаанализ, оценивающий полезность антиагрегантной терапии для предотвращения утраты сосудистого доступа, включавший 21 исследование, продемонстрировал защитный эффект в отношении тромбоза фистул и их проходимости, но отсутствие эффекта в отношении протезов (Palmer, 2013).
С. Лечение
1. Тромбозы фистулы. Тромбозы фистулы происходят или вскоре после их создания или как позднее осложнение. Пациентов следует обучать проверять фистулу ежедневно. Ранние тромбозы являются результатом технических факторов и почти всегда требуют хирургического или чрескожного вмешательства, хотя могут быть следствием непреднамеренного сдавления во время сна. Поздним тромбозам в большинстве случаев предшествует снижение кровотока, хотя гипотония и гиперкоагуляция могут также спровоцировать тромбоз в отсутствие предшествующей тенденции к снижению кровотока. Лечение тромбозов может быть сложным, должно проводиться с использованием чрескожных методов или хирургической тромбэктомии, в зависимости от опыта каждого центра. Наилучшим результатом характеризуются техники, предусматривающие удаление всего тромба целиком (Palmer, 2006).
2. Протезы. Тромбозы можно лечить хирургической тромбэктомией или тромболизисом (механическим или фармакомеханическим) - также в зависимости от опыта центра. Лечение следует проводить немедленно, чтобы избежать использования временного доступа. Вся зона кровотока по доступу должна быть тщательно обследована во время вмешательства. Остаточные стенозы, превышающие 85%, следует исправлять баллонной ангиопластикой или хирургической ревизией. Роль антиагрегантных препаратов или варфарина у пациентов с повторными тромбозами неясна. Пациентов следует обучать избегать внешнего сдавления протеза, необходимо оценивать гиперкоагуляцию и наличие отсроченной гипотонии после диализа. Рутинное наблюдение за протезом необходимо восстановить сразу после успешного лечения. У пациентов с неудачными тромбэктомией или тромболизисом следует предпринять хирургическое вмешательство, ориентированное на создание вторичной фистулы из вен, дренировавших протез. Создание таких фистул возможно из-за расширения вен и утолщения их стенки благодаря существовавшему протезу; их использование в качестве фистулы возможно очень скоро после ее создания. Рекомендации KDOQI предлагают рассматривать возможность создания вторичной фистулы в каждом случае утраты протеза.
V. ИШЕМИЯ КОНЕЧНОСТИ С AV-ДОСТУПОМ. Связанная с диализом ишемия конечности, обычно обозначаемая как синдром обкрадывания, осложняет 1-20% доступов и может привести к болям, утрате функции или даже к потере конечности. Одним из механизмов ишемии является артериальное обкрадывание в результате ретроградного тока в дистальную артерию по направлению к доступу, но свой вклад может вносить артериальный стеноз или дистальная артериолопатия, вовлекающая малые сосуды. Фактором риска является расположение доступа на плече, болезнь периферических артерий или диабет.
А. Выявление. Пациентов с установившейся фистулой следует оценивать ежемесячно по событиям за прошедший месяц и физикальным обследованиям. Клинически это боли, жалобы на то, что мерзнут руки, дистальные парестезии, особенно в ходе диализа, что может усиливаться до возникновения цианоза, отсутствия пульса, ишемических язв и даже сухой гангрены, развивающихся за дни, недели или месяцы. Начало может быть немедленным после создания доступа или постепенным, за дни и недели. Обследование требует сравнения температуры, пульса и функции другой руки.
Измерение давления, чрескожная оценка оксигенации или артериография (с открытым и прижатым доступом) полезны в обследовании, но не являются необходимыми всегда. Диагноз базируется на клинических симптомах и признаках, а также на демонстрации ухудшения циркуляции в конечности. Дифференциальный диагноз включает: синдром карпального туннеля, периферические болезни сосудов, нейропатию, травмы нерва или ишемическую мононейропатию в результате утраты кровоснабжения нерва.
В. Лечение. Легкую ишемию, которая манифестируется холодными руками или парестезиями, но без сенсорных и моторных нарушений, можно вести выжидательно. Боли в руке при нагрузке в результате эффекта обкрадывания (или в крайних случаях в покое) или появление незаживающих язв обычно требуют хирургического вмешательства. Утрата моторной функции руки является неотложным показанием для немедленного ушивания или перевязки доступа.
1. Процедура DRIL (distal revascularization interval ligation). При типичной луче-головной фистуле, созданной бок-в-бок, анастомоз лучевой артерии часто вызывает обкрадывание системы локтевой артерии. Перевод анастомоза из позиции «бок артерии» в позицию «конец артерии» может иногда уменьшить ишемию вследствие обкрадывания. Тяжелые случаи синдрома обкрадывания требуют перевязки AV-фистулы, но процедура дистальной реваскуляризации с интервальным лигированием (DRIL) может разрешить ишемию при сохранении проходимости фистулы. Вмешательство предполагает перевязку артерии непосредственно дистальнее исходной фистулы и создание сброса по реверсированной большой подкожной вене из артерии проксимальнее анастомоза в артерию дистальнее места лигирования. В одном исследовании показано, что эффективность DRIL выше, если байпас из вены начинается достаточно высоко над фистульным анастомозом, чтобы избежать формирования зоны пониженного давления в артерии над фистульным анастомозом (Kopriva, 2014).
2. Ушивание. Обкрадывание вследствие высокого кровотока можно скорректировать ушиванием анастомоза, что может быть сделано минимально инвазивной процедурой (Miller, 2010).
3. Другие процедуры. Лечение отека руки после наложения AV-фистулы состоит в переводе анастомоза из позиции «бок вены» в позицию «конец вены» или селективной перевязке вен. Небольшое увеличение окружности руки (на 2-3 см) после наложения доступа является обычным результатом, но большее увеличение указывает на венозную гипертензию, обычно в результате стеноза центральных вен.
VI. ПСЕВДОАНЕВРИЗМА. Травмирование доступа повторными пунктированиями в тех же самых областях может вызвать повреждение всех слоев вены или материала протеза. Большие аневризмы могут препятствовать адекватной установке игл и ограничивать места возможных пункций. Эти расширения могут увеличиваться еще больше, особенно если присутствует стеноз ниже по кровотоку, вызывая повышенное давление внутри доступа. Аневризмы и псевдоаневризмы имеют склонность к инфицированию и могут способствовать тромбозу. Главным опасением является риск разрыва, способный к фатальному кровотечению. Признаки угрожающего разрыва включают в себя истончение кожи, продолжительное кровотечение или изъязвление поверхности и быстрое увеличение аневризмы. Раннее вмешательство критично для предотвращения этих осложнений.
A. Фистула. Псевдоаневризмы наблюдаются значительно чаще, чем истинные аневризмы. Они являются следствием несоблюдения требования смены места пункции, неадекватного гемостаза или гематом, возникающих при удалении иглы. Большинство псевдоаневризм и истинных аневризм ведутся консервативно при исключении пункции фистулы в этой зоне; в некоторых случаях требуется хирургическая коррекция.
B. Протез. В случае протеза невозможно истинное расширение просвета сосуда. Стенка псевдоаневризмы формируется слоями наружных мягких тканей. Требуется иссечение псевдоаневризмы и укрепление стенки протеза, если она быстро расширяется, превышает 12 мм в диаметре и/или угрожает жизнеспособности лежащей над ней кожи. Псевдоаневризму протеза следует исправить хирургически, если она ограничивает число мест возможной пункции или вызывает симптоматику (боль или пульсацию).
C. Стенты. Стенты используются для чрескожного лечения псевдо аневризмы (Fotiadis, 2014). Хотя это приводит к немедленному выключению псевдоаневризмы, повторное ее образование и повреждение стент-протеза в результате повторных проколов остается большой проблемой. Сломанные балки стента могут иногда выходить сквозь кожу, создавая угрозу для персонала, работающего с этими пациентами. Выключение псевдоаневризмы при помощи стент-протеза представляет собой его использование не по показаниям («off-label»). Существует также риск инфицирования стент-протеза. Безопасность его пунктирования не была подтверждена в проспективных исследованиях. Аналогично роль хирургических вмешательств в лечении псевдоаневризмы напрямую не сравнивалась с использованием стент-протезов. Этот подход представляет собой метод спасения в случае сосудистых разрывов, связанных с ангиопластикой. Полный разрыв является одной из ситуаций, в которых стент-протез показан, поскольку это стабилизирует доступ и снимает потребность в немедленном хирургическом вмешательстве.
VII. ИНФЕКЦИИ. Инфекции сосудистого доступа обычно проявляются покраснением, болью или гнойным экссудатом из мест пунктирования. Часто первым признаком является лихорадка без других очевидных источников и положительные результаты посевов. Доступ не следует использовать, если он инфицирован. Следует взять посевы крови или содержимого раны (если имеется) и начать терапию антибиотиками. Следует оценить возможность эндокардита или других источников инфекции, в зависимости от обнаруженного патогена, особенно если посевы не становятся стерильными на фоне антибактериальной терапии. Ультразвуковое исследование окружающих мягких тканей иногда полезно в выявлении скопления жидкости. Инфицированный доступ обычно требует хирургического вмешательства для излечения или иссечения.
А. Фистулы. Инфекции являются редкими и обычно вызываются стафилококками. Их следует лечить, как и подострый эндокардит, назначением антибиотиков на 6 недель. Диагноз устанавливается на основе местных признаков воспаления. Неотложная терапия антистафилококковыми средствами часто эффективна; терапию начинают после посевов крови и местного отделяемого. Септическая эмболия в ходе терапии требует удаления фистулы.
В. Протез. Инфицирование протезов происходит в 5-20% случаев, а число инфекции бедренных протезов еще выше. Профилактическую антибактериальную терапию следует проводить у пациентов, проходящих процедуры, способные вызвать бактериемию (удаление зуба или гинекологические манипуляции). Большинство инфекций вызывается стафилококками. Грамотрицательные микроорганизмы (.Escherichia coli) можно высеять при бедренных протезах (На-rish and Allon, 2011). Начальная антибактериальная терапия должна покрывать грамоположительные и грамотрицательные микроорганизмы и энтерококки. Местное инфицирование протеза лечится антибактериальными препаратами (на основе посевов) и иссечением инфицированного сегмента. Распространенная инфекция требует полного удаления протеза.
Септицемия может развиться без местных признаков. В таких случаях сканирование с лейкоцитами, меченными технецием, может помочь выявить инфекцию протеза; перед сканированием необходимо удалить все пропитанные кровью перевязочные материалы, поскольку они могут дать ложноположительный результат. В случае разрыва инфицированного протеза может произойти кровотечение. Протез, который инфицировался в течение 30 дней от установки, возможно, следует удалить.
1. Немые инфекции в тромбированных протезах. Старые тромбированные протезы могут инфицироваться без явных местных признаков; вероятно, такие протезы следует удалять сразу после прекращения их использования. Они могут являться причиной повышенного уровня ЦРБ и резистентности к терапии эритропоэтином. Однако поскольку хирургическое удаление требует значительного иссечения тканей, эта проблема требует дальнейшего исследования, перед тем как можно будет дать твердые рекомендации.
VIII. СЕРДЕЧНАЯ НЕДОСТАТОЧНОСТЬ. Сердечная недостаточность является необычным осложнением доступа на предплечье, но может развиться у пациентов с фистулами плеча или бедра, особенно если у них есть сопутствующее заболевание сердца. Хотя считается, что долгосрочное существование фистулы, как правило, не влияет на сердечные функции, закрытие сосудистого доступа было связано с уменьшением массы левого желудочка и улучшением признаков левожелудочковой концентрической и эксцентрической гипертрофии (Movilli, 2010). Повышенный кровоток в легких (который связан с высоким потоком по доступу) может усилить легочную гипертензию.
Некоторые доступы демонстрируют постепенное увеличение кровотока по ним. Существует риск сердечной недостаточности с высоким выбросом, когда кровоток по доступу превышает 20% сердечного выброса. Плечевой доступ и доступ с кровотоком более 2 л в минуту увеличивает такие риски (Stern and Klemmer, 2011). В этих случаях следует рассмотреть ушивание доступа для снижения кровотока (Miller, 2010). Несмотря на теоретические преимущества временного закрытия доступа, следует предпочесть хирургическое сужение или ушивание, когда исследования показывают значимое изменение сердечного выброса. У пациентов с необъяснимым высоким сердечным выбросом следует оценить и скорректировать возможную анемию. Использование вазодилататоров, таких как миноксидил или гидролазин без бета-блокады, является другой частой корректируемой причиной высокого сердечного выброса. Наконец, перегрузка жидкостью типична для диализных пациентов, и ее следует исключить у пациентов с симптомами и признаками сердечной недостаточности.
IX. ОСЛОЖНЕНИЯ ЧРЕСКОЖНЫХ ВМЕШАТЕЛЬСТВ. Наиболее частым осложнением, связанным с ангиопластикой, является разрыв сосуда, что проявляется излитием контраста и/или кровотечением. Это осложнение относительно часто (2%) и может проявляться от клинически не значимого до тяжелого. Субклиническое излитие контраста в месте ангиопластики обычно не вызывает беспокойства. В легких случаях разрыва сосуда может развиться гематома, но пациент не демонстрирует симптоматики. Большие гематомы могут нарушить кровоток по доступу, а очень большие гематомы - привести к полному или почти полному разрыву вены. В таких случаях введение внутрисосудистого стента может быть полезным для остановки кровотечения.
Другим осложнением ангиопластики является воздушная эмболия, особенно во время тромбэктомии. Клинически значимая воздушная эмболия происходит редко. Дистальная эмболизация, или тромбоз артерии, может произойти во время тромбэктомии; в этих случаях тромб следует немедленно удалить эмболэктомическим катетером.
X. КЛИНИЧЕСКИЕ ЦЕЛИ И МОНИТОРИНГ
А. Создание команды сосудистого доступа и программа постоянного улучшения качества. Для благополучного существования сосудистого доступа важно взаимодействие команды, состоящей из нефролога, хирурга, интервенциониста, координатора сосудистого доступа и диализного персонала. В идеале такая команда должна регулярно встречаться и рассматривать результаты работы на основе критериев качества в соответствии с рекомендациями KDOQI. Собираемые данные должны включать в себя число и тип созданных сосудистых доступов, частоту инфекции и тромбозов, число и тип проведенных вмешательств и время до утраты доступа. Центрам следует следить за исходами после тромбозов и устанавливать минимальные цели для непосредственной и долгосрочной проходимости доступов. Необходимо анализировать тенденции и обеспечивать информацией всю команду. Такой подход облегчает своевременные действия и обеспечивает сохранение, а не восстановление сосудистых доступов, помогая минимизировать использование венозных катетеров и обеспечить проведение адекватного диализа.
Ссылки и рекомендуемая литература
Agarwal АК, Asif A. Interventional Nephrology. Washington, DC: American Society of Nephrology, NephSAP; 2009.
Asif A, et al., eds. Textbook of Interventional Nephrology. New York, NY: McGraw Hill; 2012.
Ayus AC, Sheikh-Hamad D. Silent infections in clotted hemodialysis access grafts. I Am Soc Nephrol. 1998; 9: 1314-1317.
Badr B, et al. Transonic, thermodilution, or ionic dialysance to manage vascular access: which method is best? Hemodial Int. 2014; 18: 127-135.
Beathard GD. A practicioners resource guide to physical examination of the vascular access. ESRD Network of Texas; 2012. http://www.esrdnetl5.org/QI/C5D.pdf.
Besarab A, et al. Simplified measurement of intra-access pressure. ASAIO I. 1996; 42: M682-M687.
Besarab A, et al. The utility of intra-access monitoring in detecting and correcting venous outlet stenoses prior to thrombosis. Kidney Int. 1995; 47: 1364-1373.
Besarab A, Sherman R. The relationship of recirculation to access blood flow. Am I Kidney Dis. 1997; 29: 223229.
Campos RP, et al. Stenosis in hemodialysis arteriovenous fistula: evaluation and treatment. Hemodial Int. 2006; 10: 152-161.
Chemla ES, et al. Complex bypasses and fistulas for difficult hemodialysis access: a prospective, single-center experience. Semin Dial. 2006; 19: 246-250.
Chin Al, et al. Intra-access blood flow in patients with newly created upperarm arteriovenous native fistulas for hemodialysis access. Am J Kidney Dis. 2004; 44: 850-858.
Coca SG, Perazella MA. Use of iodinated and gadolinium-containing contrast media. In: Daugirdas JT, ed. Handbook of Chronic Kidney Disease Management. Philadelphia, PA: Kluwer; 2011: 363-375.
CoentrSo L, Faria B, Pestana M. Physical examination of dysfunctional arteriovenous fistulae by non-interven-tionalists: a skill worth teaching. Nephrol Dial Transplant. 2012; 27: 1993-1996.
Crowther MA, et al. Low-intensity warfarin is ineffective for prevention of PTFE graft failure in patients on hemodialysis: a randomized controlled trial. Am J Soc Nephrol. 2002; 13 (9): 2331-2337.
Depner TA, Krivitsky NM, MacGibbon D. Hemodialysis access recirculation measured by ultrasound dilution. ASAIO J. 1995; 41: M749-M753.
Fontsere N, et al. Practical utility of on-line clearance and blood temperature monitors as noninvasive techniques to measure hemodialysis blood access flow. Blood Purif. 2011; 31: 1-8.
Fotiadis N, et al. Endovascular repair of symptomatic hemodialysis access graft pseudoaneurysms. J Vase Access. 2014; 15: 5-11.
Gradzki R, et al. Use of ACE inhibitors is associated with prolonged survival of arteriovenous grafts. Am J Kidney Dis. 2001; 38: 1240-1244.
Harish A, Allon M. Arteriovenous graft infection: a comparison of thigh and upper extremity grafts. Clin J Am Soc Nephrol. 2011; 6: 1739-1743.
Haskal ZJ, et al. Stent graft versus balloon angioplasty for failing dialysis access grafts. N Engl J Med. 2010; 362: 494-503.
Huijbregts HJ, Blankestijn PJ. Dialysis access - guidelines for current practice. Eur J Vase Endovasc Surg. 2006; 31:284-287.
Jiang SH, et al. Validation of the measurement of haemodialysis access flow using a haemoglobin dilution test. Blood Pur if. 20 IE 32:48-52.
Kaufman JS, et al. Randomized controlled trial of clopidogrel plus aspirin to prevent hemodialysis access graft thrombosis. J Am Soc Nephrol. 2003; 14: 2313-2321.
Kopriva D, McCarville DJ, Jacob SM. Distal revascularization and interval ligation (DRIL) procedure requires a long bypass for optimal inflow. Can J Surg. 2014; 57: 112-115.
Krivitski NM. Theory and validation of access flow measurement by dilution technique during hemodialysis. Kidney Int. 1995;48:244-250.
Kumbar L, Karim J, Besarab A. Surveillance and monitoring of dialysis access. Int J Nephrol. 2012; 2012:649735.
Lok CE, et al. Reducing vascular access morbidity: a comparative trial of two vascular access monitoring strategies. Nephrol Dial Transplant. 2003; 18: 1174-1180.
Maya ID, et al. Vascular access stenosis: comparison of arteriovenous grafts and fistulas. Am J Kidney Dis. 2004; 44: 859-865.
Miller GA, et al. The MILLER banding procedure is an effective method for treating dialysis-associated steal syndrome. Kidney Int. 2010; 77: 359-366.
Mohan S, et al. Effective ionic dialysance/blood flow rate ratio: an indicator of access recirculation in arteriovenous fistulae. ASAIO I. 2010; 56: 427-433.
Movilli E, et al. Long-term effects of arteriovenous fistula closure on echocardiographic functional and structural findings in hemodialysis patients: a prospective study. Am J Kidney Dis. 2010; 55: 682-689.
National Kidney Foundation. K/DOQI clinical practice guidelines for vascular access: update 2006. Am J Kidney Dis. 2006; 48 (suppl 1): S188-S306.
Oakes DD, et al. Surgical salvage of failed radiocephalic arteriovenous fistulas: techniques and results in 29 patients. Kidney Int. 1998; 53: 480-487.
Ohira S, Коп T, Imura T. Evaluation of primary failure in native AB-fistulae (early fistula failure). Hemodial Int. 2006; 10: 173-179.
Ortega T, et al. The timely construction of arteriovenous fistulas: a key to reducing morbidity and mortality and to improving cost management. Nephrol Dial Transplant. 2005; 20: 598-603.
Palmer RM, et al. Is surgical thrombectomy to salvage failed autogenous arteriovenous fistulae worthwhile? Am Surg. 2006; 72: 1231-1233.
Palmer SC, et al. Antiplatelet therapy to prevent hemodialysis vascular access failure: systematic review and meta-analysis. Am J Kidney Dis. 2013; 61: 112-122.
Paulson WD, Moist L, Lok CE. Vascular access surveillance: an ongoing controversy. Kidney Int. 2012; 81: 132-142.
Rayner HC, et al. Vascular access results from the Dialysis Outcomes and Practice Patterns Study (DOPPS): performance against Kidney Disease Outcomes Quality Initiative (K/DOQI) Clinical Practice guidelines. Am J Kidney Dis. 2004; 44 (5 suppl 3): 22-26.
Roca-Tey R, et al. Five years of vascular access stenosis surveillance by blood flow rate measurements during hemodialysis using the Delta-H method. J Vase Access. 2012; 13: 321-328.
Saran R, et al. Association between vascular access failures and the use of specific drugs: the Dialysis Outcomes and Practice Patterns Study (DOPPS). Am I Kidney Dis. 2002; 40: 1255-1263.
Sessa С, et al. Treatment of hand ischemia following angioaccess surgery using the distal revascularization interval-ligation technique with preservation of vascular access: description of an 18-case series. Ann Vase Surg. 2004; 18:685-694.
Stern AB, Klemmer PJ. High-output heart failure secondary to arteriovenous fistula. Hemodial Int. 2011; 15: 104-107.
Tessitore N, et al. Clinical access assessment. J Vase Access. 2014; 15 (suppl 7): 20-27.
Tordoir J, et al. EBPG on vascular access. Nephrol Dial Transplant. 2007; 22 (suppl 2): ii88—ii 117.
White JJ, et al. Paulson relation between static venous pressure (VP), hemodialysis graft blood flow (Q), and stenosis: analysis by fluid mechanics model [Abstract]./Am Soc Nephrol. 2005; 16: F-PO531.
Zasuwa G, et al. Automated intravascular access pressure surveillance reduces thrombosis rates. Semin Dial. 2010;23:527-535.
Интернет-ссылки
An excellent teaching guide, introduction to vascular access, with pictures of anatomy, etc. http://www.fistula-first.org/atlas/index.html.
Information on interventional nephrology, annual meetings, credentialing, publications, and statement papers. http://www.as di n .org.
